本文由论文第一作者李黎明博士受邀协助撰写。
中枢神经系统在人体生命活动中发挥关键的调控作用,脊髓损伤(SCI)是严重的中枢神经系统疾病,往往致使患者损伤截断以下感觉和运动功能丧失,目前尚没有有效的临床治疗手段。复杂的抑制性病理微环境是阻碍神经修复的主要因素,对微环境的综合调节是治疗SCI的关键。高建青教授团队在前期研究中构建了黏附性多肽修饰的生物相容性水凝胶,携载间充质干细胞(Mesenchymal stem cell,MSC)进行移植,对全横断型SCI的治疗显示了良好的效果(ACS Applied Materials & Interfaces, 2017, 9(4): 3330.),团队还针对SCI抑制性微环境,利用抗氧化性MnO2纳米粒复合的水凝胶进行微环境的抗氧化和抗炎调节,从而促进移植后的MSC细胞存活与脊髓神经组织修复(ACS Nano, 2019, 13, 14283?14293)。近年研究发现,MSC的修复功能主要与其旁分泌作用有关,而干细胞在疾病微环境中较高的死亡率及潜在的长期安全问题限制了其疗效与应用。作为MSC细胞旁分泌物的天然载体,MSC来源的外泌体继承了MSC的神经营养和炎症、过氧化微环境调节等功能,因此,利用MSC外泌体替代MSC细胞进行脊髓损伤局部的移植,是极具前景的SCI治疗策略。由于SCI后组织中继发性损伤的持续进展与细胞外基质缺失,外泌体在脊髓损伤局部的高效递送与缓释成为调节微环境和促进神经修复的关键。
高建青教授团队将药剂学缓释埋植制剂的技术应用于组织再生与修复,通过层粘连蛋白来源多肽修饰的黏附性水凝胶三维携载MSC细胞外泌体,补充损伤组织细胞外基质的同时,进行外泌体在脊髓损伤局部的缓释递送移植。团队前期工作已证明层粘连蛋白来源的多肽PPFLMLLKGSTR可促进MSC细胞与脊髓组织在透明质酸(HA)水凝胶中的黏附生长,鉴于MSC外泌体膜上同样具有能与层粘连蛋白结合的整合素结构,在本研究中,高建青教授团队进一步合成了可黏附性携载外泌体的生物相容性水凝胶。实验表明,该水凝胶-外泌体三维体系的脊髓移植可实现外泌体在损伤脊髓组织中的保留和持续释放以及向远端脊髓组织的融合,从而改善炎症和过氧化微环境,促进神经组织修复,最终显著促进了SCI大鼠的运动功能恢复并减轻其神经源性膀胱损伤。
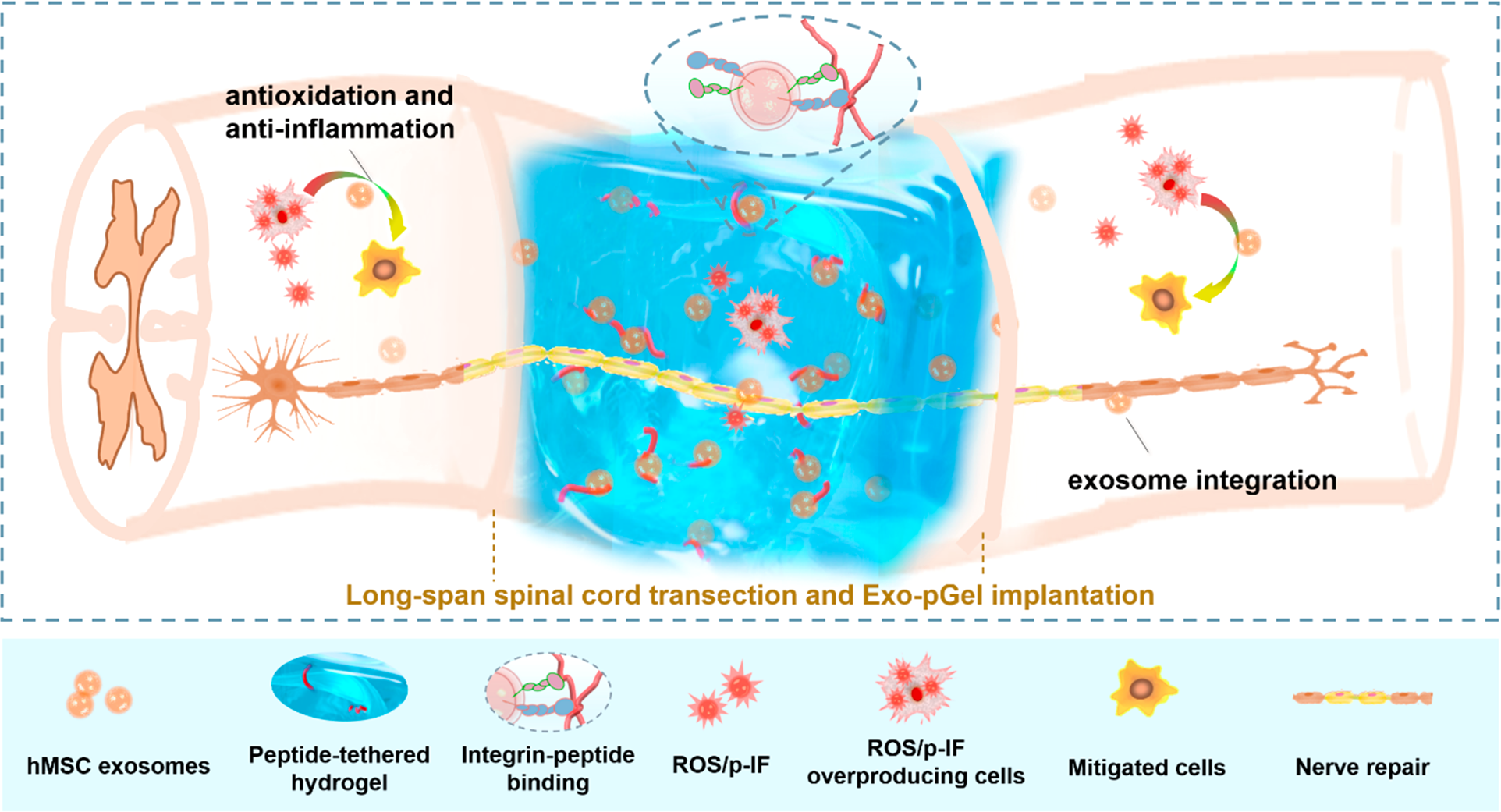
图1. 研究示意图。MSC细胞外泌体通过膜表面的整合素与水凝胶中的多肽结合从而黏附性包载于三维水凝胶中进行脊髓损伤部位的移植,移植体系持续释放外泌体以改善损伤微环境,从而促进神经组织修复。
研究团队采用基于尺寸排阻色谱原理的分离柱结合超速离心的方法成功提取获得纯化的MSC外泌体。分别合成醛基和氨基的修饰的HA,将层粘连蛋白来源的多肽PPFLMLLKGSTR与HA链上的部分醛基连接,利用席夫碱反应构建具有良好黏附性与生物相容性的水凝胶。肽修饰显著提高了水凝胶对MSC外泌体的包载效率,MSC外泌体于水凝胶中黏附并呈现三维空间分布,体外释放实验显示该体系可维持超过10天的外泌体释放。
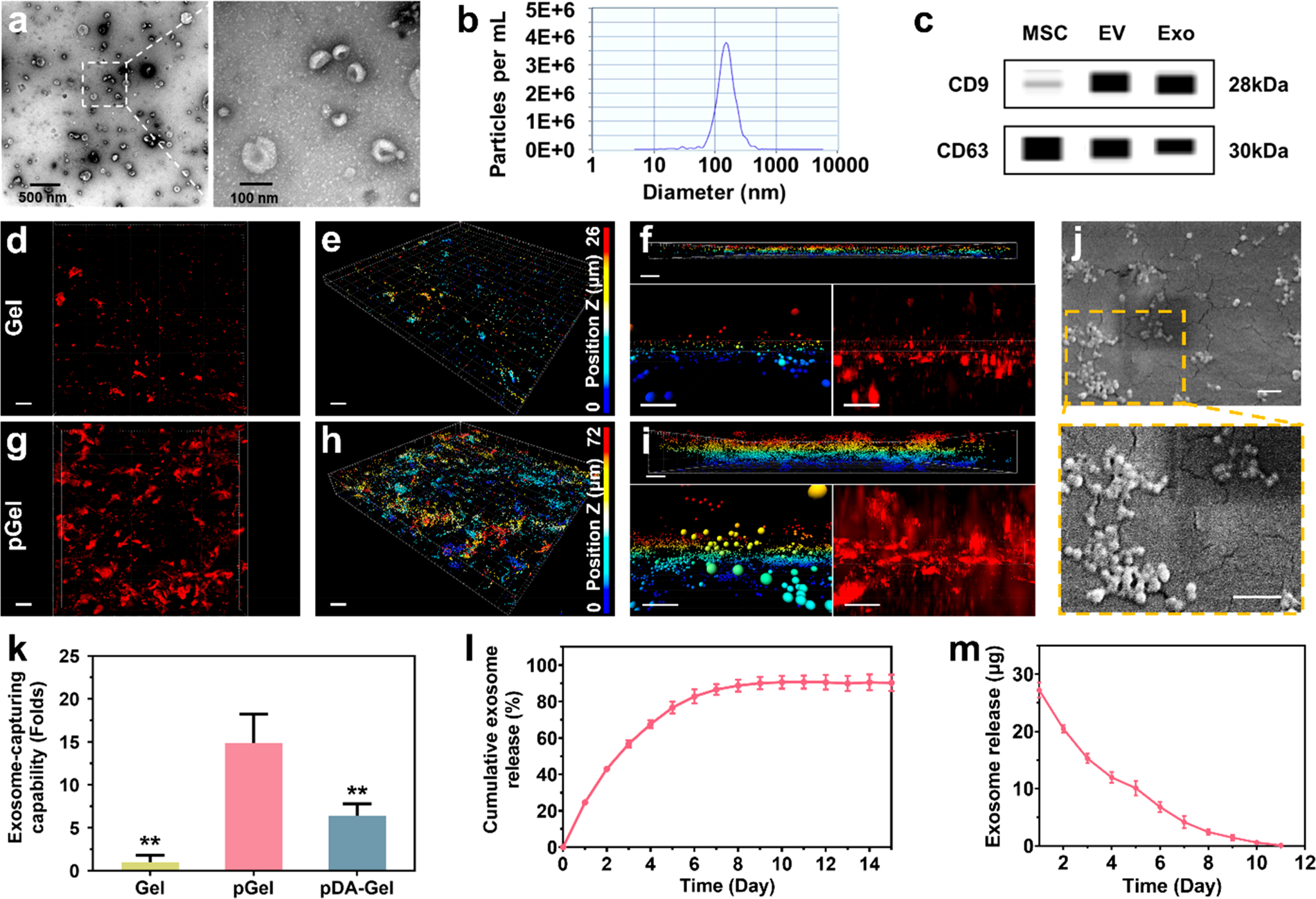
图2. 外泌体的表征与在水凝胶中的黏附分布和释放
团队在前期研究中构建了严重型的大鼠“大跨度”脊髓全横切损伤模型,将大鼠脊髓通过手术暴露后,在T9-T10节段处完全切断脊髓并制造4~5mm的断口,将外泌体-水凝胶体系(Exo-pGel)移植入断口部位进行脊髓修复治疗。在28天的治疗周期内,未进行移植治疗的SCI大鼠表现为后肢拖动的瘫痪状态,单独移植空白水凝胶(Blank)对于大鼠运动功能恢复具有一定促进效果,而Exo-pGel移植治疗的大鼠可实现后肢关节的大幅活动,表明该策略中局部递送的外泌体所发挥的神经修复作用。另外,对大鼠膀胱组织的考察表明,Exo-pGel移植治疗能够显著改善SCI后的神经源性膀胱损伤。对治疗后脊髓神经组织的解剖和免疫组化染色考察发现,Exo-pGel移植显著缓解了炎性和过氧化性的损伤微环境,有效抑制星形胶质细胞增生,促进了损伤的脊髓神经组织中神经纤维的生长。
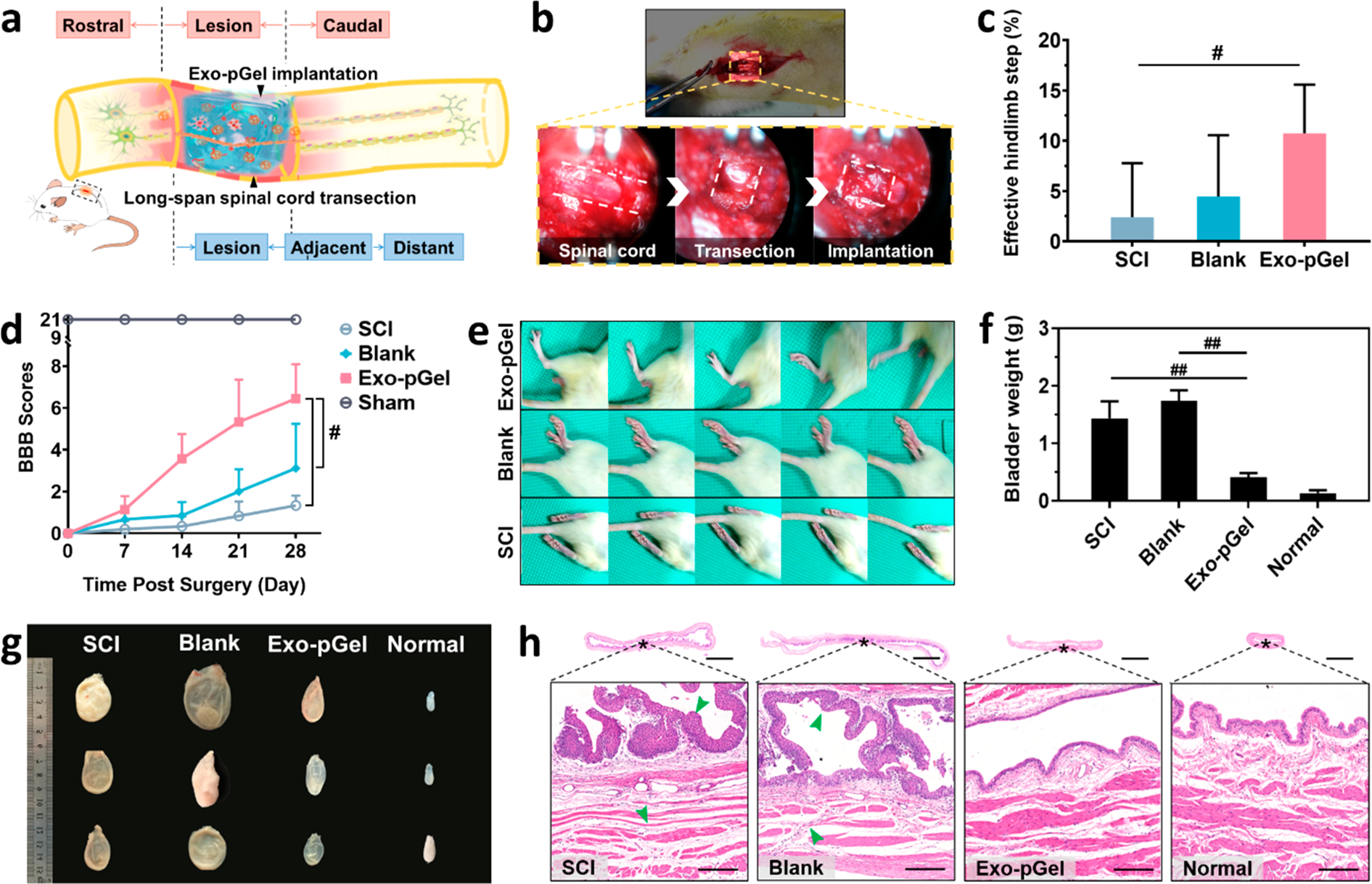
图3. 大鼠脊髓全横切损伤的外泌体-水凝胶移植治疗显著促进后肢运动功能恢复并缓解神经源性膀胱损伤

图4. 外泌体-水凝胶(Exo-pGel)移植与空白水凝胶(Blank)移植后28天脊髓神经组织的修复效果
高建青教授团队所构建的生物相容性水凝胶黏附性携载MSC细胞外泌体的三维移植体系,有效实现了对外泌体的脊髓局部递送,从而达到治疗SCI、重建运动功能的疗效,该研究为基于外泌体的中枢神经系统相关疾病的治疗及病理性微环境的调节提供了重要的理论和实验依据。
以上成果发表在Nano Letters杂志上 ,论文的第一作者为浙江大学药学院博士后李黎明,通讯作者为高建青教授。
论文链接:https://dx.doi.org/10.1021/acs.nanolett.0c00929
- 新医大一附院盛伟斌教授/华科大马良教授 AFM:构建了仿生多功能水凝胶贴片-在脊髓损伤治疗方面取得新进展 2026-03-02
- 中山三院何留民教授/北化薛佳佳教授 Adv. Mater.:脊髓损伤微环境重塑与神经再生新进展 2025-09-15
- 华科大罗志强教授团队 Adv. Mater.: 电容耦合响应水凝胶提供无线化电刺激促进脊髓损伤组织再生 2024-01-14
- 长春应化所王大鹏/唐纪琳、长春中医药大学刘芳馨、南京工业大学王瑞Adv. Mater.:水凝胶敷料集成可溶性微针,利用扩散机制达成“时空级联反应”策略实现糖尿病伤口高效促愈 2026-06-09
- 中山大学吴进等 AFM:基于坚韧可降解皮革水凝胶的自供电、超灵敏柔性H2S气体传感器 2026-06-05
- 中国石油大学(华东)张丽媛/青岛科技大学程浩然 Nat. Commun.:在耐盐水凝胶领域获重要进展 2026-06-04
- 东华大学沈明武研究员/史向阳教授团队 AFM:仿生外泌体伪装的pH响应型树状大分子纳米凝胶作为疫苗通过重编程多种细胞类型治疗胰腺癌 2026-02-20
