最近,四川大学生物医学工程学院/国家生物医学材料工程技术研究中心张兴栋院士团队的王启光副研究员和樊渝江教授开发了一种治疗骨关节炎的新策略:利用来自脐带的间充质干细胞衍生的外泌体(UCMSC-EXOs)进行无细胞治疗。研究人员首先开发了软骨细胞靶向聚合物修饰的外泌体,并将其封装在巯基化透明质酸微凝胶中,形成“两步”释放系统,协同提升OA软骨修复,并通过大鼠OA模型得到了验证。该研究发现了UCMSC-EXO对OA软骨细胞再年轻化的作用,并揭示了UCMSC-EXO中的p53信号通路是恢复老化软骨细胞功能的关键因素。通过结合软骨细胞靶向和缓释策略,外泌体在体内的保留时间和作用效率得到了有效提升。这项工作发表在“ACS Nano”上,题为“Cell-Free Osteoarthritis Treatment with Sustained-Release of Chondrocyte-Targeting Exosomes from Umbilical Cord-Derived Mesenchymal Stem Cells to Rejuvenate Ageing Chondrocytes”。论文第一作者为四川大学生物医学工程学院博士生曹洪芙。该研究得到了国家自然科学基金委面上项目的支持。
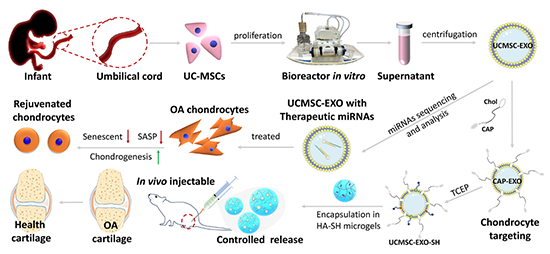
图1 可持续释放的软骨细胞靶向UCMSC-EXO的治疗示意图
研究人员发现,UCMSC-EXOs中高表达的功能性miRNA与OA的形成相关,并通过分析靶基因确认p53信号通路是OA软骨细胞在年轻化的关键因素,同时利用体外细胞实验验证了UCMSC-EXOs对OA软骨细胞的再年轻化和细胞外基质再生的作用(图2)。
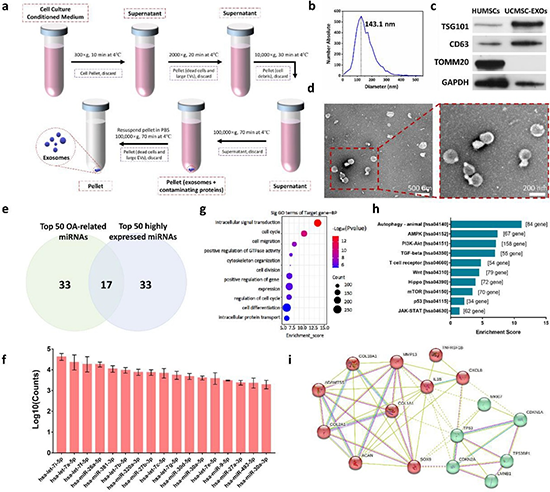
图2. UCMSC-EXOs的提取及其功能性miRNA分析
为进一步提高外泌体在体内的治疗效率,研究人员使用CLS-PEG-CAP高分子对外泌体表面进行了软骨细胞靶向肽(CAP)修饰,显著提高了UCMSC-EXOs在软骨病变部位的富集,并减少了在其它器官中的扩散。
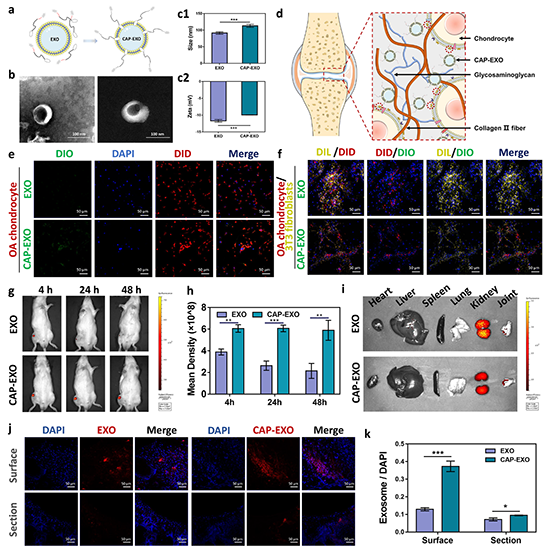
图3. CAP修饰的外泌体可特异性靶向关节内的软骨细胞。
此外,研究人员利用二硫键/共混双重机制将外泌体封装在巯基化透明质酸(HA-SH)微凝胶中,构建了“两步”释放系统,即部分未与HA-SH材料结合的外泌体首先快速释放,在关节软骨表面富集“先头兵”;而通过二硫键与HA-SH结合的外泌体随着降解逐步释放(图4)。实验结果表明,该体系可实现外泌体在关节腔内14天以上的持续释放。
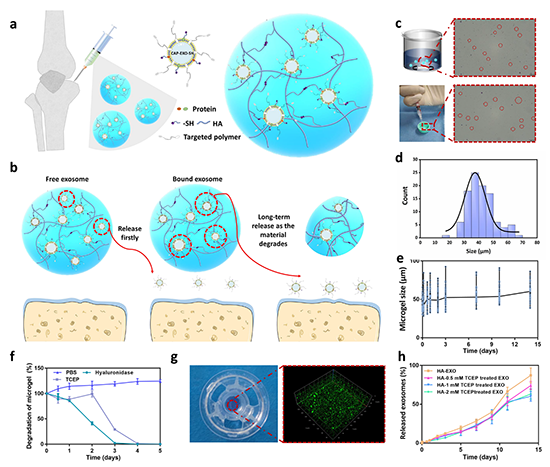
图4. 可注射HA-SH微凝胶中外泌体的“两相”缓释
体内实验结果表明,具有软骨细胞特异性靶向和体内缓释功能的工程化UCMSC-EXOs在OA治疗中显示出良好协同效应,其治疗效果显著性优于天然外泌体和仅具有特异性靶向或体内缓释作用的外泌体对照组(图5)。
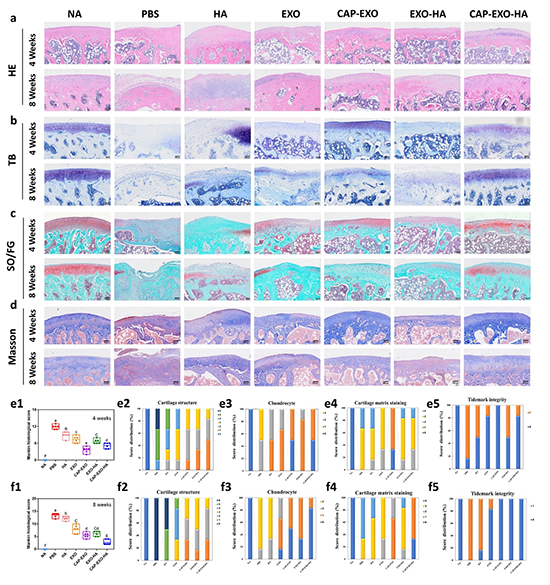
图5. 具有软骨细胞特异性靶向和体内缓释功能的外泌体显示出良好的OA治疗效果
这项工作是该团队近期对工程化外泌体平台构建的最新进展之一。利用软骨特异性靶向和HA-SH微凝胶负载缓释的工程化UCMSC-EXOs可以显著提高其在关节部位恢复衰老软骨细胞功能的效率和有效时间,在OA治疗中具有良好的临床应用前景。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.3c01612
- 西湖大学吕久安课题组诚招博士生、博后、科研助理 - 材料、高分子、化学、电子、光学、光电、机械 2026-06-02
- 重庆理工大学杨朝龙/王凯悌团队 AFM:长寿命、高亮度的高分子室温磷光材料 2026-05-31
- 天工大张佳玮教授课题组 AFM:宽温域高阻尼形状记忆高分子水凝胶 2026-05-28
- 东华大学沈明武研究员/史向阳教授团队 AFM:仿生外泌体伪装的pH响应型树状大分子纳米凝胶作为疫苗通过重编程多种细胞类型治疗胰腺癌 2026-02-20
- 北京化工大学蔡晴/喻盈捷 AFM:三重生物粘附性微球赋能金属离子工程化外泌体疗法,实现血管化骨再生 2026-02-18
- 东南大学张天柱教授团队《ACS Nano》:封装脂肪干细胞外泌体补片用于调节炎症和促进组织再生 2025-06-09
- 东华大学沈明武研究员/史向阳教授团队:不对称含磷树状大分子递送菠萝蛋白酶用于骨关节炎的抗炎和软骨保护治疗 2025-06-13
