软组织具有高断裂韧性,然而其力学机制尚不清晰。近日,西安交通大学唐敬达教授与哈佛大学锁志刚教授合作,围绕“胶原软组织的增韧机制”开展研究,通过力学实验与显微观测,得到了软组织的牵引-分离定律,揭示了胶原软组织高断裂韧性的微观机制,对仿生软材料的设计具有指导意义。相关成果以Why are soft collagenous tissues so tough?为题,发表在国际期刊《Science Advances》上,并得到期刊主页推荐。

右下为Sci. Adv. 期刊推荐的本文图片
胶原软组织,如皮肤、肌腱和心脏瓣膜,通常具有较高的断裂韧性。例如,牛心包这种胶原软组织用于人类心脏瓣膜置换手术,能承受数亿次开闭循环而不开裂(图1A,B)。本研究选取牛心包作为研究对象,探讨了胶原软组织的增韧机制。胶原软组织的微观结构如图1C-F所示。
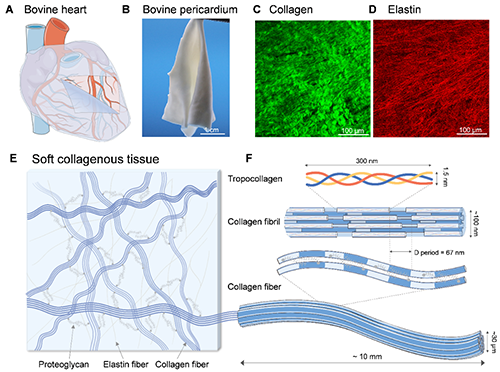
图1.胶原软组织微观结构
当裂纹在胶原软组织中扩展时,胶原纤维在裂尖解卷曲,沿拉伸方向重新定向,从裂纹表面抽出形成桥接区阻碍裂纹扩展(图2),该桥接过程可通过断裂力学中的牵引-分离曲线(traction-separation curve)描述。
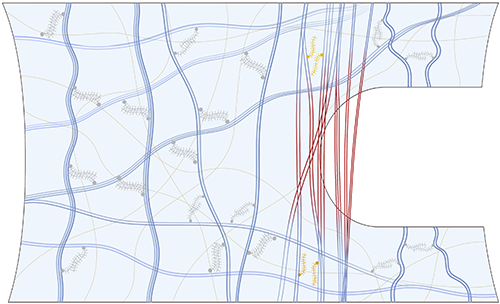
图2.胶原纤维桥接裂纹
研究人员设计了“纤维抽出试验”与“裂纹扩展试验”两种方法,测得了胶原组织的牵引-分离关系曲线。纤维抽出实验中,在样品两侧分别裁切预置裂纹,仅留下宽度约为300 μm的胶原纤维束(图3A,B),然后直接从基质中抽出胶原纤维,记录其抽出过程中的力-位移曲线,进而获得牵引分离曲线。结果显示,牛心包组织的峰值牵引应力约为60 MPa,最大裂纹分离长度约为6 mm(图3C,D)。
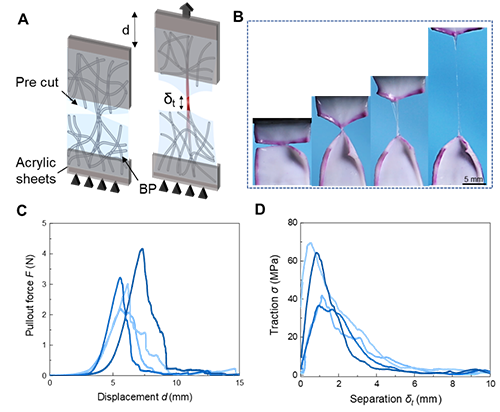
图3.胶原纤维抽出实验
为了探明纤维抽出过程中的微观机制,研究人员使用偏振光显微镜(图4A)和双光子显微镜(图4B)记录了胶原纤维在拉伸过程中不同阶段的形貌变化。未变形时,卷曲的胶原纤维嵌入在弹性蛋白网络中。抽出过程中,胶原纤维开始解卷曲,并沿拉伸方向重新定向,胶原纤维逐步被抽出,最终约10mm长的胶原纤维被完全抽出。
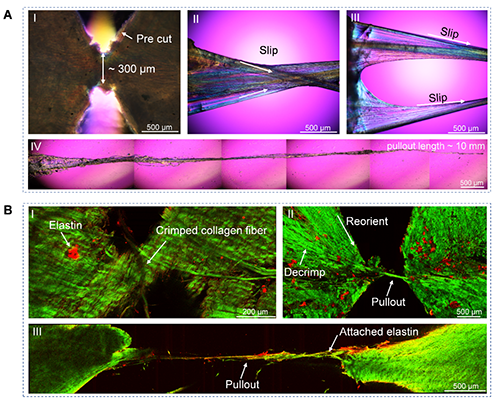
图4.胶原纤维抽出过程中的微观形貌变化
随后,研究人员基于裂纹扩展过程中能量释放率与牵引分离曲线的关系,设计“裂纹扩展实验”测量了胶原软组织的牵引分离曲线。首先观察了裂纹扩展过程中,胶原纤维在裂尖的行为和微观形貌变化。结果显示,在未变形的样品中,裂纹尖端保持完整,纤维呈卷曲状(图5A)。随着拉伸比的增加,裂纹钝化,卷曲的胶原纤维束拉直并沿拉伸方向重新取向(图5B)。随着进一步拉伸,裂纹开始在软基体中扩展,胶原纤维被拉出并桥接裂纹,在裂纹尖端形成一个明显的桥接区(图5C)。

图5.裂尖胶原纤维在扩展过程中的形貌变化
随后,研究人员准备了预切裂纹的矩形样品,对样品进行拉伸(图6A,B),使用黑色标记点对裂纹尖端的表面进行标记(图6C)。研究人员根据裂纹尖端标记点的状态和裂纹扩展进程,识别出胶原软组织具有两个特征能量释放率值:GA和GB。实验结果显示,牛心包的两个特征能量释放率GA = 16.2 kJ/m2,GB = 112.1 kJ/m2。峰值牵引力σ0约为60.9 MPa。最大分离长度δ0约为4.8 mm(图6D,E)。研究人员还研究了软组织的牵引分离曲线随样品高度、纤维取向和含水量的变化。
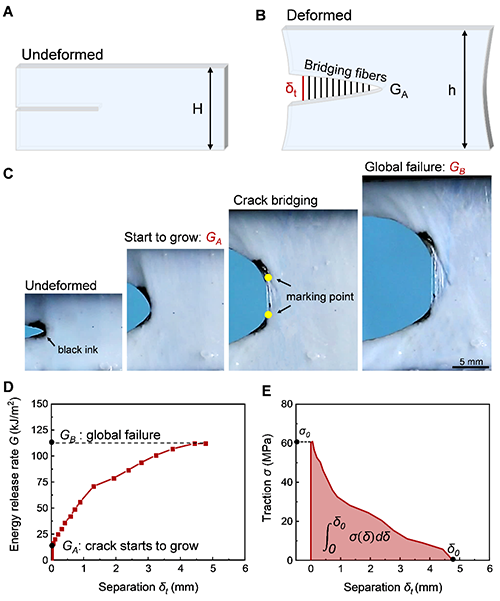
图6.裂纹扩展实验
研究人员将胶原软组织的牵引分离曲线与一些经典材料进行比较。软组织的峰值牵引力约为60 MPa,接近骨骼、珍珠层和鱼鳞片等,远高于单向纤维/环氧树脂复合材料。软组织的最大分离长度约为6 mm,高于合成材料。由于胶原软组织与硬组织的牵引力相当,而裂纹分离长度远高于硬组织的,因此,胶原软组织的断裂韧性比硬生物组织高1~2个数量级(图7A)。长胶原纤维从软组织裂纹表面抽出形成较大尺寸的桥接区,提供高桥接应力,有效阻碍裂纹扩展,导致了软组织的高断裂韧性和裂纹不敏感性(图7B)。最后比较了几种经典材料的裂纹桥接机制(图7C)。
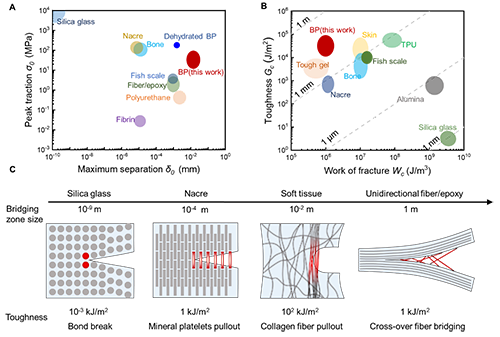
图7.胶原软组织的增韧机制
该项工作揭示了胶原软组织高断裂韧性的力学机制,量化了裂纹桥接的牵引-分离关系,为开发仿生材料(如人造心脏瓣膜)提供了理论依据。
上述研究得到了国家优秀青年基金的资助,特别致谢上海纽脉医疗科技股份有限公司提供的牛心包样品。
论文第一作者为西安交大硕士生唐婧嫄、通讯作者为西安交大唐敬达教授和哈佛大学锁志刚教授,论文作者还包括西安交大博士生陈曦、刘丰恺,毕业硕士曾梁松(现为美国西北大学博士生)。
论文链接 https://www.science.org/doi/10.1126/sciadv.adw0808
