发展智能药物递送与控释技术是实现精准医疗的关键技术支撑,对提升重大疾病防治能力、推动生物医药产业高质量发展具有重要战略意义。近年来,生物技术、材料科学、人工智能和电子信息等领域的技术进步正在重塑药物在体内的输送方式。智能小型化药物递释器械融合上述前沿技术,可实现精准的药代动力学控制、靶向分布与可编程释放,在提升疗效、减轻毒副作用的同时提升患者依从性,代表了下一代药物递释器械的发展方向:更智能、更安全、更轻巧。

2026年3月26日,浙江大学药学院、先进药物递释系统全国重点实验室顾臻教授、Hongming Chen院士、魏鑫伟研究员,与麻省理工学院Robert Langer院士、Giovanni Traverso教授,牛津大学Molly Stevens院士,布朗大学Tejal Desai院士,美国北卡罗来纳大学教堂山分校John Buse教授等,在Nature正刊发表题为“Towards intelligent and miniaturized drug delivery devices”的述评文章,系统阐述了新一代基于药械组合的药物递释系统的研发进展与未来发展前景。文章介绍了IMDDDs的关键类别和设计原则,并重点分析了人工智能在辅助器械设计、制造及性能增强方面的作用,并针对肿瘤、糖尿病、心血管疾病等临床场景,以及未来面临的挑战与机遇进行了深入讨论。文章特别强调人工智能与生物智能、材质智能的融合为IMDDDs的快速发展提供了可能。顾臻为该文的通讯作者,魏鑫伟为第一作者。
区别于传统“自下而上”通过自组装等工艺制备的微纳制剂(如脂质体、脂质纳米颗粒、微球等),IMDDDs通常采用“自上而下”的制造工艺,尺寸通常在微米至厘米级。通过集成生物电子、智能响应等控制模块,结合可穿戴、植入式等多种递送模式,IMDDDs不仅能智能递送小分子和生物大分子药物,还可高效递送病毒、细胞乃至机体组织,广泛应用于疾病治疗与疫苗接种等领域。典型器械形式包括柔性电子贴片、微针、渗透泵、无线植入器械、智能隐形眼镜及可吞咽装置等,这类器械时常融入智能材料与先进算法,可实现对药物的长效、靶向、响应性、闭环及程序化释放的精准控制(图 1)。
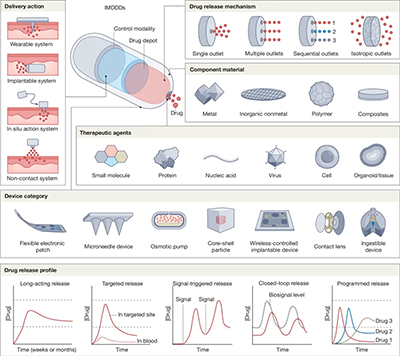
图1. 智能小型化药物递释器械IMDDDs组件和类别示意图
IMDDDs器械类型
根据所集成模块的类型和性质,IMDDDs可分为四类(图 2)。
(1)生物电子治疗器械
这类器械通常将微电子与生物传感技术相结合,集成于可穿戴或可植入等系统中,通过电信号实现药物的精准控释,具有响应快、可编程等优势,并支持实时生理监测与闭环给药。其中典型的闭环系统包括三个核心部分:用于监测生理信号的传感器、控释药物的储库、以及负责数据处理与通信的数字模块。与传统的开环递送方式不同,闭环系统可通过血液、汗液、组织液等生物体液实时监测生理信号,并依据反馈动态调节给药。除直接电触发外,电能也可转化为光、磁、热或力等非电形式以触发药物释放。
(2)物理触发式器械
该类器械能响应外部非电物理刺激,如机械力、声、热、光与磁信号。机械触发器械通过压缩/拉伸力、剪切力或超声波等机械作用激活释放药物,也可利用预存储的机械能(如弹簧、气体压力)实现定向递送。近期开发的一种渗透压驱动的长效输注贴,可实现24小时持续稳定释药。声学触发主要借助超声的空化、热及机械效应;热触发则依赖温敏材料,通过电热、磁热或光热等方式实现有线或无线控释。光触发器械采用光敏材料或分子,通过特定波长光照实现空间精准的药物释放。磁触发器械则利用外磁场引起磁性载药结构变化,可实现无创深部组织递送。
(3)生理化学信号响应性器械
这类系统直接利用体内生理化学信号实现精准治疗,主要设计策略集中于三类触发因素:离子变化、小分子变化与生物分子相互作用。体液中丰富的离子(如钙离子)可作为局部给药的触发信号;pH变化是另一关键机制,特定材料(如碳酸盐、缩醛/酮、亚胺等)会在相应pH下发生结构或亲水性改变,从而实现pH响应释放。硼酸与葡萄糖的可逆结合已广泛应用于糖尿病管理器械中,例如基于此原理的微针类胰岛素递释器械已在动物模型中展示出良好的血糖调控能力。此外,利用ATP-适配体高亲和相互作用、缺氧敏感基团以及活性氧响应元件的系统,也为按需释药提供了多样化的化学途径。
(4)活性器械
活性器械指细胞、细菌或复杂组织培养物等活性治疗组分集成于IMDDDs的新兴体系。其开发关键在于维持生物组分的活力与功能,需精确调控物质交换(如氧气、氨基酸)与环境条件(如pH、温度)。多孔膜覆盖的腔室结构可通过孔隙实现内外双向交换;将药物封装于多糖、海藻酸盐或明胶等聚合物微凝胶/水凝胶中,有助于保持治疗活性;预血管化技术可进一步改善氧与营养输送。此外,微孔、微槽与微柱等微观结构可为治疗细胞提供附着与生长的空间支持。
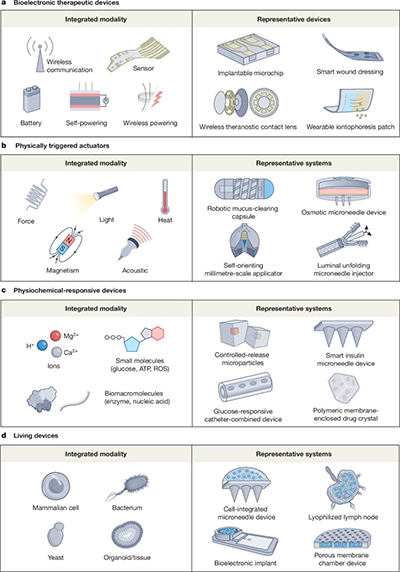
图2. 典型的IMDDDs类型示意图
AI赋能IMDDDs
(1)AI辅助IMDDDs设计与制造
人工智能技术正在推动药物递送领域发生深刻变革,其强大的计算与学习能力为器械设计、制造与功能优化提供了全新可能,助力实现更精准、个性化的治疗(图3)。人工智能辅助IMDDDs创新主要体现在以下方面:药物研发、器械设计与制造、数据处理与控制优化。
深度学习等人工智能算法已被广泛应用于靶点识别与虚拟筛选,可优化药物分子结构并预测其吸收、分布、代谢、排泄及毒性特性,同时还能评估联合疗法的效果与毒性风险,提升药物安全性。此外,基于体外毒理学数据与计算模型的人工智能方法,正在为个性化给药方案的制定提供新途径,减少对传统实验的依赖。在器械设计与制造方面,人工智能能够分析药物物化性质与释放行为,快速筛选最佳配方并优化器械的载药量、释放精度及稳定性。制造过程中,人工智能可与3D打印等技术结合,实时监测与调整参数,推动个性化医疗器械制造。计算机视觉系统与机器学习能实时检测生产缺陷,反馈至生产线以提升质量控制水平。数字孪生技术通过虚实交互实现工艺参数的动态优化,为大规模稳定生产奠定基础。
在医疗大数据处理与分析层面,人工智能显著提升了效率、准确性与自动化水平。卷积神经网络、循环神经网络等模型能有效解析脑电图、心电图等生理信号,实现疾病分类与早期预警。在连续健康监测中,AI模型支持构建无创、持续的血压估算系统。糖尿病管理中,AI可通过分析持续血糖数据优化预测并制定个性化胰岛素方案。医学影像分析中,AI在CT、MRI等多种模态中表现优异。此外,基于深度学习的语音识别技术还能通过声学特征辅助疾病筛查,拓展健康管理应用场景。
(2)典型的AI驱动IMDDDs
AI驱动的闭环类器械整合传感、分析与自主给药功能,可根据患者生理状态动态调整治疗方案。例如,在糖尿病管理中,系统通过持续血糖监测与机器学习预测趋势,实现血糖达标时间超过80%;在癫痫治疗中,AI能快速识别发作并触发自适应给药;针对慢性伤口,智能敷料可评估感染风险并按需释放抗生素或生长因子;闭环输注系统还能通过实时监测血药浓度,将化疗药物维持在治疗窗口内,实现增效减毒。
人工智能也推动了个性化医疗设备与药物递送系统的发展。计算机视觉技术可通过图像信息识别评估患者状况,例如结合智能手机皮肤镜拍摄病变图像,并利用喷墨打印制作形状、剂量个体化的精准治疗贴片;无人机可借助机器视觉识别定位患者并投递、注入药物,特别用于急救场景。智能胶囊则为未来图像引导的口服疗法提供基础。语音识别提供无需动手的交互方式,可集成于给药平台辅助用药管理。例如,一种仿生人工纤毛阵列能够识别特定声波频率并触发药物释放。
AI驱动的微型机器人在药物递送中同样前景广阔。AI算法可提升其导航能力,例如通过Q学习引导机器人在动态环境中精确抵达目标。基于深度学习的集群控制技术能实现协同规划与自主适应。磁导航系统结合图像处理可无线引导微型机器人定向移动;进化算法可用于设计活体机器人结构,为体内安全递送提供创新方案。人工智能正推动微型机器人向更智能、更可靠的方向发展。
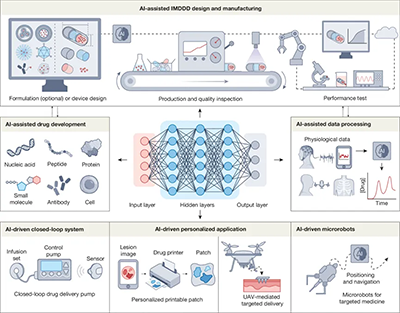
图3. AI赋能IMDDDs的设计、制造与应用
IMDDDs的临床应用
为提升肿瘤治疗效果,多种精准递送技术正不断发展。例如,局部喷雾凝胶、3D打印支架与生物载体能增强CAR-T细胞的存活与功能;微针贴片结合纳米颗粒可提升药物穿透深度;植入式生物电子设备通过无线控制实现主动靶向与远程释药;光动力复合系统则支持微创介入与深层治疗,为突破传统疗法局限提供新途径。在糖尿病管理领域,可穿戴透皮贴片已实现血糖实时监测与药物反馈调控;口服胰岛素胶囊通过仿生定向、微针肠壁给药及喷射释药等设计,显著提高生物利用度。皮下植入方面,无线供电平台、工程细胞植入物及封装胰岛β细胞的装置,为严重胰岛素缺乏患者提供了创新治疗策略。
针对疫苗接种,微针贴片可作为无痛、易用的替代方案,适用于包括mRNA在内的多种抗原递送,且可在室温下长期保存,尤其利于资源有限地区的广泛接种。吸入式疫苗则以其非侵入性特点,有助于提升接种依从性。此外,用于心血管领域的柔性智能贴片可同步监测心电并释药,以降低心梗风险;微针增强型支架能实现血管深层靶向给药,减少再狭窄。伤口管理方面,集成传感器的敷料可依据环境指标控制抗生素释放,并结合电刺激或光疗法促进愈合。基于微针的皮下植入还可实现长效避孕药物持续释放,为低收入地区提供安全、可及的解决方案。
总结与展望
IMDDDs正推动药物递释器械向个性化、智能化、小型化方向发展,但其临床转化往往也面临一些挑战,包括性能一致性、生物相容性和规模化制造等。在治疗层面需实现精准控制:慢性病要求长效稳定释放,急性治疗则需快速响应。结合生物响应制剂与智能算法,可构建基于实时生理信号的闭环个性化给药系统。可靠性涉及材料、结构及生物界面等多方面,设备需在体内复杂环境中保持稳定。柔性电子与软材料技术可改善机械匹配,增强组织贴合。微机电系统与高精度3D打印等先进工艺,结合AI质量检测,有助于提升产品一致性与临床成功率。设备小型化是精准微创治疗的必然趋势,但也受限于载药量与能源供应。高载药密度材料可提高药物负载,无线供能与能量收集技术则为器械微型化提供新路径。除了尺寸缩小,未来设备将进一步整合生理监测、自适应释药与安全保障等多重功能。安全性涵盖生物相容性、材料毒性及系统运行等方面。植入设备易引发免疫反应与生物膜形成,表面改性是有效应对策略。材料须确保组织安全,系统应具备失效保护机制,通信需兼顾低延迟、高灵敏与数据安全。为实现广泛普及,可通过使用耐用生物材料、智能制造技术、自动化生产流程及柔性生产模式等,降低规模化与个性化制造成本,实现经济高效的制造方案。展望未来,IMDDDs将朝着更集成、更智能、以患者为中心的方向演进。个性化治疗是核心,系统将依据患者生理特征、基因信息与生活方式动态调节。人工智能通过持续学习患者响应模式,将进一步优化给药策略,实现更精准、自适应的治疗闭环。
原文链接 https://www.nature.com/articles/s41586-026-10221-3
- 西南交大杨维清教授/邓维礼副教授 Adv. Mater. 综述:离子水凝胶传感器 - 迈向下一代个性化健康监测 2025-10-31
- 山东大学崔基炜教授团队《Adv. Mater.》:“以瘤治瘤”的水凝胶疫苗 - 实现个性化肿瘤免疫治疗新突破 2025-10-09
- 清华大学/北京清华长庚医院李舟、邹洋 AFM:受应力激励的仿生表皮传感吸盘用于个性化心血管监测 2025-09-30
- 宁波材料所陈涛/肖鹏团队《Adv. Mater.》: 柔性凝胶电子器件实现吸湿-解吸实时监测与智能化湿度管理 2026-02-05
- 北科大许利苹教授/理化所万茜子副研究员 AFM:按需可剥离比色(ODC)贴片实现慢性伤口的智能化无创监测 2025-07-20
- 中科大庄涛涛团队 JACS:高品质因子和高稳定性的圆偏振发光体系及其在信息加密防伪和智能化织物方向的应用 2023-02-07
- 北京大学韩梦迪 Sci. Adv.:小型化的无线植入式传感系统 2024-03-22
