在组织工程与再生医学领域,长期保存具备复杂结构与功能的细胞-生物材料构建体,并满足临床“按需使用”的核心需求,一直是亟待突破的关键难题。常规细胞冷冻保存技术易受冰晶损伤、冷冻保护剂毒性影响,导致细胞活性与功能大幅下降,且复苏后细胞需重新培养才能恢复黏附形态,无法直接用于活性组织构建,严重限制了工程化组织的临床应用效率。
2026年2月,中国科学院动物研究所顾奇研究员团队创新性开发出集成冷冻保存功能的双相生物墨水系统 - CAMP(冷冻保存用于黏附与维持打印),成功打通细胞冷冻保存与生物制造的无缝衔接通道,为“现货型”工程化组织制备提供全新策略。
相关工作以Cryopreservative Bioink Enables Direct Bioprinting of Adherent Cells为题发表在国际顶级材料学期刊《Advanced Materials》上。
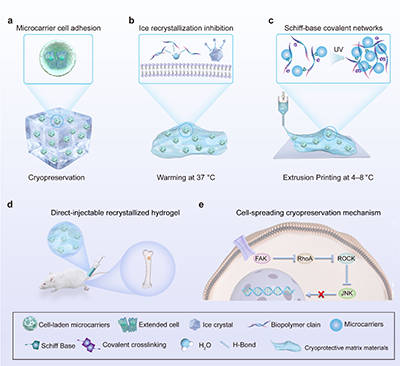
图1 CAMP(冷冻保存用于黏附与维持打印)系统工作流程。细胞在凹面透明质酸微载体上培养并伸展,随后被封装于具有冷冻保护功能的氧化甲基丙烯酸化海藻酸钠/明胶基质中,于液氮中储存。需要时解冻,可直接进行挤出打印或注射治疗。
CAMP 系统作为双相生物墨水平台,由两大核心结构协同构成:细胞微载体相采用团队自主研发的凹陷透明质酸微载体,可支撑间充质干细胞等细胞高效黏附、铺展与增殖,让细胞预先形成贴近生理状态的伸展形态;冷冻保护基质相则以氧化甲基丙烯酸化海藻酸钠/明胶复合水凝胶为核心,依托分子间氢键束缚水分子,在冷冻-复苏全程有效抑制冰晶重结晶,为细胞提供全方位物理保护。该系统突破多项传统技术瓶颈,展现出卓越的综合性能:全程无需使用二甲基亚砜(DMSO)等有毒化学冷冻保护剂,液氮冻存后细胞存活率仍可达约80%;区别于常规细胞墨水冻存后细胞变圆的缺陷,CAMP 中的细胞复苏后可完整保留黏着斑与伸展细胞骨架结构,维持生理黏附形态;同时具备优异的剪切稀化与自愈合流变特性,4–8 ℃条件下可直接完成挤出式3D生物打印,并通过光交联快速固化成型。研究还揭示,CAMP 中保持伸展状态的细胞,黏着斑激酶磷酸化水平升高,可激活促存活信号通路、抑制凋亡相关 JNK 通路,从分子层面增强细胞抗冻存应激能力。
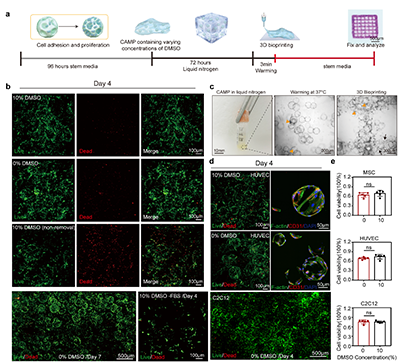
图2 CAMP适用于多种细胞冷冻保存
此外,CAMP 的冰晶重结晶抑制活性显著优于常规冷冻保护液,在大鼠股骨缺损修复实验中,冻存后的 CAMP 构建体植入体内3个月,MicroCT 结果清晰显示骨缺损得到有效修复,验证了其优异的体内再生效果。
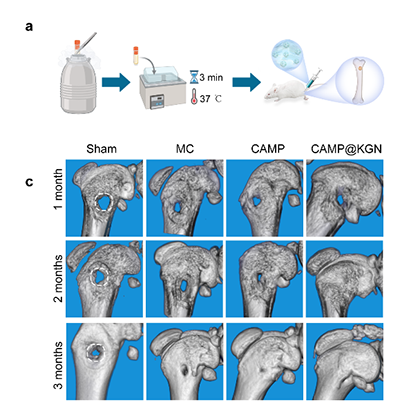
图3 CAMP应用于骨缺损治疗。冻存的CAMP构建体植入大鼠股骨远端缺损处3个月后,Micro CT显示骨缺损得到有效修复。
这项研究实现了“细胞扩增与黏附—长期深低温保存—按需生物打印/移植”全流程整合,彻底解决了活性移植物保存与使用的时效性痛点,为临床紧急需求提供可长期储存、随时取用的 “现货型” 组织工程产品方案。同时,该平台技术还可为类器官、器官芯片等复杂生物模型的标准化保存与运输提供重要参考,在生物制造与低温生物学交叉领域取得突破性进展,推动工程化组织向便捷化、实用化临床应用迈出关键一步。
标题:Cryopreservative Bioink Enables Direct Bioprinting of Adherent Cells
期刊:Advanced Materials
通讯作者:顾奇研究员
第一作者:赵喜源;丁声龙;孙大地博士
DOI:https://doi.org/10.1002/adma.72714
