在人机交互和柔性健康监测需求快速增长的背景下,如何把人体日常活动中的微弱机械刺激高效转化为可用电信号,是构建新一代软体电子系统的关键问题。离子压电凝胶(piezoionic gels)兼具与生物组织相近的柔软性和离子型信号传导机制,在可穿戴生物界面、柔性传感和能量收集等方向展现出重要潜力。从机理上看,这类材料的输出本质上来源于受力过程中阴阳离子迁移与极化行为的差异,因此,如何通过材料设计精确调控离子动力学,是提升离子压电性能的核心。
但是,现有离子压电材料的性能通常受限于阴阳离子迁移差异有限,受压后能够建立的局部电势差较小,因而电压输出和功率密度普遍偏低,难以同时满足超低压感知和直接驱动器件的需求。此前,东华大学武培怡教授和雷周玥研究员已通过微相分离结构设计,在《Advanced Materials》上报道了高灵敏离子压电弹性体(Adv. Mater. 2024, 36, 2313127),证明了通过结构设计调控离子迁移过程,可以显著提升离子压电响应。这项工作也为进一步从多尺度上协同放大离子压电效应奠定了基础。
在此基础上,该团队近期再次在 Advanced Materials 上发表成果,提出了一种多尺度结构的协同增强设计。通过分子间相互作用、微观几何结构和宏观不对称电极的协同调控,将离子压电效应的电压灵敏度提升至>104 mV kPa-1 (0.03-0.07 kPa),功率密度达到135.1 μW cm-2。相关论文以“Colossal Piezoionic Effect from Hierarchical Asymmetries in Soft Ionotronics”为题发表。
这项研究分别在分子、微观和宏观三个尺度上对离子压电响应过程中的离子运动和分布进行协同调控。分子尺度上,使用聚丙烯酸苄酯(PBzA)作为聚合物网络,利用其苯环通过阳离子-π相互作用选择性束缚EMIM+阳离子,从而强化TFSI-阴离子的迁移能力;微观尺度上,设计了微锥阵列结构以集中应力,增强局部推动离子运动的驱动力;宏观尺度上,利用不同金属电极的功函数差异构建内电场,诱导空间电荷极化,并利用TPU薄膜作为压力门控。
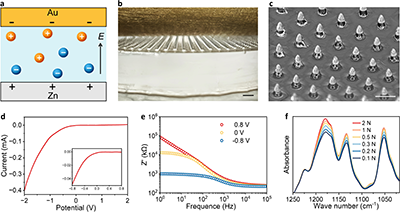
图1. 多尺度不对称离子压电凝胶的设计
在0.06 kPa的超低压下,开路电压达到了703 mV,凝胶的电压灵敏度超过104 mV kPa-1,比传统离子压电材料高出四个数量级,甚至领先于最先进的柔性压电材料。
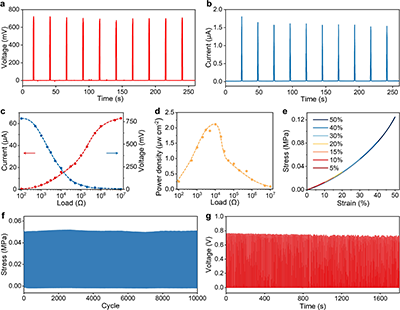
图2. 通过多尺度结构设计协同实现巨大的离子压电响应
为验证该策略的普适性,团队进一步将多尺度不对称设计拓展至基于聚乙烯醇(PVA)和P(SBMA-co-HEMA)双网络的两性离子水凝胶体系中。该水凝胶具备高离子电导率和生物相容性。在不对称电极和微锥结构的共同作用下,该水凝胶在约0.06 kPa超低压下产生了约990 mV的开路电压,电压灵敏度高达1.7×104 mV kPa-1。
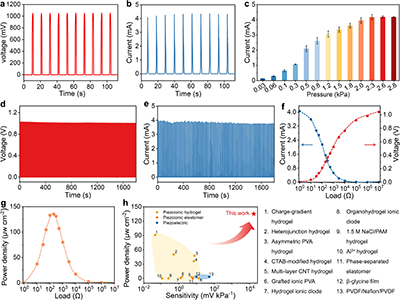
图3. 多尺度协同策略的普适性
将8个基本单元串联堆叠为4层复合结构,在仅0.5 N的微弱压力下即可产生约4.5 V的开路电压和约7.2 μA的短路电流,足以直接驱动一串10个LED同时明亮发光。将该多层器件贴附于胸口,受试者吸气时胸腔扩张产生的微弱压力即可点亮LED,呼气时熄灭,形成与呼吸节律同步的明灭循环。这种直接驱动光电器件的能力,证明了其输出电能具有高电压、内在整流等优质特性,无需外部整流桥即可与储能模块兼容。
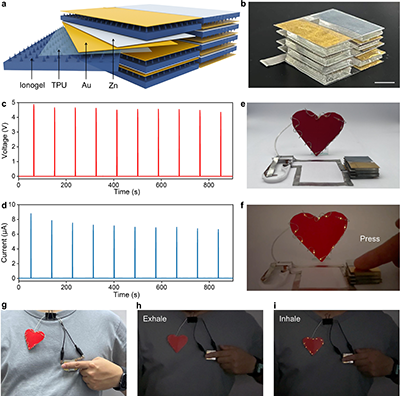
图4. 能量收集与可穿戴应用的演示
这项研究不仅大幅提高了离子压电材料的性能,且在离子凝胶和水凝胶体系中均验证有效,展示了该材料在自供能生物界面、可穿戴传感器和软体能量收集器中的广阔前景,为下一代高性能离子电子学提供了通用材料框架,也为人机交互的自主式生物接口开辟了新路径。
文章链接:http://doi.org/10.1002/adma.73067
- 暂无相关新闻
