糖尿病足溃疡是糖尿病的一种严重并发症,其特征为创面难以愈合,长期陷入高糖渗出液过多、持续感染、氧化应激、细胞增殖受损的恶性循环。然而,传统敷料虽能被动吸收渗出液,但其亲水性特性会使其在换药时与创面发生粘连,造成二次损伤,从而限制治疗效果;现有Janus敷料缺乏对创面微环境的调控能力,难以缓解持续性炎症,也同样无法有效促进创面再上皮化进程。
针对上述难题,东华大学陈志钢教授团队开发了一种可调控糖尿病创面微环境的多功能Janus结构纤维膜(P/2PHECaPDA)。该体系集成抗重力渗液管理、光热杀菌、钙离子释放、葡萄糖响应型药物递送四大功能。纤维膜由疏水聚乳酸(PLA)层与亲水复合层(2PHECaPDA)组成,后者为CaPDA及通过硼酸酯键接枝表没食子儿茶素没食子酸酯(EGCG)的透明质酸的复合层。这一多功能平台为感染性糖尿病创面的治疗提供了极具前景的新策略。
这种具备梯度孔隙与差异化润湿性的不对称结构,可利用水分子从范德华力吸附向有序氢键网络的转变,实现自泵式渗液清除,速率达1.96 g·cm?2·h?1。其中 CaPDA 组分具有优异的光热抗菌活性(杀菌效率>99%),并可持续释放 Ca2?以促进愈合。同时,通过硼酸酯键连接的EGCG 可实现葡萄糖响应型抗氧化剂释放,有效缓解氧化应激,并使M2型巨噬细胞极化水平相较于基线提升3.5倍。体内实验证实,该材料生物相容性优异,可显著加速创面闭合。
2026年4月14日,相关工作以“Self-Pumping Janus Membranes for Calcium Delivery in Diabetic Wound Healing”为题,发表于《Advanced Functional Materials》上。论文第一作者为东华大学青年研究员文玫,通讯作者为青年研究员余诺和陈志钢教授。
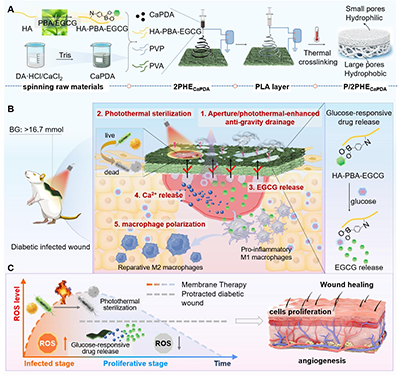
图1.P/2PHECaPDA 的制备流程及其作用下的创面微环境和创面愈合的不同阶段展示
本研究通过盐酸多巴胺与氯化钙在缓冲液中自聚合24小时合成CaPDA NPs,并将透明质酸与PBA和表没食子儿茶素没食子酸酯(EGCG)通过硼酸酯键接枝得到HA-PBA-EGCG (HE),再通过分步静电纺丝构筑出疏水聚乳酸(PLA)层与亲水功能层(2PHECaPDA)组成 Janus 结构纤维膜 P/2PHECaPDA(图1.A)。研究表明,其微观形貌连续均匀、界面结合牢固,可依靠界面能梯度与拉普拉斯压差实现高效自泵式引流,速率高达 1.96 g?cm?2?h?1。(图1-2)
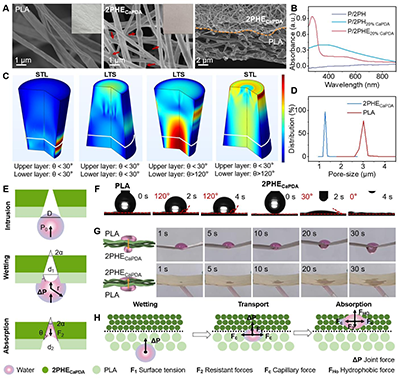
图2.P/2PHECaPDA 的表征与抗重力自泵渗液的功能验证
同时,为验证敷料的钙离子/药物协同可控释放性能,本研究通过体外释放动力学,系统评价了2PHECaPDA中Ca2?与EGCG的释放性能的优良性;另外,通过DPPH与ABTS自由基清除实验,证明该敷料具有优异的抗氧化性能,可实现近乎完全的ABTS自由基清除(~99%)(图3)
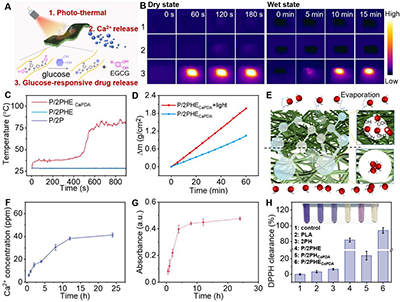
图3.P/2PHECaPDA 膜的光热、释药、抗氧化性能验证及膜内水分传输机理示意图
总体来看,P/2PHECaPDA 膜这种具备梯度孔隙与差异化润湿性的不对称结构,可利用水分子从范德华力吸附向有序氢键网络的转变,实现自泵式渗液清除。其中CaPDA 组分具有优异的光热抗菌活性(杀菌效率>99%),并可持续释放Ca2?以促进愈合。同时,通过硼酸酯键连接的 EGCG 可实现葡萄糖响应型抗氧化剂释放,有效缓解氧化应激,并使M2 型巨噬细胞极化水平相较于基线提升3.5 倍。且体内实验证实,该材料生物相容性优异,可显著加速创面闭合。
原文链接:https://doi.org/10.1002/adfm.202600053
- 山东大学王志宁教授团队《ACS AMI》:类水凝胶Janus膜用于膜蒸馏过程高效抗润湿、抗污染 2023-04-13
- 天工大张松楠副研究员/福大赖跃坤教授 CEJ:可高效集雾的兼具Cu(OH)?微针和嵌入式串珠状纳米纤维膜的四元仿生亲疏复合材料 2022-12-16
- 江苏大学王钱钱副教授《ACS Nano》综述:Janus纳米纤维素 2022-09-10
- 东华大学毛吉富、张倩 AFM:纳米互锁增强电活性敷料 - 电磁感应促进糖尿病伤口愈合和伤口微环境监测 2025-08-08
- 福州大学林子俺研究员团队 AFM:一种具有自氧化特性的邻位二羟基广谱抗菌共价有机框架水凝胶用于促进糖尿病伤口愈合 2025-05-06
- 东南大学葛丽芹教授/刘玲教授 CEJ:多功能微针贴片与电刺激协同调节伤口微环境 促进感染糖尿病伤口愈合 2025-02-17
