硫氧还蛋白还原酶(TrxR)是一种在多种癌细胞中过量表达的二聚体硒酶,与肿瘤的恶性程度、生长、侵袭及耐药性等密切相关。研究表明,通过降低肿瘤细胞内TrxR的活性,可以增强肿瘤细胞对化疗药物的敏感性,并抑制肿瘤细胞的迁移/侵袭能力,大大降低患者治疗后残余癌细胞转移与复发的风险,因此TrxR已经成为新一代肿瘤治疗的“明星”靶点。该还原酶的 C-末端的硒代半胱氨酸残基(Sec)具有高度活性,对TrxR的生理活性起到至关重要的作用。Sec暴露于TrxR的外表面,在还原性生理条件下处于SeH/SH状态,容易被电负性化合物修饰,是TrxR抑制剂药物的主要作用靶点。
基于课题组之前发现的含硒动态化学反应,清华大学许华平教授课题组设计了一种具有荧光成像能力,且可作为TrxR还原底物的靶向含硒两亲高分子纳米药物载体(RGD-PEG-PUSeSe-PEG-RGD)。在TrxR的刺激下,该含硒纳米载体可以实现化疗药物吉西他滨(GEM)的可控释放。载体中的双硒键可与TrxR C-末端的活性位点Sec残基通过含硒动态化学交换形成新的Se-Se/Se-S键,抑制TrxR活性,从而达到化疗增敏及抑制肿瘤转移复发的效果。该工作利用含硒纳米药物递送体系将实体肿瘤治疗与治疗后干预进行了有效的结合 (图1)。

图1. 以含硒两亲高分子材料为基础的实验设计示意图。
在体外实验中,该含硒纳米药物载体在不影响TrxR表达量的情况下,有效抑制TrxR活性,诱导A549细胞产生大量ROS,从而增强肿瘤细胞对化疗药物GEM的敏感性,导致细胞发生凋亡。此外,他们选取小分子HOC3SeSPh与单体(HOC3Se)2用以模拟TrxR以及含硒高分子药物载体。在NADPH的还原作用下,该反应过程监测到新的Se-Se/Se-S键的生成,从侧面印证TrxR与含硒高分子胶束之间可通过含硒动态交换,实现TrxR活性抑制的机理 (图2)。
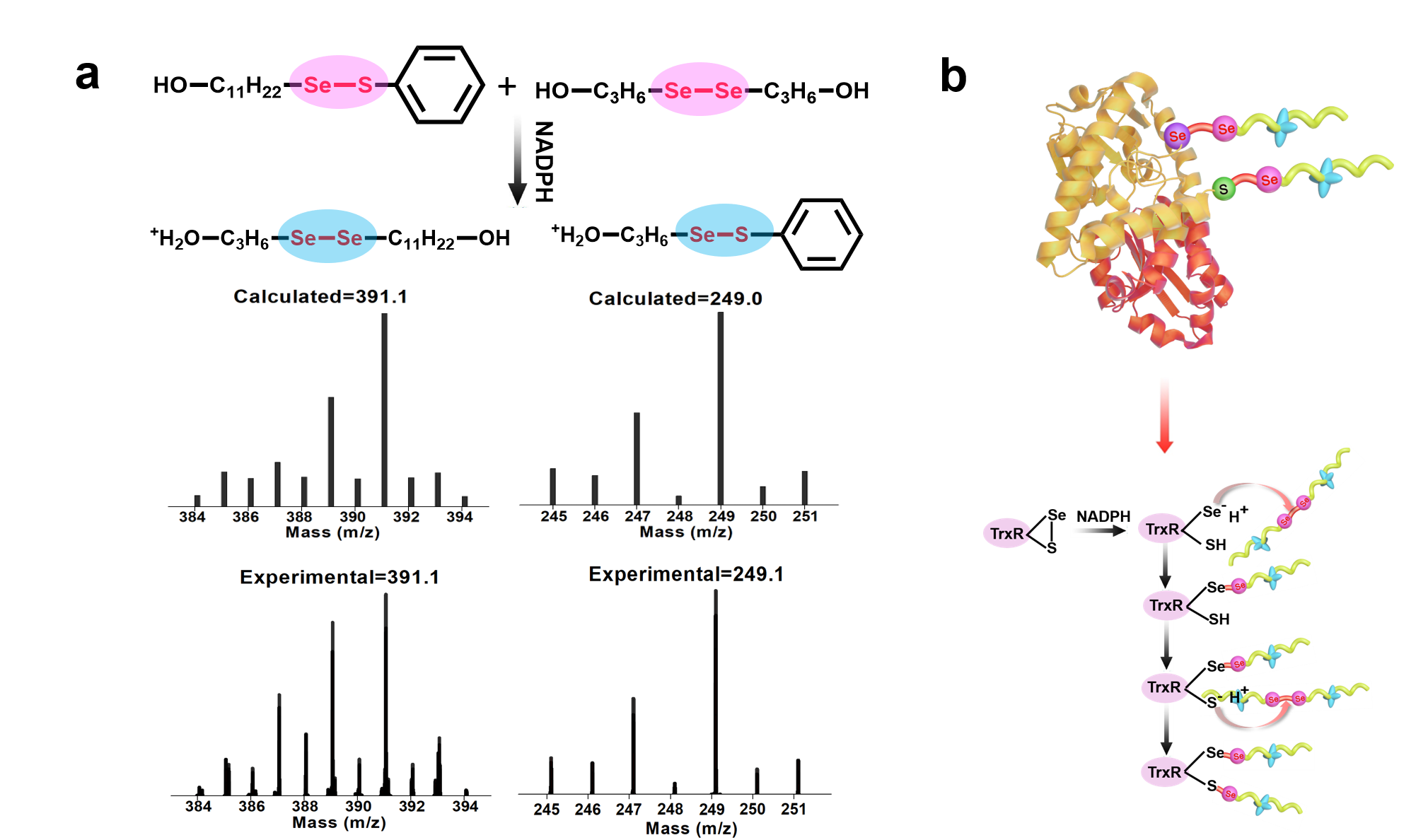
图2. 利用小分子模拟实验,验证含硒高分子胶束通过含硒动态化学反应实现TrxR活性抑制机理。
在对A549皮下肿瘤模型的治疗实验中,该含硒纳米药物递送载体可实现GEM的高效靶向递送。通过建立肿瘤原位复发与肺转移模型,直观的验证了该含硒纳米药物载体通过对TrxR活性的抑制,降低肿瘤转移与复发风险的可行性 (图3)。

图3. 建立原位复发及肺转移模型,验证该含硒纳米药物递送体系降低肿瘤转移与复发风险的可行性。
以上相关成果发表在Biomaterials上。论文的通讯作者为清华大学化学系许华平教授,第一作者为清华大学化学系杨纪春博士。
论文链接:https://doi.org/10.1016/j.biomaterials.2020.120054
- 清华大学许华平教授团队 Angew:具有β-硒代羰基结构的聚氨酯同时实现塑料降解和废物升级 2024-01-02
- 苏州大学华道本团队:第一例辐射防护高分子药物 2020-10-09
- 清华大学许华平教授课题组:含硒高分子的合成及其在动态材料及生物医学领域的应用 2018-10-25
- 四川大学何斌/蒲雨吉 ACS Nano:高分子化丁酸纳米平台治疗肠炎 2023-12-24
- 华南理工朱伟 Adv. Sci.:基于红细胞和MOF-级联酶的人工生物杂化体用于高尿酸血症治疗 2023-12-17
- 长期有效 | 西南交大周绍兵教授团队诚招博士、推免硕士 - 材料、生物医学工程 2023-09-23
