天津大学赵燕军教授、王征教授团队 ACS Nano: 自由基捕获手性高分子调控非可控炎症
2023-06-24 来源:高分子科技
非可控炎症由细胞因子风暴引发,并在诸多疾病(例如Covid-19)的发生发展中扮演重要角色。非可控性炎症的调控网络及分子机制异常复杂,可导致多器官功能障碍,目前尚无有效疗法,是亟需解决的临床问题。近年研究发现非可控炎症与多种免疫细胞的脂质代谢异常和细胞膜脂质过氧化密切相关,并具有氧化应激和炎症反应的正向串扰耦合的关键特征。脂质过氧化主要发生在细胞膜,可诱发铁死亡、焦亡、程序性坏死等多种细胞死亡形式,靶向脂质过氧化为治疗非可控炎症提供了新思路。
近日,天津大学药学院赵燕军教授、王征教授团队设计了侧链共价偶联自由基捕获功能基团的两亲性聚乙二醇-聚赖氨酸双嵌段高分子,并利用脂多糖诱导的细胞和动物模型进行了药效考察。首先,该类高分子具有α-螺旋构象,能显著延长细胞膜滞留时间,并可组装为纳米胶束 (图1)。由于细胞膜是脂质过氧化的主要场所,膜滞留显著增强了手性高分子的脂质过氧化抑制效能,进而高效抑制了包括铁死亡、焦亡和程序性坏死在内的多种细胞死亡形式,相关标记物浓度显著降低,包括丙二醛、4-羟基壬烯酸、caspase 1、caspase 11、NLRP3炎症小体、MLKL、RIPK3 (图2)。手性高分子还可显著降低多种促炎细胞因子的分泌,包括单核细胞趋化因子1 (MCP-1)、肿瘤坏死因子α (TNF-α)、白介素-6 (IL-6)和白介素-1β (IL-1β),并可上调抗炎细胞因子白介素-10 (IL-10)的浓度(图3)。此外,手性高分子胶束显著延长了小分子自由基捕获剂的体循环,提高了递送效率。该工作以“Attenuating Uncontrolled Inflammation by Radical Trapping Chiral Polymer Micelles”为题发表在《ACS Nano》杂志,天津大学药学院博士生李瑶同学为论文第一作者。

图1. 自由基捕获手性高分子促进细胞膜滞留。
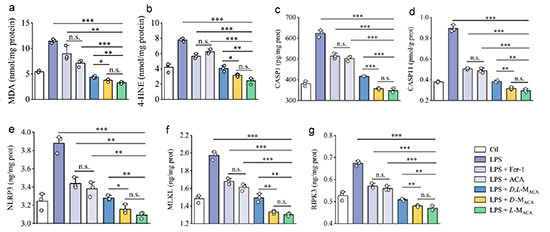
图2. 自由基捕获手性高分子抑制铁死亡、焦亡和程序性坏死。

图3. 自由基捕获手性高分子显著降低脂多糖诱导的促炎细胞因子分泌。
更多信息见课题组主页:https://www.x-mol.com/groups/dds
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.2c12356
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 浙工大徐立新/叶会见团队 AFM 封面:基于自由基捕获策略制备超高储能性能聚合物电介质薄膜 2025-02-07
- 郑州大学化学学院张伟教授团队招聘教师、博士后 - 高分子合成、手性高分子、超分子组装和功能高分子材料、DFT和分子动力学计算合成/组装 2026-03-17
- 郑州大学化学学院张伟教授团队招聘教师及博士后 - 高分子合成、手性高分子、超分子组装和功能高分子材料、DFT和分子动力学计算合成/组装 2026-01-12
- 吉大吴宗铨教授/合工大周丽团队 Angew:光控的对映选择性和螺旋选择性-活性聚合 2023-11-17
- 天津大学赵燕军教授/王征教授 ACS Nano: 缺氧条件选择性增敏细胞铁死亡 2020-11-09
- 中科大王育才/朱书/蒋为团队 Science:系统揭示高分子载体材料发生系统性清除的底层机制 2026-03-20
- 浙江大学王立教授、俞豪杰教授团队 JCIS:用于安全磁共振成像和刺激响应药物递送的纳米粒子 2025-09-09
