长春应化所陈学思/宋万通团队《Mater. Horiz.》:基于聚氨基酸的脾靶向递送mRNA的磷脂酰聚合物文库
2024-04-03 来源:高分子科技

由于mRNA的固有缺陷,建立稳定、有效和安全的递送系统对mRNA技术的应用至关重要。目前已有的递送系统中,脂质纳米颗粒(LNPs)处于临床转化的最前沿。然而,LNP也同时存在着高炎性反应和难以实现非肝组织递送等不足。相比之下,基于聚合物的mRNA递送系统具有灵活的化学结构和易于功能化的优势,表现出极大的应用潜力。但由于目前的聚合物递送系统存在细胞毒性大和转染效率低等阻碍,因此亟需进一步改进。
磷脂是生物膜和细胞器的关键成分,在细胞运输途径中起着重要作用。它们可以整合到天然生物膜中来增强材料的内涵体逃逸,从而克服当前纳米载体的限制。得益于聚合物灵活的化学结构,将磷脂与聚合物结合得到的磷脂酰聚合物可以利用这两种物质的双重优势。磷脂尾部赋予了聚合物优异的膜穿透能力,而阳离子聚合物经磷脂酰化后生物安全性得以提升。不仅如此,聚合物材料的亲疏水性、pKa值等理化参数也可以灵活调整,以满足实际需求。
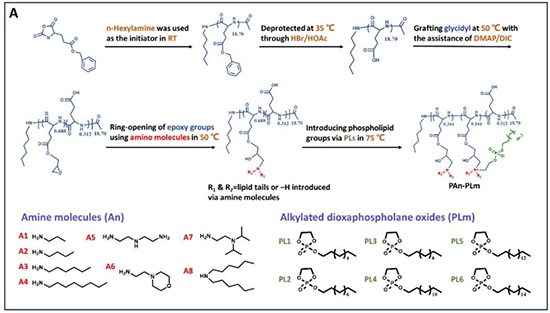
图1. PLG-PPs文库的聚合物设计和化学合成路线。
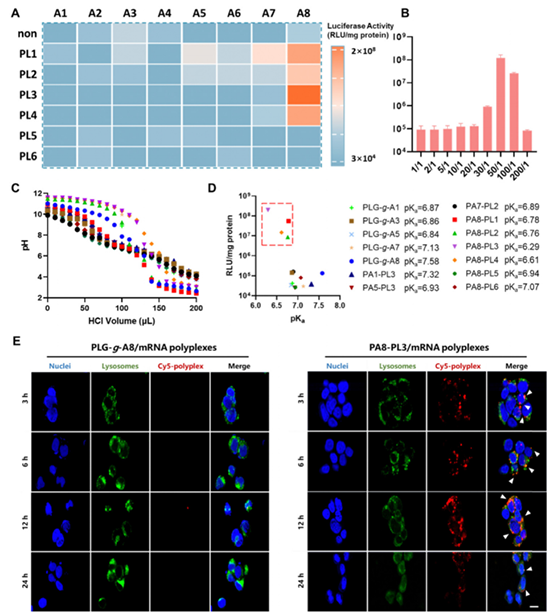
图2. PLG-PP材料的体外筛选和验证。
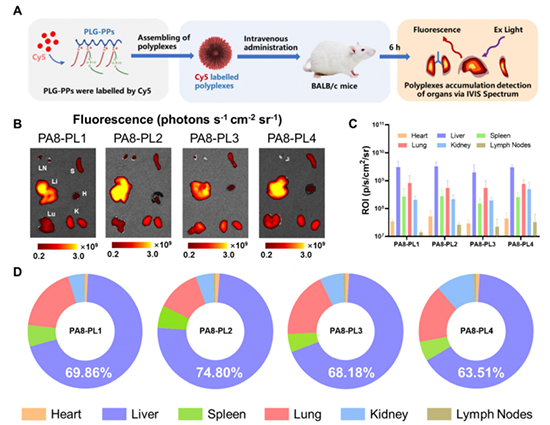
图3. PLG-PPs/mRNA的体内生物分布。
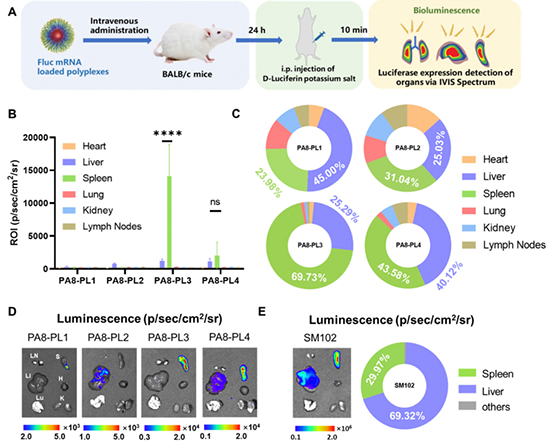
图4. PLG-PPs/mRNA的体内转染表征。
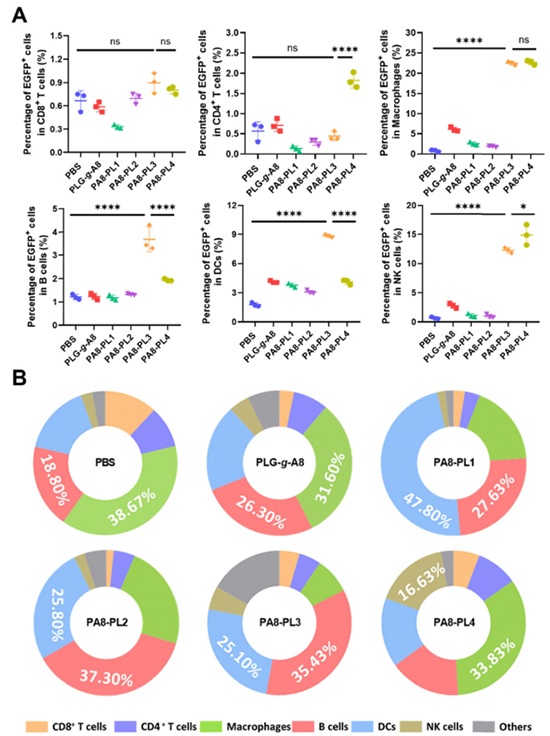
图5. PLG-PPs/mRNA的体内转染表征。
总结:
以上研究成果近期以“A polyamino acid-based phosphatidyl polymer library for in vivo mRNA delivery with spleen targeting ability”为题,发表在《Materials Horizons》上(DOI: 10.1039/d3mh02066e)。长春应用化学研究所博士研究生赵汉秦为文章的第一作者,宋万通研究员和陈学思院士为论文的共同通讯作者。该工作得到科技部、国家自然科学基金委、吉林省科学技术厅、中国科学院青年创新促进会(宋万通研究员为青促会第十批会员)等基金的支持。
原文链接:https://pubs.rsc.org/en/content/articlelanding/2024/mh/d3mh02066e
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 南京工业大学徐虹教授、李莎教授和王瑞副教授研发出可穿戴聚氨基酸水凝胶防晒剂 2019-11-01
- 中科院长春应化所陈学思研究员系统评述:聚谷氨酸接枝聚乙二醇抗肿瘤药物靶向输送系统的机遇与挑战 2019-05-22
- 东华大学史向阳教授课题组在聚谷氨酸杂化纳米凝胶的诊疗应用上取得新进展 2018-04-17
- 华东理工张大朋教授/李永生教授团队 Angew:器官靶向mRNA递送单组分Janus树枝状大分子载体 2025-04-11
- 中科大王育才/李敏团队 Nat. Biomed. Eng.: 设计低免疫原性mRNA递送载体在体内重编程耐受性APC 2025-04-01
- 西湖大学程建军教授团队 ACS Nano:阐释脂质纳米颗粒(LNP)的PEGylation修饰在肝脏mRNA递送中的构效关系 2025-02-05
- 王育才/刘庄/蒋为 JACS:发展聚合物–脂质载体通过配方优化建立mRNA器官选择性递送的定量预测模型 2026-03-03
