纤维素作为地球丰富的天然聚合物,在生物燃料、先进碳材料等领域潜力巨大,却因高度有序晶体结构中的大量氢键形成高溶解能垒,难以在常规溶剂中溶解。现有溶剂如NaOH/尿素水溶液溶解能力有限且易降解,水/乙醇混合溶剂效率低,离子液体成本高、难回收且有毒性,LiCl/DMAc等有机溶剂需苛刻预处理并产生有害废物。而氯化胆碱类深共晶溶剂(DESs, Deep eutectic solvent)虽因低毒、可生物降解等优势成为研究热点,但对其破坏纤维素晶体结构的机制探索不充分,未明确晶格缺陷的作用,也缺乏对DESs分子结构与溶解效率关联的定量研究。基于以上背景,本研究提出“缺陷介导渗透”溶解机制,通过MD模拟与实验表征结合,证实晶格缺陷是DESs高效渗透破坏纤维素晶体的核心驱动力,含π共轭氢键供体(HBD,Hydrogen bond donor)的DESs能快速诱导纤维素多晶型转变且大幅提升溶剂可及表面积;发现π共轭HBD的“双作用协同”效应,即通过“氢键+π-π堆积”双模式与纤维素作用,显著提升溶解效率,相关定量数据为高效DESs设计提供靶点;建立“热力学-动力学耦合”溶剂筛选框架,结合溶剂热力学与动力学特性构建定量标准,突破经验优化局限;系统探究聚合度与温度影响,发现低聚合度的纤维素更易被溶解,且温度对溶解度影响小,完善了溶解理论体系。这些发现为合理的溶剂筛选和分子设计建立了可转移的框架,推动了从经验优化走向基于热力学动态耦合原则的预测性范式。这里概述的机制框架广泛适用于其他生物质基底和超分子组装,要求对氢键网络进行有针对性的破坏。尽管有这些发现,纤维素再生的过程仍然复杂,仍需进一步研究。这些发现为设计下一代高效、选择性和环境兼容的绿色溶剂提供了宝贵的基础。
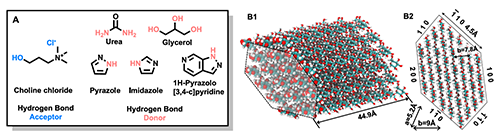
图1. (A)深共晶溶剂组成:胆碱氯化物为氢键受体(hydrogenbondacceptors,HBA);尿素、甘油、吡唑、咪唑和1H-吡唑[3,4-c]吡啶等作为氢键供体(HBD)。(B1)由多个链组成的纤维素Iβ晶体的原子模型。(B2)带标记晶格参数和层间距的纤维素Iβ的晶体晶格结构。
图2通过动态快照和散射图谱结合呈现了下列趋势,图2(A1-A4)至图2(D1-D4)以时间轴展示了乙醇/水、氯化胆碱/甘油、氯化胆碱 /咪唑、氯化胆碱/吡唑,四种溶剂体系中纤维素链的结构变化,清晰对比出π共轭DESs溶解效率远超常规溶剂和非π共轭DESs;图2(E1-E3)为SAXS(小角散射)图谱,E1对比不同溶剂平衡态下的散射曲线,图2(E2-E3)为氯化胆碱/咪唑和氯化胆碱/吡唑体系的时间分辨SAXS(小角散射)曲线,从结构层面证实π共轭DESs能破坏纤维素晶体并诱导多晶型转变。
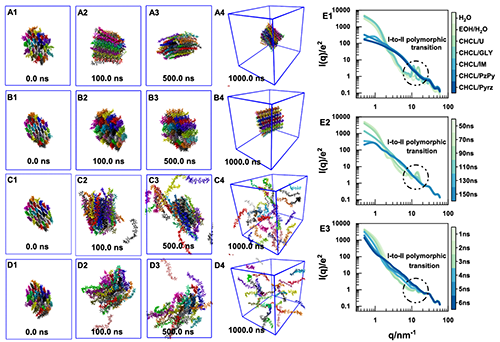
图2. 不同溶剂体系中纤维素的时间依赖性溶解行为:(A1-A4)乙醇/水,(B1-B4)氯化胆碱/甘油,(C1-C4)氯化胆碱/咪唑,(D1-D4)氯化胆碱/吡唑.(E1)各种溶剂中纤维素在平衡时的SAXS(小角散射)谱图;(E2)氯化胆碱/咪唑体系的时间分辨SAXS(小角散射)数据;(E3)氯化胆碱/吡唑体系的时间分辨SAXS(小角散射)数据.为了清晰起见,溶剂分子被省略,每个彩色链条表示一个独立的纤维素聚合物。
图3为多维度定量分析纤维素溶解的过程。图3(A)展示溶剂可及表面积(SASA)演化,体现π共轭DESs对纤维素聚集态的破坏作用;图3(B-C)呈现氢键数量变化,证实DESs破坏纤维素分子内/间氢键是溶解关键;图3(D)分析纤维素-溶剂相互作用能,表明π共轭HBD的范德华作用更强;图3(E1-E3)与图3(F1-F3)分别展示二维氢键网络和密度分布,直观呈现缺陷从表面到内部的传播及晶体解体过程。
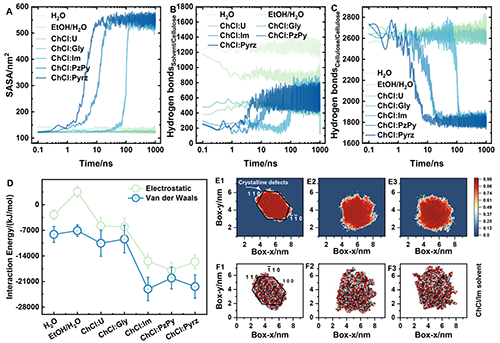
图3. 纤维素溶解动力学和结构演变的定量分析:(A)纤维素的溶剂可接触表面积(SASA)概况;(B)纤维素-溶剂和(C)溶剂-溶剂相互作用的氢键分析;(D)纤维素与溶剂之间的相互作用能;(E1-E3)二维氢键网络和(F1-F3)在5.0,50.0和60.0纳秒下氯化胆碱/咪唑中纤维素的二维密度,沿[001]轴投影。
图4(A)为WAXD衍射图谱(XRD广角散射),显示空白纤维素及经不同DESs处理后的晶体结构变化,从衍射角度证实π共轭DESs能破坏纤维素I型晶格;图4(B)以柱状图对比80℃与100℃下氯化胆碱/咪唑、氯化胆碱/甘油、氯化胆碱/尿素三种DESs的纤维素溶解度,表明氯化胆碱/咪唑溶解度更高且温度对溶解度影响小。
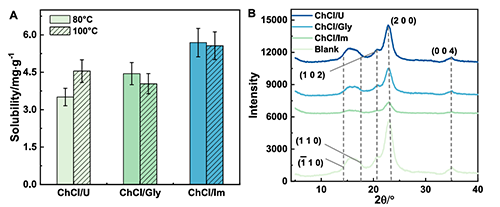
图4. (A)在80°C和100°C下不同DES的溶解度。(B)在80℃下不同深共晶溶剂(DES)溶解的纤维素的广角X射线图谱。
图5通过扫描电子显微镜观察不同溶剂处理后的纤维素宏观形貌。图5(A1-A3)为空白纤维素,呈现紧密堆积的刚性纤维束;图5(B1-B3)为氯化胆碱/咪唑处理后的纤维素,纤维破碎溶胀;图5(C1-C3)和图5(D1-D4)分别为氯化胆碱/甘油和氯化胆碱/尿素处理后的纤维素,仅出现轻微表面溶胀,直观印证不同DESs的溶解能力差异。

图5. 在不同溶剂中溶解后的纤维素的SEM图像(扫描电子显微镜):(A1-A3)空白样品,(B1-B3)氯化胆碱/咪唑,(C1-C3)氯化胆碱/甘油,以及(D1-D4)氯化胆碱/尿素,在不同的放大倍率下(5μm、10μm和20μm)。将1.0wt%的纤维素晶体添加到溶剂中。混合物在80°C下保持4-6小时。
图6从动力学和热力学维度解析溶剂性能。图6(A)为模拟系统示意图,说明参数计算的系统设置;图6(B)为均方位移(MSD)曲线,体现π共轭DESs分子迁移速度更快;图6(C1-C2)分别为扩散系数和溶剂化自由能数据,表明π共轭DESs兼具高扩散性和强热力学溶解驱动力;图(D1-D4)为范霍夫相关函数,展示不同溶剂分子的定向结合能力差异。

图6. (A)用于扩散系数计算和溶剂化自由能确定的分子动力学模拟设置示意图。(B)353K时关键物种的均方位移曲线。(C1)扩散系数,(C2)溶剂化自由能。范霍夫相关函数结果:(D1)乙醇/水,(D2)氯化胆碱/尿素,(D3)氯化胆碱/咪唑,以及(D4)氯化胆碱/吡唑。
图7定量分析聚合度(DP=6、8、10、12)对溶解的影响。图7(A)为不同DP的SASA(溶剂可及面积)演化,显示低DP纤维素更易被渗透;图7(B-C)为不同DP的氢键变化,证实低DP纤维素内部结构更易破坏;图7(D1-D5)与图7(E1-E5)分别为二维氢键网络概率分布和结构快照,直观展示不同DP纤维素的溶解过程差异。
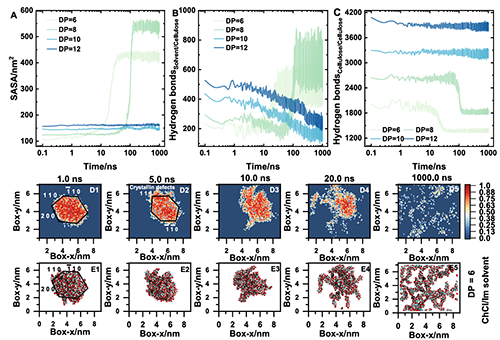
图7. 纤维素在不同聚合度(DP)下的溶解动力学和结构演变的定量分析。(A)表面积-体积比(SASA)概况;(BC)纤维素-溶剂与溶剂-溶剂相互作用的氢键分析;(D1-D5)二维氢键网络概率分布,以及(E1-E5)在不同模拟时间点的相应代表快照。
图8分析温度对溶剂分子迁移能力的影响。图8(A)为氯化胆碱/咪唑体系在不同温度下的MSD(均方位移)曲线,表明温度升高提升溶剂分子迁移率;图(B)为不同DESs的扩散系数-温度关系,显示π共轭DESs扩散系数更高且受温度影响更显著,同时结合溶解度数据明确温度并非溶解效率的核心决定因素。
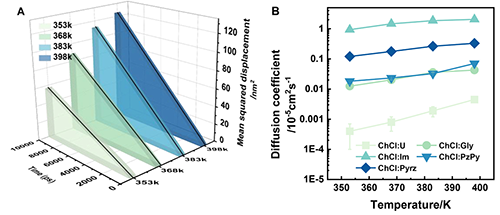
图8. 不同温度下溶剂的动态属性:(A)溶剂氯化胆碱/咪唑的均方位移轮廓,(B)不同温度下DES的扩散系数。
相关研究成果近日以“Defect-mediated permeationofdeepeutecticsolventsincellulosecrystals:Acombinedexperimentalandmoleculardynamicsstudy”为题,在线发表于Carbohydrate polymers(DOI:10.1016/j.carbpol.2025.124331)。重庆三峡学院的2024级硕士研究生余沅鸿为第一作者,重庆三峡学院宋先雨副教授为通讯作者。该工作得到来自广西大学赵双良教授、华东理工大学刘洪来教授,以及川庆钻探工程有限公司钻采工程技术研究院周楚翔工程师的支持。
原文链接https://doi.org/10.1016/j.carbpol.2025.124331
原文获取(40天内免费下载)
https://authors.elsevier.com/c/1lkyYWy0-gIpU
- 北师大汪辉亮教授团队 Nat. Commun.:具有超长室温及高温磷光的非芳香族聚合物-深共晶溶剂复合物 2026-03-31
- 华南理工大学孙大文院士团队 CEJ:双重生物激励的柔性光热共晶凝胶用于被动式界面抗冻 2024-04-16
- 哈尔滨理工大学翁凌团队 Small:基于可聚合的深共晶溶剂的自愈合导电弹性体 2023-11-26
- 兰州化物所在微/纳米胶囊单向渗透行为的研究有新进展 2009-12-11
