在严重创伤或外科手术中,失血往往决定生死。人体依赖血凝块来完成止血过程,它通过将血细胞与纤维蛋白聚集在一起,形成一个临时的屏障来阻止血液流失。然而,自身形成的血凝块并不总是可靠——形成缓慢、结构脆弱,容易在复杂生理环境中破裂或脱落。
近日,麦吉尔大学李剑宇团队和合作者提出了一种全新的解决思路:将血凝块视为一种“可设计的材料”,从结构层面重构其性能,实现更快速、更稳定的止血,并显著促进组织再生。
2026年4月29日,相关研究以“Engineering tough blood clots for rapid haemostasis and enhanced regeneration”为题发表在Nature 上。该文章的通讯作者为加拿大麦吉尔大学李剑宇教授,第一作者为蒋帅兵博士,现为哈佛医学院博后。合作者包括麦吉尔大学鲍光宇博士,杨真博士,吴靖,Joo Eun June Kim,Roselyn Jiang,Oliver Zhan,Alexander Nottegar,刘殷博士;科罗拉多大学博尔德分校龙荣教授,杨兴伟博士,麦吉尔大学Anastasia Nijnik教授,Versiti血液研究所Christian Kastrup教授, 不列颠哥伦比亚大学高祖华教授,多伦多大学Andrew Beckett教授。
被忽视的关键问题:血凝块一类高度细胞化材料的性能天然受限
从材料角度来看,血凝块属于一类典型的高度细胞化材料,其中红细胞约占45%的体积,而真正承担结构支撑作用的纤维蛋白却不到1%。 这种“巧妇难为无米之炊”的特性,使得天然血凝块在力学上较为脆弱,容易发生断裂。同时,凝血过程本身较慢,通常需要数分钟才能形成稳定结构。在高压出血、持续血流冲刷或组织运动等复杂环境中,这种结构不仅难以及时形成,还可能发生破裂或脱落,从而显著限制止血效果,甚至影响后续组织修复。
科学思维的转变:从自身凝血到人工设计凝血,从聚合物主导到细胞主导
过去的改进策略大多集中在增强纤维蛋白网络或加快凝血反应,例如提高凝血因子活性、增强纤维蛋白交联或利用血小板收缩来提升刚度。这些方法虽然在一定程度上改善了血凝块的性质,但难以同时解决两个核心问题:快速形成与力学性能跨越提升。现有的生物材料增强策略主要集中在聚合物网络的结构设计上,并不适用于血凝块这类高度细胞化材料。相比之下,直接利用数量丰富的细胞成分来构建凝血通路和承力结构,成为一种更具潜力的方向。
在这样的背景下,研究团队提出了一种全新的策略——“点击凝血(click clotting)”。该方法利用超快速的生物正交点击化学反应,在数秒内将高密度红细胞通过共价键连接起来,形成连续的细胞网络结构——细胞凝胶(cytogels),并进一步与天然凝血过程中形成的纤维蛋白网络交织,构建出工程化血凝块(engineered blood clots, EBC)。 在这一体系中,红细胞不再是被动的填充成分,而是直接参与承载外力,成为材料的基本结构单元,从而从根本上改变了血凝块的结构属性。
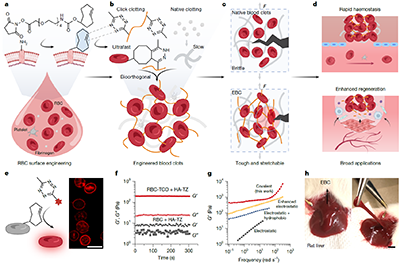
图1:点击凝血与工程化血凝块的构建原理与基本特性
为什么它更强韧?一个全新的力学机制
这一结构设计带来了一个关键的力学机制转变。研究发现,细胞凝胶的韧性提升并不依赖于增加聚合物含量,而是来源于细胞本身。在外力作用下,红细胞会逐渐发生微观破裂,从而吸收并耗散能量。实验显示,血红蛋白释放量与拉伸程度呈正相关,表明细胞破裂是材料耗能的主要来源。这种类似“牺牲结构”的机制可以有效抑制裂纹扩展,使材料在受到冲击或拉伸时不发生瞬时断裂,从而显著提高整体韧性。
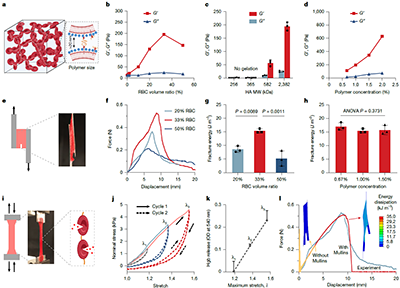
图2:红细胞凝胶的点击凝血与断裂行为
独特结构实现性能跃升
工程化血凝块构建了一种独特的互穿网络:红细胞形成连续承载与耗能网络,纤维蛋白提供结构稳定与粘附支撑。两者协同,使材料在受力时通过细胞逐步破裂耗散能量,同时保持整体完整性,从而显著增强抗破裂能力。同时,点击凝血反应的快速与可调性,使血凝块能够在数秒内形成,并实现对凝固时间的精确控制。
正是这一结构带来了显著的性能跃升。工程化血凝块相比天然血凝块,其凝固时间从分钟级缩短至数秒,同时断裂韧性提升约13倍,粘附能提升约4倍,并表现出更高的抗压能力和结构稳定性。
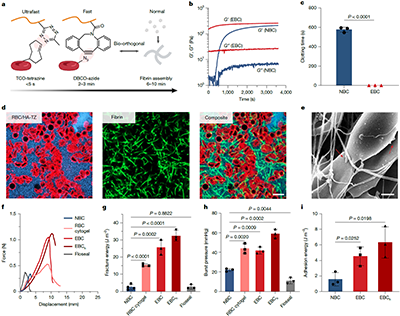
图3:工程化血凝块的结构与力学性能
体内验证:从快速止血到组织再生
更重要的是,这种材料在体内展现出显著的治疗潜力。在大鼠肝脏出血模型中,它能够迅速封堵伤口,将失血量从约1813 mg降低至24 mg,并将止血时间从265秒缩短至约5秒。 与此同时,由于其主要由天然血液成分构成,该材料表现出良好的生物相容性,不仅显著减少异物反应,降低炎症反应,还能促进组织再生。在28天内,受损组织接近完全恢复,而对照组则出现明显瘢痕。此外,该材料还显著降低了术后粘连发生率(约17% 对比 83%)。
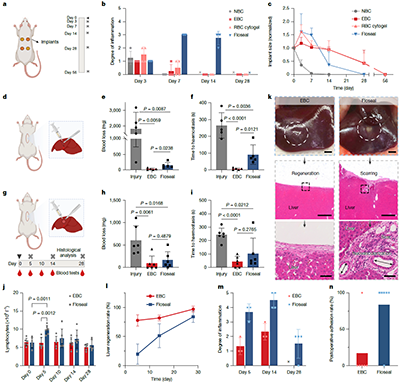
图4:工程化血凝块的生物相容性、止血效果与促进组织再生能力
结语
从整体来看,这项研究的意义不仅在于实现了更高效的止血,更在于提出了一种新的设计思路:将血凝块从一个自然形成的生物产物,转变为一个可以工程化设计的材料体系。当红细胞从“填充物”转变为“结构单元”,血凝块也随之获得了全新的功能与潜力。随着进一步的研究与临床转化,这种工程化血凝块有望在创伤急救、外科手术和再生医学中发挥重要作用。细胞凝胶策略也为工程化组织,类器官等高度细胞化材料的发展提供新思路。
李剑宇团队近年来关于止血材料和血块力学方面的其他研究如下:
(1) Guangyu Bao^, Qiman Gao, Massimo Cau, Nabil Ali-Mohamad, Mitchell Strong, Shuaibing Jiang^, Zhen Yang^, Amin Valiei, Zhenwei Ma^, Marco Amabili, Zu-Hua Gao, Luc Mongeau, Christian Kastrup, Jianyu Li*, Liquid-infused microstructured bioadhesives halt non-compressible hemorrhage, Nature Communications, 13, 5035 (2022).
(2) Shuaibing Jiang^, Shiyu Liu^, Sum Lau^, Jianyu Li*, Hemostatic biomaterials to halt non-compressible hemorrhage, Journal of Materials Chemistry B, 10, 7239-7259 (2022).
(3) Shiyu Liu^, Aram Bhamani^, Gabriella Paige Sugerman, Zhen Yang^, Manuel Rausch, Farshid Ghezelbash*, and Jianyu Li*, Adhesive and cohesive fracture of blood clots: Experiments and modeling, Journal of the Mechanics and Physics of Solids, 105858 (2024).
(4) Shiyu Liu^, Guangyu Bao^, Zhenwei Ma^, Christian J. Kastrup, Jianyu Li*, Fracture mechanics of human blood clots: Measurements of toughness and critical length scales, Extreme Mechanics Letters, 101444 (2021).
原文链接:https://doi.org/10.1038/s41586-026-10412-y
- 北京化工大学蔡晴/喻盈捷 AFM:三重生物粘附性微球赋能金属离子工程化外泌体疗法,实现血管化骨再生 2026-02-18
- 浙江大学周民教授团队《ACS Nano》:工程化微藻细胞外囊泡通过调控线粒体稳态预防放射性皮炎 2025-07-26
- 东南大学葛丽芹教授团队 CEJ 综述:具有免疫调节特性的工程化微胶囊在癌症、炎症和自身免疫中的应用 2025-04-09
- 中国科大李良彬教授团队崔昆朋/李薛宇 Macromolecules:双交联强韧聚两性电解质水凝胶的多轴应力松弛机制 2026-04-29
- 南开大学刘遵峰 Adv. Mater.:制冷新突破 - 强韧人造蛛丝用于扭热制冷 | 附26级博士招生信息 2026-03-19
- 四川大学吴锦荣教授团队 Nat. Commun.:可解缠的瞬态缠结 - 实现聚丙烯酰胺水凝胶的强韧化 2026-03-07
- 华东理工刘润辉教授与合作者《Bioact. Mater.》:易于制备的抗氧化和抗菌水凝胶薄膜 → 快速止血和促进感染性糖尿病创面愈合 2025-07-31
