在人体中,能量代谢主要依赖以D-葡萄糖作为能源物质的三羧酸循环,在长期的进化中,人体形成了一套精细的、专一性识别和代谢葡萄糖分子的生物系统。随着人民生活水平提高,糖尿病这一“无声的杀手”已经严重危害民众健康并给社会带来了沉重的经济负担。频繁检测血糖含量和注射胰岛素的治疗方式给患者带来不适,也存在着注射剂量难以控制和血液疾病传播等潜在风险。因此,研制智能控释胰岛素释放的仿生生物材料,是一种实现糖尿病患者血糖水平长效控制的理想解决方式。
无论是食品中还是人体的体液中,均存在多种葡萄糖同分异构体,人体的生物酶可以准确地识别葡萄糖分子,具有高度专一性,但是人工合成具有专一性识别葡萄糖分子的化学结构非常困难。这是由于葡萄糖分子与其同分异构体(例如半乳糖、果糖等)的分子结构极其相似,并且它们只有单一的羟基官能团,难以被精确的化学识别。已报道的少数具有葡萄糖专一性识别能力的化学配体几乎都存在合成过程比较复杂等问题。
最近,陕西科技大学陈咏梅教授和王任其副教授团队与郑州大学梅英武副教授合作,利用β-环糊精主环直径与葡萄糖分子尺寸相匹配这一特点,设计了一种基于二齿-β-环糊精的水凝胶体系。通过在2,6-二甲基- β-环糊精(DMβCD)上精确引入一对苯硼酸取代基团,形成符合D-葡萄糖分子拓扑结构的分子狭缝,可专一性地与D-葡萄糖分子结合并释放出质子,造成水凝胶体积溶胀,从而促使水凝胶中预载的胰岛素快速释放到血液环境中。二齿-β-环糊精的制备仅需3步反应,不需要苛刻的合成条件,而且反应收率很高。装载二齿-β-环糊精的水凝胶在I型糖尿病小鼠体内快速响应高血糖症并释放胰岛素,可实现12小时内长效控制血糖水平。
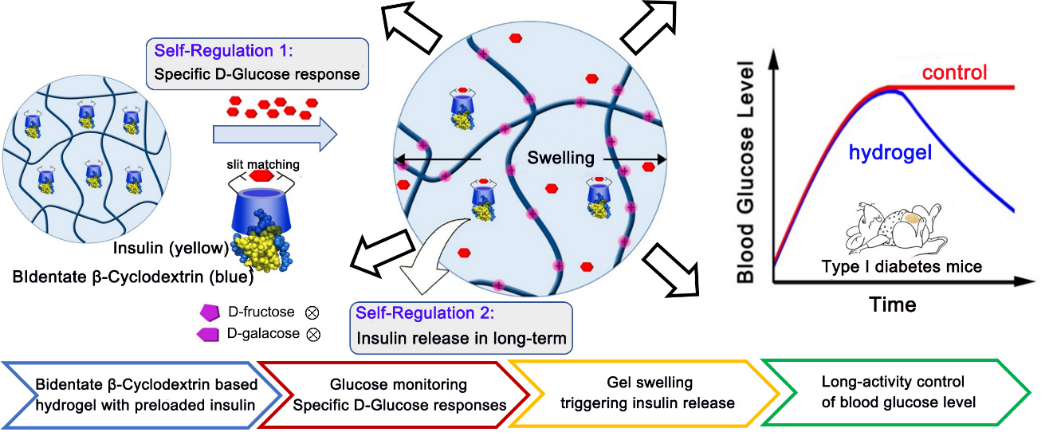
新型D-葡萄糖配体——二齿-β-环糊精
与以往化学合成的D-葡萄糖配体不同,二齿-β-环糊精具有良好的生物相容性,并且制备方法简便。研究者利用β-环糊精主环直径与D-葡萄糖分子尺寸相匹配的特征, 在β-环糊精主环上精确引入了两个苯硼酸取代基团,形成与D-葡萄糖分子拓扑结构和顺式二羟基官能团均匹配的分子缝隙,从而制备可专一性识别D-葡萄糖的二齿-β-环糊精。利用基质辅助激光解吸飞行时间质谱(MALDI-TOF-MS),核磁氢谱和二维核磁(COZY和NOESY)表征(图1),证实了新型β-环糊精的超分子结构。
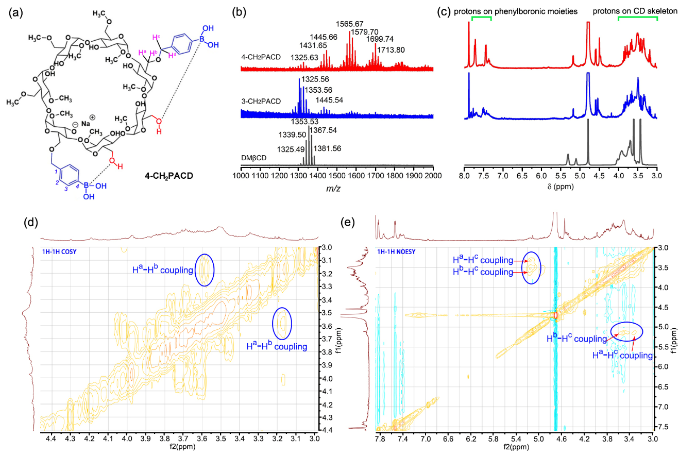
图 1 (a)二齿环糊精(4-CH2PACD)的分子结构, (b) MALDI-TOF-MS, (c) 1H NMR 图谱 DMβCD (黑色), 3-CH2PACD (蓝色),和 4-CH2PACD (红色), 4-CH2PACD 的2D 1H-1H COSY (d)和1H-1H NOESY (e).
葡萄糖专一性响应
如图2a所示,含有二齿-β-环糊精的聚丙烯酰胺水凝胶(4#)在葡萄糖溶液中会发生膨胀,而该水凝胶在不含葡萄糖的PBS溶液中(3#)不会发生膨胀。图2b为显微镜照片,二齿-β-环糊精在水凝胶中呈现直径约为100 微米的微粒(3#),在葡萄糖溶液中,由于葡萄糖与二齿-β-环糊精上的苯硼酸基团产生相互作用,导致二齿-β-环糊精微粒分解(4#)。如图2c所示,该凝胶体系在葡萄糖溶液中的膨胀响应呈现先快后慢的速率,最终膨胀系数约达到20%。在一系列D-葡萄糖的同分异构体中,二齿-β-环糊精水凝胶呈现专一性响应D-葡萄糖的膨胀行为。当葡萄糖的浓度达到40mM时,含有10mM二齿-β-环糊精的水凝胶膨胀系数达到最大值。
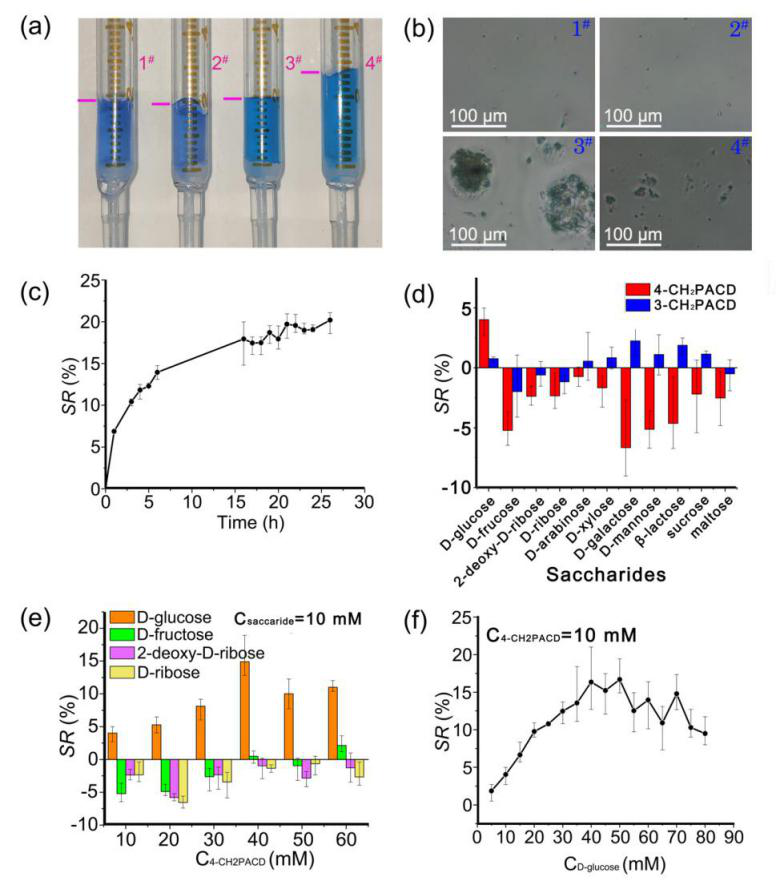
图2 (a)葡萄糖溶液中水凝胶膨胀,(b)水凝胶显微照片,(c)膨胀系数随时间变化曲线,(d)水凝胶膨胀对糖的选择性,(e)水凝胶膨胀系数随不同糖及浓度变化,(f)水凝胶膨胀系数随葡萄糖浓度变化
长效血糖浓度控制的按需释放胰岛素水凝胶
I型糖尿病小鼠模型的体内研究证实,尽管双齿β-CD水凝胶预载了短活性胰岛素,它在12小时内对血糖水平进行长时间控制。
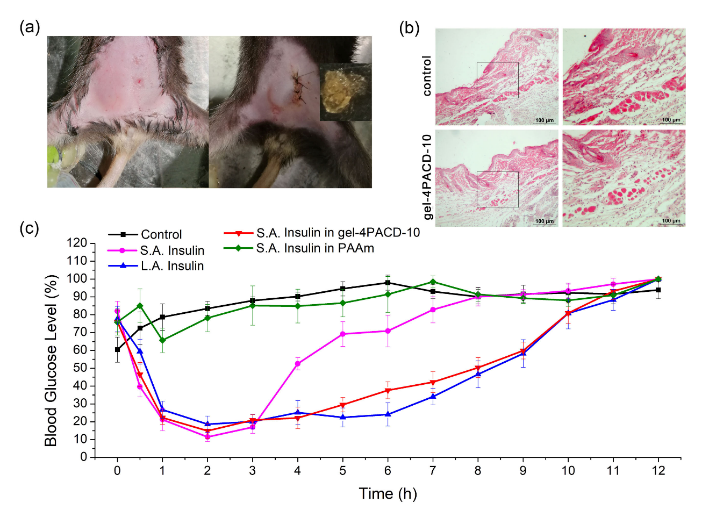
图3 腹腔注射胰岛素或腹腔植入胰岛素预载水凝胶的治疗效果。(a)小鼠植入胰岛素预载凝胶-4PACD-10前后的照片,插图显示胰岛素预载凝胶在小鼠腹腔内停留12小时后,凝胶呈血浆淡黄色,(b)H&E染色结果,(c)未治疗的糖尿病小鼠(对照组,黑色)和注射短活性胰岛素(S.A.胰岛素,粉红色)、长活性胰岛素(L.A.胰岛素,蓝色)、短活性胰岛素预载凝胶(红色)治疗糖尿病小鼠血糖水平的变化曲线。
通过简便的合成方法制备了一种基于二齿 β-CD的新型葡萄糖配体。该二齿 β-CD( 4-CH2PACD)包含葡萄糖狭缝,并显示出与 D-葡萄糖的高效特异性结合。将4-CH2PACD 掺杂到水凝胶中,赋予水凝胶对 D-葡萄糖的特异性体积响应。高浓度D-葡萄糖导致凝胶膨胀,该特征有助于实现自我调节的特定葡萄糖响应性胰岛素释放。动物实验表明,在糖尿病小鼠中植入预加载二齿 β-CD 和短活性胰岛素的水凝胶能够实现长效血糖控制,为双重自我调节智能胰岛素释放系统提出了一种新思路。
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202104488
团队负责人介绍

陈咏梅,陕西科技大学特聘教授,博导,获日本北海道大学博士学位,师从世界著名凝胶材料专家Yoshihiro Osada和Jian Ping Gong教授。曾任日本北海道大学特任助教、特任副教授,西安交通大学教授、博导。兼任中国化学会应用化学学科委员会委员,中国生态学学会微生物生态专业委员会委员,中国微米纳米技术学会纳米科学技术分会纳米生物材料专业委员会委员。主持国家自然科学基金面上3项、高等学校博士学科点专项基金、教育部留学人员回国启动基金、科技部政府间科技合作项目等10余项。以第一或通讯作者在Chem. Soc. Rev.、Nat. Commun.、Adv. Funct. Mater.、Small、Biomaterials、Green. Chem.、ACS Appl. Mater. Interfaces、Nanoscale等国际影响力期刊发表论文60余篇,其中ESI高被引论文3篇,授权国家专利18件,日本专利2件,美国专利1件,2017年入选英国皇家化学会综合化学领域Top1%高被引中国作者榜单。
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 南通大学孙文旭/张雷团队 AFM:仿生界面工程设计兼具高拉伸与高灵敏度的双纳米复合水凝胶 2026-05-29
- 华东理工刘润辉教授课题组 JACS:双胍基化聚噁唑啉-胰岛素复合物在小型猪中实现长效葡萄糖响应性胰岛素释放 2025-10-25
- 合工大胡颖团队 AFM:植物叶片启发的可编程形变与湿致变色软体驱动器 2026-03-28
- 武汉大学刘兴海教授团队《Small》:仿生超韧快速响应水凝胶 2026-02-02
- 兰州大学吕少瑜 Adv. Mater.:破局“强韧矛盾” - 利用可调晶域实现水凝胶磷光寿命和韧性协同增强 2025-10-16
