组织诱导性生物材料是一种不添加细胞和(或)生物活性因子,经过设计用于受损或缺失的组织或器官再生的生物材料,已列入二十一世纪生物材料定义,代表生物材料发展的新方向和前沿。材料诱导组织再生的理念源于生物材料骨诱导性的发现和确证,其典型代表是已获批上市的骨诱导磷酸钙生物陶瓷,广泛应用于临床骨缺损的再生修复,表现出媲美自体骨和生长因子的修复效果。尽管如此,陶瓷本身的脆性使其在承重部位骨缺损修复应用中有较高的风险。相较于生物陶瓷,医用金属和高分子材料具有广阔的力学调控空间,在承重骨修复方面具有独特的优势。在生物材料骨诱导理论指导下,前期已有骨诱导性多孔金属的相关报道,但开发兼具骨诱导性和适宜力学强度的医用高分子材料一直是骨科生物材料领域面临的难题和挑战,至今鲜有成功报道。

在研究过程中,首先通过对PEKK支架表面进行磺化处理,引入多微孔结构和亲水性SO3H-基团,诱导类骨磷灰石纳米粒子在支架表面的原位自组装和生长沉积,实现多尺度结构和力学仿生PEKK支架的设计和构建。

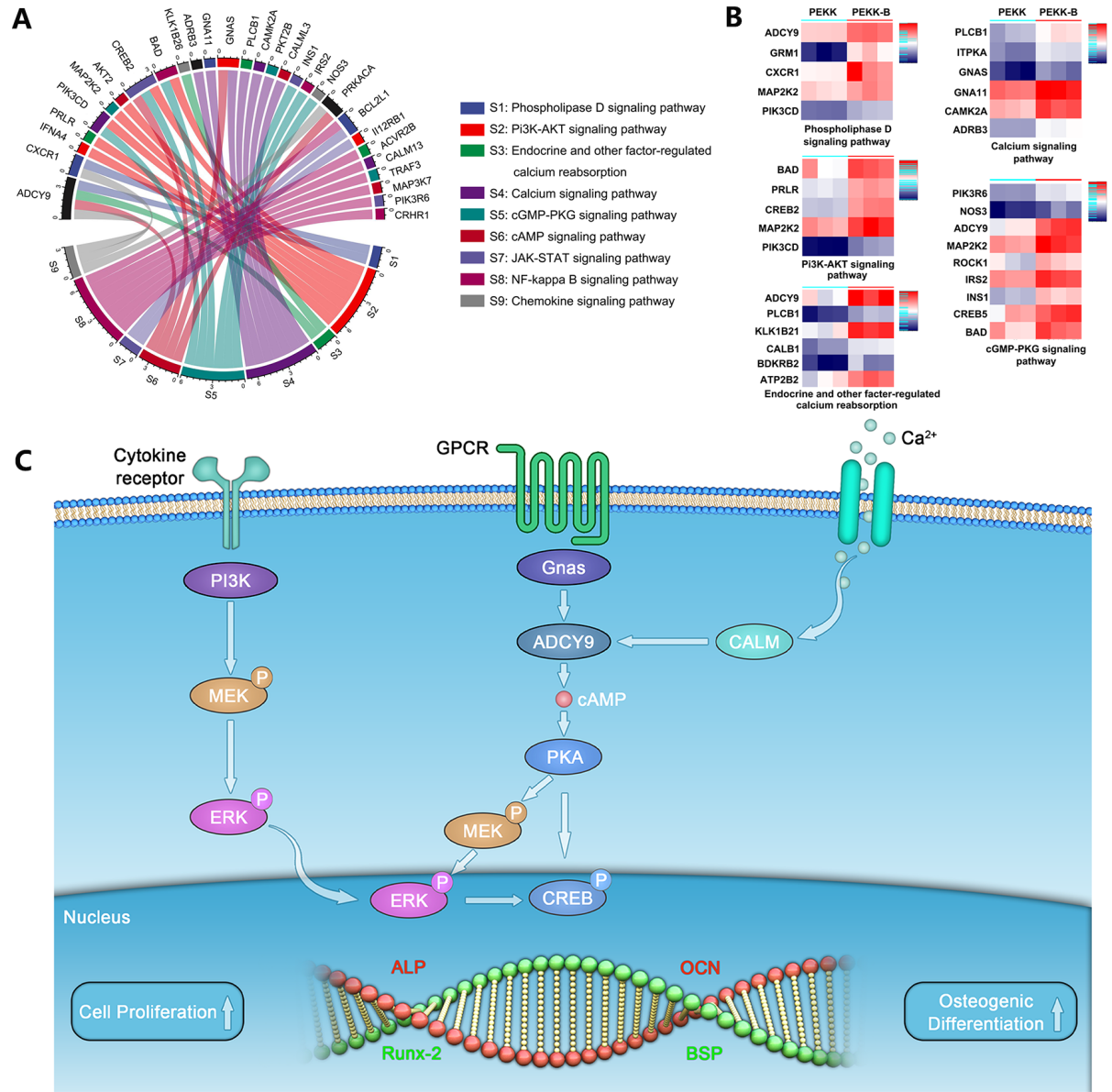
生物材料诱导骨再生的内涵机制是极其复杂的,涉及材料和多细胞及蛋白的相互作用。其中,干细胞(MSCs)的来源和分化途径仍是目前研究的关键问题。前期许多研究已经证实材料可以通过刺激MSCs中的BMP2和其他信号分子促进其向成骨分化,但材料刺激MSCs表达这些信号分子的具体途径仍是未知的。本研究发现,ADCY9在仿生PEKK诱导干细胞分化过程中发挥了关键作用。进一步研究证实,ADCY9能够通过介导cAMP/PKA信号通路促进MSCs成骨分化,诱导异位骨形成。
小结:本研究结果确证了生物材料骨诱导性在医用高分子材料中的普适性,既是对我国原创生物材料组织诱导理论的补充和完善,还为新型骨和其它组织诱导类植入器械开发提供了研究思路和材料基础。
论文链接:https://www.science.org/doi/10.1126/sciadv.abq7116
- 四川大学吴宏教授团队 Nat. Commun.:碳纤维骨架仿生原位生长氮化硼网络用于高效散热与电磁屏蔽 2026-05-20
- 俞书宏/何振团队 Nat. Commun.: 牙釉质启发兼具高力学和自修复性能的仿生纳米复合材料 2026-05-19
- 多伦多大学Eugenia Kumacheva团队 AFM:AI赋能多组分复合水凝胶逆向设计-精准定制仿生粘弹性网络 2026-05-14
- 四川大学于海洋/魏强 Adv. Sci.:种植体用皮质骨启发的功能化复合材料 - 与皮质骨力学-生物性能适配抗微动磨损 2023-02-28
- 温医大宋伟宏院士团队包敏课题组全球招聘研究员、副研、博后 - 神经生物学、脑科学、分子/细胞生物学、生物材料学、生物力学、生物信息学 2026-04-17
- 浙江大学高长有团队 Prog. Mater. Sci.:用于组织修复的自适应性生物材料 2025-11-30
- 武汉理工戴红莲课题组 Coordin. Chem. Rev.:苯硼酸生物材料 - 从化学原理到材料设计 2025-09-23
