化疗是许多实体恶性肿瘤的主要治疗方法,因其缺乏靶向性,会形成更适合恶性肿瘤转移的免疫抑制性肿瘤微环境(TME)。该微环境中的肿瘤浸润细胞毒性T淋巴细胞(CTLs)水平较低,而免疫抑制细胞如调节性T细胞(Tregs)和M2型肿瘤相关巨噬细胞(TAMs)的水平较高,从而限制了化疗疗效。因此,选择合适的化疗药物靶点和调节免疫微环境的双重策略,将有效诱导机体的正向免疫应答反应,从而达到理想的治疗效果。
在众多化疗方式中,以内质网(ER)为靶点的治疗很有前景。众所周知,内质网是蛋白质折叠和运输的主要场所,参与多种细胞功能。肿瘤细胞的过度增殖导致错误折叠和未折叠蛋白的增加,从而引发内质网应激(ERS)。为了解决这个问题,肿瘤细胞启动一种生存机制恢复细胞稳态,称为未折叠蛋白反应(UPR)。IRE1α-XBP1是UPR中最保守的进化分支,调节相关基因的表达,恢复肿瘤细胞的稳态和生存。丰加霉素(Toy)是一种嘌呤核苷类似物,通过阻断IRE1α-XBP1信号通路,使肿瘤细胞产生持续性的内质网应激,从而引起肿瘤细胞凋亡和免疫原性死亡(ICD)。值得注意的是,持续性的化疗会使肿瘤细胞表面免疫检查点配体的表达上升,从而产生免疫逃逸。免疫检查点阻断(ICB)疗法通过使用程序性细胞死亡配体1(PD-L1)等抗体,可以重新激活T细胞,增强抗肿瘤免疫治疗。
为了实现肿瘤的高效治疗,需要开发集诊断和治疗于一体的纳米平台。金纳米粒子(Au NPs)具有较高的原子序数、X射线吸收系数和良好的生物相容性等优点,在计算机断层扫描(CT)成像中具有巨大潜力。同时已有研究表明,含Au NPs的树状大分子纳米材料可诱导巨噬细胞复极化为M1型,在CT成像引导下实现增强的肿瘤免疫治疗。
在众多的纳米平台中,纳米凝胶(NGs)集合了纳米材料和凝胶的双重特性,具有三维网状结构、高水合性、高收缩扩张特性等优点,因此受到研究者的关注。TME响应性(如氧化还原)纳米凝胶一方面通过增强的通透和滞留效应(EPR),高效聚集在肿瘤部位,降低毒性反应;另一方面实现了化疗药物在肿瘤部位的精准释放,减少不良反应。目前在众多的聚合物纳米材料中,第3代聚酰胺-胺(PAMAM)树状大分子(G3.NH2)具有高度的分支结构和丰富的表面官能团,因此可以作为合成纳米凝胶的一种前体材料。
肿瘤组织丰富的细胞外基质,降低了肿瘤微环境中的血流灌注,最终阻碍药物递送到肿瘤细胞。超声靶向微泡破坏(UTMD)技术利用微泡产生的瞬间空化效应增加血流灌注,使纳米材料在肿瘤部位有效富集。因此,诊疗一体化纳米平台在UTMD技术的联合作用下,可以进一步增强癌症的精准监测和高效治疗。

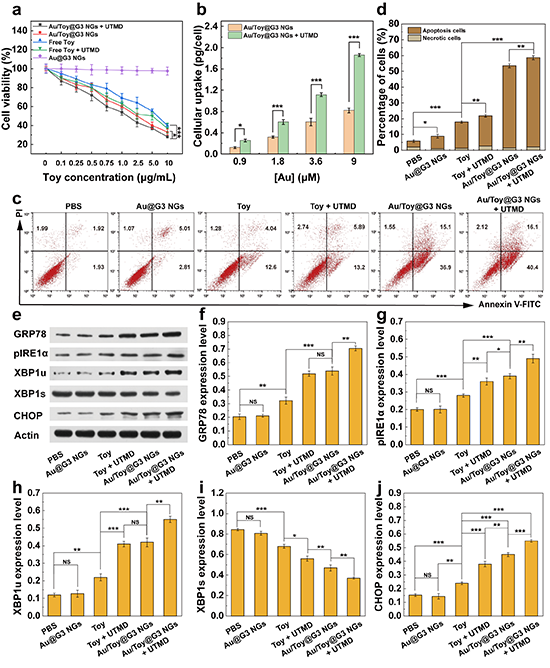
图3.(a)不同材料处理后Pan02细胞的活力;(b)Pan02细胞在不同浓度Au/Toy@G3 NGs和Au/Toy@G3 NGs + UTMD处理6 h后,对Au NPs的吞噬情况;(c-d)不同材料处理后Pan02细胞的凋亡流式分析和定量分析;(e)内质网应激相关蛋白的Western blot实验结果图;(f-j)不同材料处理后Pan02细胞内相关蛋白的表达水平。
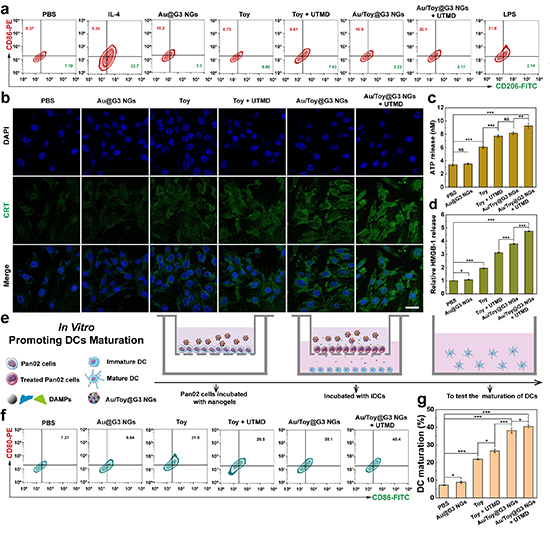
图4.(a)Pan02经不同实验组处理后的流式分析图;(b)Pan02经不同实验组处理后CRT的表达,(c)ATP的分泌,(d)HMGB-1的释放情况分析图;(e)Transwell示意图;(f-g)树突细胞的熟化情况结果分析图。


图6.(a)小鼠肿瘤部位CD86和CD206染色结果;(b)小鼠肿瘤部位CD4+和CD8+T细胞的分布情况;(c)小鼠肿瘤部位Tregs的表达情况;(d-f)CD4+ T、CD8+ T细胞和Tregs细胞的表达水平;(g)脾脏CD4+和CD8+ T细胞的免疫荧光染色结果分析。
简而言之,该研究设计的Au/Toy@G3 NGs具有以下优势:1)通过反相微乳液法形成的杂化NGs,在TME中响应性释放Au NPs和Toy,以提高它们的生物利用度;2)Au/Toy@G3 NGs一方面可通过Toy增强的内质网应激介导肿瘤细胞凋亡和免疫原性死亡,进一步刺激树突细胞熟化,从而激发抗肿瘤免疫反应;另一方面,Au NPs可将TAMs从M2型转向M1型,重新调控免疫抑制TME,在增强抗肿瘤免疫治疗的同时实现肿瘤CT成像;3)UTMD增强的肿瘤渗透和PD-L1抗体介导的ICB,可以实现增强的抗肿瘤化学/免疫联合治疗效果。本研究构建的响应型Au/Toy@G3 NGs在UTMD增强的组织穿透力和CT成像引导下,通过靶向肿瘤细胞和免疫细胞的化学/免疫联合治疗策略,实现了肿瘤高效诊疗疗,为开发新型肿瘤高效治疗纳米药物提供新思路。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202301759
- 东华大学史向阳团队 ACS Materials Lett.:树状大分子纳米凝胶共递送药物/免疫激动剂用于缓解肿瘤耐药 2024-01-05
- 东华大学沈明武研究员/史向阳教授团队 AFM:仿生外泌体伪装的pH响应型树状大分子纳米凝胶作为疫苗通过重编程多种细胞类型治疗胰腺癌 2026-02-20
- 东华大学沈明武研究员/史向阳教授团队:不对称含磷树状大分子递送菠萝蛋白酶用于骨关节炎的抗炎和软骨保护治疗 2025-06-13
- 东华大学史向阳教授团队:外泌体包裹的响应性树状大分子纳米凝胶可实现急性肺损伤的免疫调节和抗氧化联合治疗 2025-05-15
- 华科大李子福教授 Nat. Commun.:相变纳米凝胶赋能生物医学新突破 2025-12-22
- 山东大学栾玉霞教授团队 Nat. Nanotech.:发现解决CAR-T细胞疗法实体瘤疗效受限的有效方法 2025-05-20
- 东华大学史向阳/沈明武团队 Acta Biomater.:仿生含铜纳米凝胶用于磁共振成像引导的肿瘤化疗-化学动力学治疗-免疫治疗 2024-10-03
