中科大王育才/蒋为团队《Nat. Nanotechnol.》:写进教科书级的发现,提出纳米药物肿瘤递送新理论
2023-09-15 来源:高分子科技
肿瘤血管是纳米药物进入肿瘤组织的主要途径,因此纳米药物的高效递送在很大程度上依赖于肿瘤血管系统。目前的研究范式主要基于1986年首次提出的“增强渗透和滞留效应”(EPR, Enhanced Permeability and Retention effect)。该理论认为,肿瘤血管内皮细胞屏障是纳米药物渗透到肿瘤组织的最后一道防线,纳米药物可以利用肿瘤血管的高渗透性来跨越这一屏障,从而直接进入肿瘤基质。然而,临床前和临床研究的结果均显示,纳米药物对肿瘤的递送效率仍然不尽如人意。某些研究数据甚至表明,纳米载体仅能将大约0.7%的药物有效递送至肿瘤组织。这一发现不禁引发了疑问:是否存在其他尚未被充分认识的机制,这些机制可能在非内皮细胞屏障层面阻碍了纳米药物的血管外渗透?

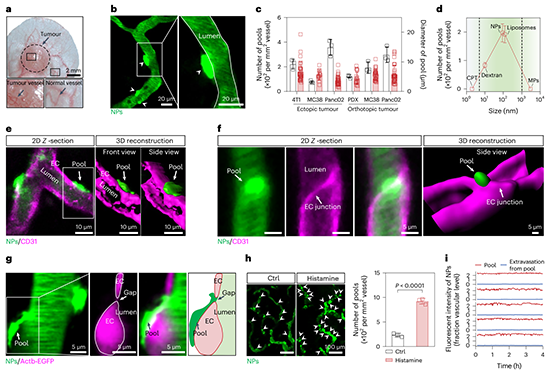
图1. 纳米颗粒在肿瘤血管外形成血池。
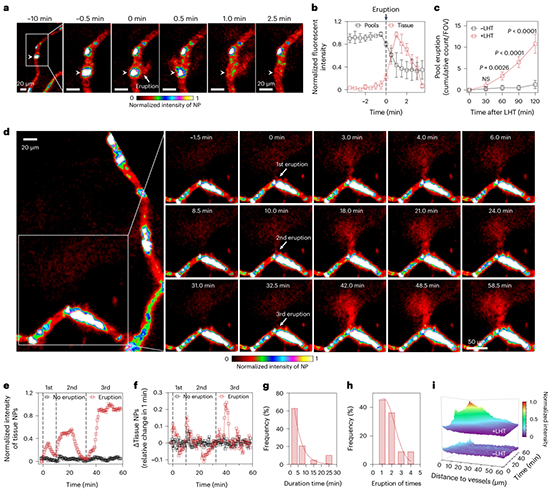
图2. 急性炎症诱导的血池喷发将“困住”的纳米颗粒释放到肿瘤间质中。

图3. 基底膜是阻止纳米颗粒进入肿瘤的屏障,通过急性炎症突破基底膜屏障,诱导火山式喷发。
原文链接:https://www.nature.com/articles/s41565-023-01498-W
版权与免责声明:中国聚合物网原创文章。刊物或媒体如需转载,请联系邮箱:info@polymer.cn,并请注明出处。
(责任编辑:xu)
相关新闻
- 中科大王育才/蒋为团队 Nat. Biomed. Eng.: 利用一氧化氮(NO)突破肿瘤血管基底膜屏障,增强纳米药物瘤内递送 2025-05-03
- 浙江大学姚克、韩海杰团队 Sci. Adv.:基底膜仿生水凝胶促进角膜损伤少瘢痕化愈合 2024-12-23
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 海南大学吴锡龙教授 AFM:聚焦纳米药物瘤内穿透难题 - 以超声/磁场双引擎驱动实现S型异质结纳米晶的深层肿瘤消融与免疫激活 2026-03-26
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 王育才/刘庄/蒋为 JACS:发展聚合物–脂质载体通过配方优化建立mRNA器官选择性递送的定量预测模型 2026-03-03
- 昆士兰大学乔瑞瑞教授团队 AFM:液态金属纳米颗粒赋能高分辨水凝胶3D打印 2025-12-01
