近日,浙江大学化学工程与生物工程学院申有青教授团队在化学领域顶级期刊《Chemical Reviews》发表题为《Tumor Abnormality-Oriented Nanomedicine Design》的综述文章,对肿瘤异常微环境进行了系统梳理,并对基于肿瘤异常微环境指导的纳米药物设计进行了深入的讨论、总结与展望(图1)。文章的通讯作者为浙江大学申有青教授、周珠贤副教授和邵世群研究员,第一作者为浙江大学周泉研究员和相佳佳研究员。浙江大学化学工程与生物工程学院为论文第一单位。
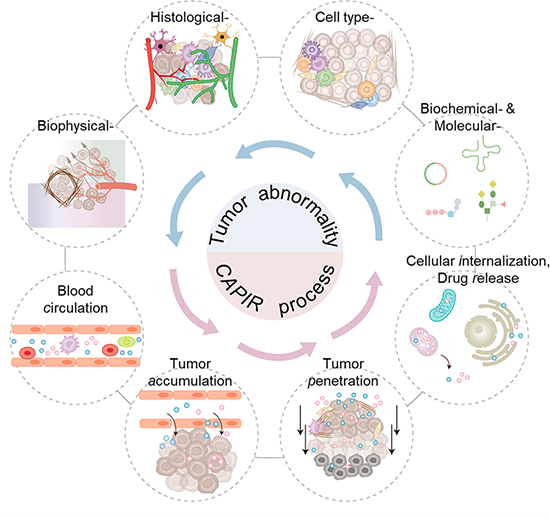
图1 面向肿瘤异常微环境的纳米药物递送载体构建
纳米药物在未来肿瘤治疗中被寄予厚望。与小分子药物相比,其能显著降低毒副作用,改善患者生存质量。迄今为止,已有超过20种纳米药物被批准临床使用,且有多个纳米药物正在临床试验当中,但目前商品化的纳米药物在疗效上未有显著改善。因此,进一步提高疗效是目前抗肿瘤纳米药物领域亟待解决的难题。
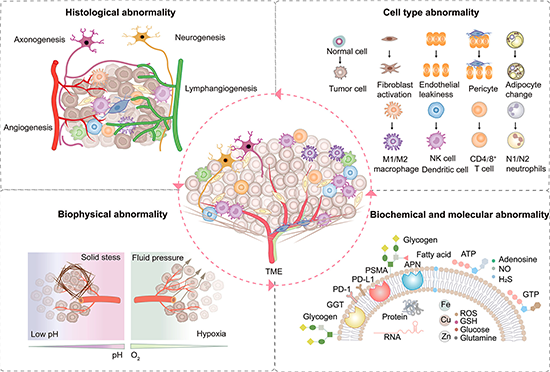
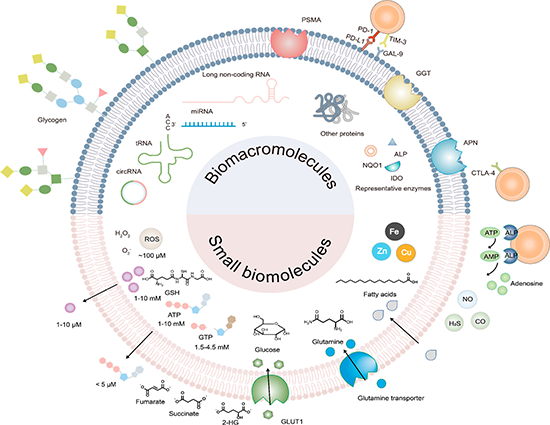
图3 部分肿瘤异常生理信号
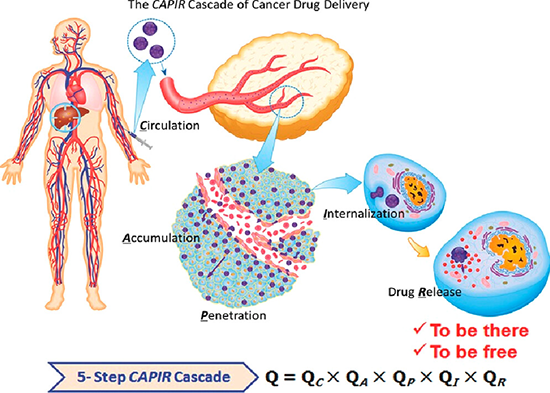
图4 肿瘤靶向药物输送过程(CAPIR,Adv. Mater. 2017, 29, 1606628)
从上述肿瘤靶向输送过程的复杂性可以看到,结构和功能简单的纳米药物无法完成这一CAPIR过程、难以获得高的疗效。因此研究者们往往通过集成各功能基元于一体,获得多功能的纳米药物以提升其递送效率,但这种多基元集成(All-into-One)的纳米药物,基本上都会面临着制造过程质控困难、体内命运和ADME难以表征清楚的困境,临床转化往往困难重重,极大程度上束缚了纳米药物的发展。因此,研究者们一直幻想着用最简单的设计来获得既高疗效又方便临床转化的纳米药物。
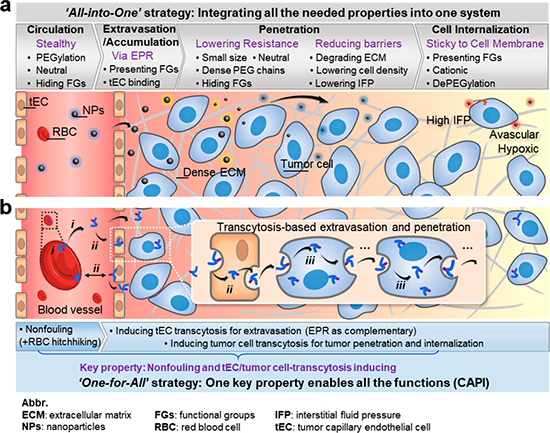
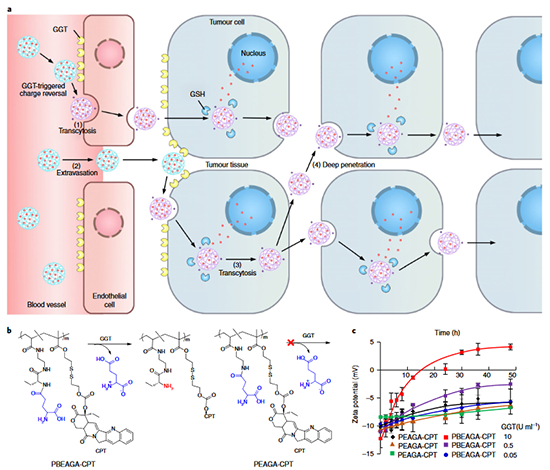
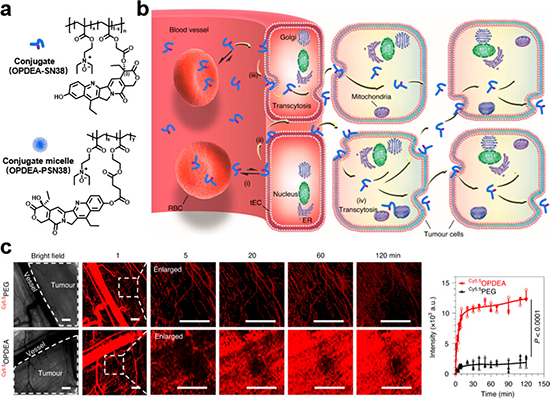
图7 基于氮氧化物的One-for-All递送策略(Nat Biomed Eng 5, 1019–1037 (2021))
论文信息:https://pubs.acs.org/doi/10.1021/acs.chemrev.3c00062
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 海南大学吴锡龙教授 AFM:聚焦纳米药物瘤内穿透难题 - 以超声/磁场双引擎驱动实现S型异质结纳米晶的深层肿瘤消融与免疫激活 2026-03-26
- 北京化工大学王兴教授团队《Adv.Healthc.Mater.》:基于双抗生素的pH响应型无载体纳米药物高效治疗混合细菌感染 2025-08-11
- 中科大王育才/朱书/蒋为团队 Science:系统揭示高分子载体材料发生系统性清除的底层机制 2026-03-20
- 浙江大学王立教授、俞豪杰教授团队 JCIS:用于安全磁共振成像和刺激响应药物递送的纳米粒子 2025-09-09
- 东南大学葛丽芹教授与合作者 Research:微气泡为模板的免疫活性金属多酚胶囊用于药物递送和增强的肿瘤免疫治疗 2025-07-31
