首个获批临床应用的聚合物胶束制剂——Genexol®PM是以mPEG-PDLLA为载体材料的载紫杉醇聚合物胶束。相较于此前的两代紫杉醇制剂——紫杉醇注射液和紫杉醇白蛋白纳米粒,Genexol®PM有效提升了紫杉醇的最大耐受剂量,并缓解了注射液中增溶剂聚氧乙烯蓖麻油相关的不良反应,在提高抗肿瘤疗效和减轻毒副作用方面表现出巨大优势。聚合物胶束是经自组装形成的动态平衡体系,由于缺乏适合的检测方法和有效的体内分离手段,关于聚合物胶束体内命运的研究长期以来进展缓慢。此外,复杂的体内环境增加了胶束体内命运的不确定性,为研究带来了更大的困难和挑战。
鉴于此,复旦大学占昌友教授团队开发了一种基于抗PEG单链抗体(anti-PEG scFv)的亲和诱捕分离方法,并借助该方法重新探究了静脉注射后载紫杉醇mPEG-PDLLA聚合物胶束的体内命运,相关成果发表于Nano Today杂志上。
亲和诱捕法实现PEG化聚合物胶束的高效分离
通过将anti-PEG scFv与PEG化聚合物胶束进行孵育可引发胶束聚集,随后向体系中引入的Ni-NTA琼脂糖凝胶可与anti-PEG scFv上His标签结合,进一步增加胶束聚集体的密度,从而在低速离心(≤ 2000 g)条件下即可实现胶束的高效分离。在血浆或血清等生物介质存在下,不同浓度聚合物胶束的分离效率均超过95%。载紫杉醇聚合物胶束体系内存在一定比例的游离药物,且游离药物比例随着胶束浓度下降而上升。
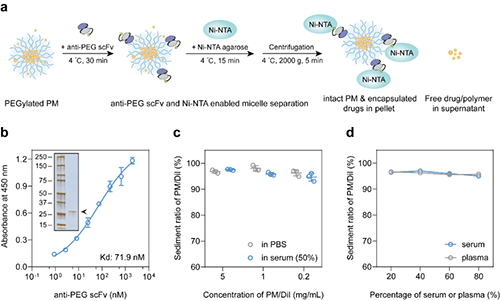
亲和诱捕法揭示mPEG-PDLLA聚合物胶束体内快速释药行为
将亲和诱捕法应用于胶束在SD大鼠和比格犬体内药动学研究,发现聚合物胶束在动物血浆中具有较好的稳定性,在静脉注射后8 h内逐步解体。另一方面,在各时间点的血浆样品中,胶束负载药物紫杉醇的总浓度与经亲和诱捕分离后的游离紫杉醇浓度非常接近,说明胶束负载的绝大部分紫杉醇在注射后发生了迅速释放,而该现象可能与胶束在血液中大量稀释以及泄露的紫杉醇高结合血浆蛋白特性相关。
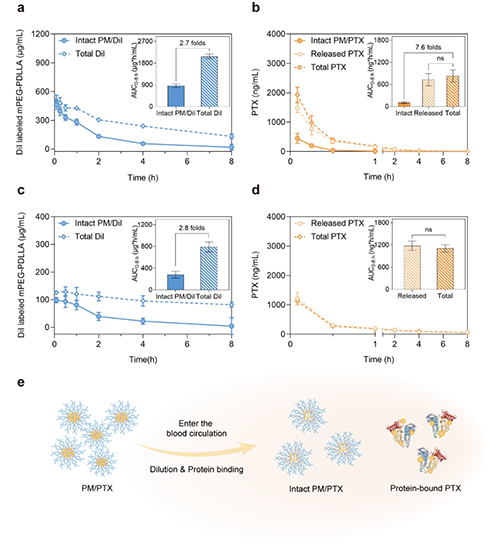
抗PEG抗体诱导聚合物胶束相关的加速清除现象和类过敏效应
长期以来,人们一直认为PEG是一种免疫原性极低的惰性物质。然而越来越多的报道指出,无论是静脉注射PEG化纳米药物,还是通过其它途径接触含PEG的日化用品和食品等,都有可能诱导机体产生特异性抗PEG抗体,这些抗体将与后续注射至机体内的PEG化纳米药物制剂发生结合,诱发一系列不良反应,从而降低药物的疗效和安全性。
目前获批上市或在临床研究阶段的聚合物胶束多数为PEG化胶束,为明晰抗PEG抗体存在下聚合物胶束制剂的安全性和有效性,该研究进一步分析了mPEG-PDLLA聚合物胶束在含有抗PEG抗体的SD大鼠和比格犬体内的药动学行为,发现抗PEG抗体能诱导胶束发生加速血液清除(ABC)现象。相较于SD大鼠,聚合物胶束在比格犬动物模型中的ABC现象更加显著。
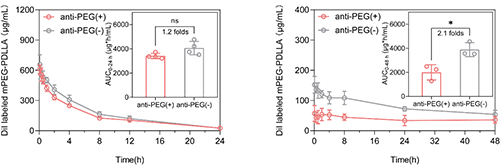
此外,抗PEG抗体与聚合物胶束结合形成的免疫复合物可激活血液补体系统,诱导比格犬发生明显的类过敏反应,主要症状包括瘫倒、呕吐、腹泻、垂涎、结膜充血以及嗜碱性粒细胞占比显著增加等。
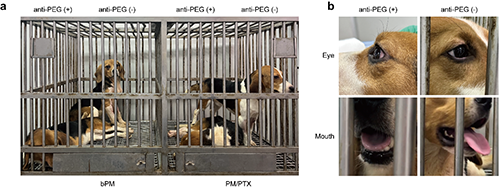
基于anti-PEG scFv的亲和诱捕法首次实现了聚合物胶束的高效分离(分离过程中胶束制剂稳定性不变),为体内外样本中聚合物胶束的分离提供了新技术。通过将方法建立与应用研究相结合,该研究率先发现载紫杉醇聚合物胶束体系内存在一定比例的游离药物,且游离药物比例随着胶束浓度的下降而升高;静注后胶束包封药物在体内可快速释放,而胶束载体本身在体内具有一定的稳定性。此外,多物种体内预存的抗PEG抗体对胶束制剂的体内命运具有显著的调控作用。
原文链接:
Shiqi Lin, Yifei Yu, Ercan Wu, Tianhao Ding, Yuxiu Chu, Feng Pan, Yang, Yang, Changyou Zhan*. Reexamining in vivo fate of paclitaxel -loaded polymeric micelles. Nano Today, 2024, 56: 102255.
https://doi.org/10.1016/j.nantod.2024.102255
- 中国海大何治宇/于良民 Adv. Sci.:基于传统中药冰片的聚合物胶束脑内药物递送系统-用于精确适应病理机制的缺血性脑卒中治疗 2025-01-21
- 国科大屈小中教授课题组 Angew:在高分子-蛋白多层次结构纳米组装体制备和应用研究中取得进展 2024-02-27
- 西工大邵东燕、孔杰等 AHM:基于IL-15共激活的聚合物胶束构建及其在NK细胞免疫治疗中作用机制研究 2023-11-23
- 浙江大学张超研究员/徐志康教授团队 Nat. Commun.:具有三维连通传输通道的纳米纤维交织凝胶膜实现二氧化碳的高效分离 2025-09-04
- 北化秦培勇/司志豪 AFM:基于层间化学共价作用构筑高性能TFC复合膜 2025-02-18
- 南京工业大学孙世鹏教授团队 Nat. Commun.:离子化亚纳米通道膜实现一、二价阴离子高效分离 2024-09-01
- 西南交大周绍兵教授团队《Sci. Adv.》:聚合物囊泡同时引发内质网应激和自噬流阻断,有效抗肿瘤及抑制肿瘤转移 2020-08-05
