在骨科和口腔种植领域,植入物相关感染与骨整合不良始终是亟待突破的两大难题。如何在确保抗菌性能的同时,兼顾成骨活性,并实现涂层的稳定性与通用性,是长期制约该领域发展的“卡脖子”基础科学问题。由于微生物入侵和宿主细胞定植之间存在生物学冲突,导致植入体面临感染风险与骨结合障碍的双重挑战。然而,传统的接触型抗菌涂层往往存在对哺乳动物细胞活性产生负面影响的风险,限制了其临床应用的前景。
针对上述难题,北京化工大学徐福建教授、段顺教授课题组联合首都医科大学附属北京口腔医院孙玉洁副主任医师团队,在前期提出的仿生“胺介导的多酚自聚涂层”策略(J. Am. Chem. Soc. 2025, 147, 20144?20158)基础上,创新性地提出通过调控种植体表面的化学结构,引导细胞与细菌在界面上的竞争性行为,以实现“高效抗菌”与“优良细胞相容性”的协同调控,成功突破了该领域长期存在的性能矛盾。相关研究成果近期发表于Advanced Materials。该论文第一作者为北京化工大学2025届博士毕业生孙美州(石河子大学定向培养师资博士研究生),共同第一作者为首都医科大学附属北京口腔医院博士生徐弛。北京化工大学博士研究生吴若楠、硕士毕业生杨千对于本研究亦有重要贡献,北京化工大学丁小康教授、赵娜娜教授、首都医科大学附属北京口腔医院耿威主任医师也对本论文提供了大力支持。该研究受到国家自然科学基金重大项目的支持。
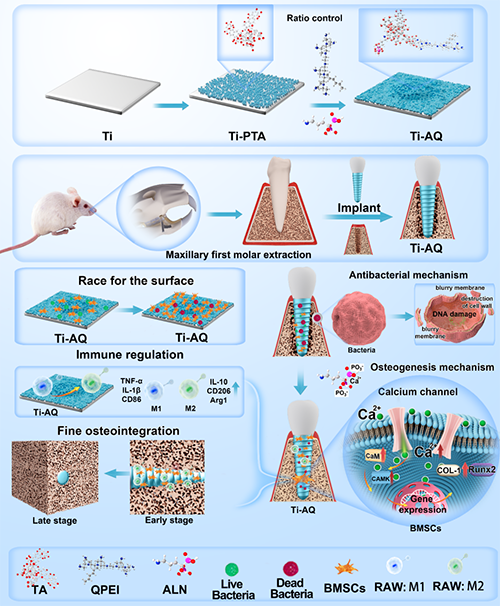
图1 抗菌季铵基团/促骨结合活性磷酸基团调控聚多酚表面性质
本研究提出了一种具有理论原创性与工程适配性的表面化学调控策略,实现了高选择性抗菌与成骨诱导性能的协同兼顾。该策略以“表面竞争”理论为出发点,精准调控植入体表面的化学结构,使其在细菌与宿主细胞竞争性定植的关键窗口期,助力哺乳动物细胞赢得“界面占领权”。
研究中,团队通过便捷的多酚-胺介导共价修饰技术,将季铵基团(Q)与磷酸基团(A)协同引入植入体表面,构建了具备双功能调控能力的Ti-AQ复合涂层。季铵基团作为接触性抗菌结构,可通过电荷作用与膜破坏机制,实现对细菌的快速杀灭;而磷酸基团则可模拟骨外基质中天然的成骨信号,诱导骨髓间充质干细胞(BMSCs)黏附、增殖与成骨分化,且不影响其抗菌性能。重要的是,该研究通过系统调控Q/A比例,获得了性能最优的Ti-AQ-2组涂层,在不释放杀菌剂的条件下,实现了对大肠杆菌和金黄色葡萄球菌超99%的杀灭率,并显著提升成骨相关基因表达和骨形成能力。
在机理层面,研究系统揭示了表面化学结构调控生物界面响应的多层次作用路径:抗菌方面,Ti-AQ-2通过抑制细菌细胞壁合成、干扰其代谢途径、降低ATP水平,破坏其膜结构,实现高效杀菌;成骨方面,涂层通过磷酸基团螯合钙离子,建立局部高钙微环境,进一步通过激活Ca2?通道引发CaM/CAMKII信号通路,驱动BMSCs成骨分化。该机制经转录组学、荧光探针、Western blot等多种技术路径得到系统验证,建立了“磷酸基团—钙离子信号—成骨分化”这一新型表面诱导机制模型。
除此之外,研究还发现Ti-AQ表面可诱导巨噬细胞向修复型M2表型极化,形成有利于骨愈合的免疫微环境,将抗感染-促成骨-免疫调控三者功能统一于同一表面设计中,为构建多功能一体化的新型植入体提供了新范式。在口腔种植体感染动物模型中,Ti-AQ-2在体内亦展现出优异的抗感染能力和骨整合性能,证实其长期生物学稳定性与应用前景。

图2 A)Ti和Ti-AQs表面S. aureus和E. coli后的膜通透染色图。B-C)Ti和Ti-AQs表面S. aureus的转录组学图。D)Ti-AQ-2材料表面细菌的TEM图像和AFM图像。E)Ti-AQ-2表面S. aureus和E. coli的ATP含量。F)Ti和Ti-AQ处理E.coli的抗菌机制图。
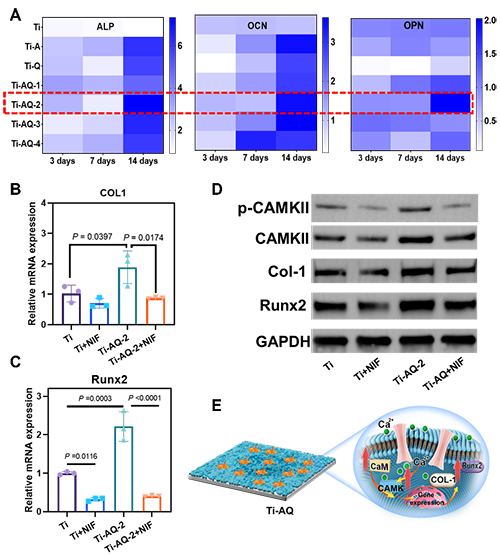
图3 A)在Ti和Ti-AQs表面上培养3天,7天和14天的BMSCs中相关基因表达水平的热图。B-D)钙离子通路抑制剂NIF抑制后BMSCs的成骨基因和相关蛋白表达的Weston blot图像;E)Ti-AQ表面促进成骨作用的机制示意图。
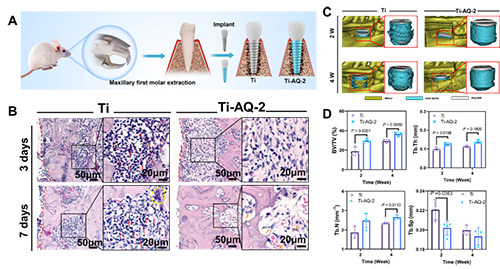
图4 A)感染性口腔种植模型的建立过程。B)Ti和Ti-AQ种植体周围H&E染色图片;C-D)Ti和Ti-AQ-2植入体周围新生骨组织的定性与定量。
总体而言,该研究从基础理论出发,系统构建了“表面化学结构调控—细菌/细胞竞争响应—成骨机制激活”的理论-机制-功能三位一体创新体系,提出了一种可广泛适用于医用金属表面的功能涂层构建策略。该策略以精准表面化学调控为核心,兼顾杀菌选择性、生物相容性与骨整合性能,为未来骨科与口腔植入材料的临床转化提供了重要的理论依据与工程路径。
针对植入材料表面细胞-细菌竞争性定植这一关键科学问题,研究团队系统构建了一类具有抗菌与成骨双重功能的涂层。团队先后提出了仿生“胺介导多酚自聚涂层”策略(J. Am. Chem. Soc. 2025, 147, 20144?20158),发展了同时具备抗菌和促细胞黏附功能的表面活化方法(Adv. Funct. Mater. 2025, 2423639),并进一步在多种基材上验证了该策略的普适性与适配性,包括在纤维膜表面实现抗菌-促成骨功能的协同(Chem. Eng. J. 2024, 490, 1385–8947)。这一系列工作不仅拓展了多酚类分子在生物医用材料表面功能化中的应用,也为植入材料表界面调控机制的深入研究提供了新思路。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202506113
- 北化徐福建/段顺、北京口腔医院孙玉洁团队 JACS: 杀菌/促骨整合仿生多酚涂层的化学结构调控 2025-05-31
- 北化张好斌教授《ACS Nano》:基于化学结构调控策略实现氧化石墨烯自发规整组装 2022-05-27
- 武汉理工赵政教授团队 Int. J. Biol. Macromol.:3D打印压电催化水凝胶用于感染伤口的高效抗菌治疗 2024-05-11
- 四川大学王玉忠/付腾团队 ACS Materials Lett.:高效抗菌防污、高阻燃性乙烯基酯树脂复合材料 2024-01-25
- 广东省科学院生医所郭会龙 ACS Mater. Lett.:高效抗菌抗炎、glucose/ROS双重响应可注射自愈合粘性水凝胶 2023-10-30
