目前,细菌性角膜炎的临床治疗方案涉及局部抗生素滴眼液到缝合式角膜移植,但均难以同时兼顾感染控制、炎症调节与组织再生。为协调高效抗菌与宿主组织保护之间的矛盾,研究人员开发了一种可注射的仿生复合基质,该基质由光响应型胶原/透明质酸-硝基苯偶联物(CHB)水凝胶与源自姜黄素和壳聚糖的多功能碳点(CC-CDs)集成而成。注射后,CHB水凝胶可在原位形成透明且具有粘附性的界面;同时,CC-CDs利用其阳离子壳聚糖组分靶向破坏细菌细胞膜,并发挥姜黄素衍生的纳米酶活性以维持细胞内的氧化还原平衡。值得注意的是,相比于疏水性姜黄素,CC-CDs的水溶性提升了4000倍以上,显著增强了其抗氧化效能,并实现了前所未有的双重效应:在接近完全清除细菌的同时,保持了98%以上的细胞存活率。基于这种优异的生物相容性,该复合水凝胶进一步促进了巨噬细胞向再生型M2表型极化。体内实验结果显示,该材料在24小时内使细菌载量降低了90%,在第4天将抗炎细胞的招募量提升了6倍,并在第28天抑制了91.8%的纤维化标志物,同时恢复了87.5%的视网膜信号幅度。这些研究结果突显了该复合水凝胶通过微创微环境调节,实现无瘢痕结构修复与视觉功能恢复的协同能力,为替代传统眼科手术提供了新策略。
临床上,细菌性角膜炎的治疗正面临着从“治标”向“治本”跨越的瓶颈。现有的治疗策略主要依赖局部频繁滴加抗生素滴眼液,但这往往因药物驻留时间短、生物利用度低而导致感染反复;而对于重症患者,缝合式角膜移植虽能重建眼表,却极易引发手术缝合相关的机械刺激、二次炎症乃至免疫排斥。更为严峻的是,单一的治疗手段往往顾此失彼,强力杀菌可能加剧宿主细胞的氧化损伤,而单纯的物理修复又难以应对复杂的炎症微环境。因此,开发一种能同时兼顾病原体精准清除、炎症状态双向调节与角膜组织原位再生的全效修复体系,已成为眼科再生医学领域亟待突破的课题。
近期,四川大学生物医学工程学院/国家生物医学材料工程技术研究中心孙静/范红松团队针对细菌性角膜炎治疗中病原体滋生与炎症损伤并存的临床挑战,利用水热法将壳聚糖与姜黄素前驱体转化为带正电荷的碳点(CC-CDs),实现了类酶抗氧化活性与靶向抗菌功能的有效整合。研究团队首先通过密度泛函理论(DFT)从分子水平揭示了碳点的催化机理,验证了其非活性氧依赖的选择性抗菌机制,克服了传统抗菌系统易导致宿主细胞无差别损伤的局限性。随后,团队将该具有类酶活性的CC-CDs引入光敏胶原/透明质酸基质中,构建了一种兼具免缝合粘附功能与时空协同治疗效应的复合类酶水凝胶(CHB@CC)。该水凝胶不仅展现出优异的透明度、组织粘附力及活性氧(ROS)清除能力,更能诱导巨噬细胞向抑炎型(M2型)极化。在新西兰兔细菌性角膜炎模型中,该体系实现了创面的即时密封与早期抗炎杀菌,并通过抑制瘢痕生成、引导角膜组织无瘢痕愈合,成功恢复了眼球的光电信号转化功能。这项研究为构建安全、高效的新型抗菌纳米医药系统提供了理论依据,也为角膜损伤后的微环境调控与功能再生提供了新的临床转化思路。
2026年2月14日,相关研究成果以“Enzyme-Mimetic Hydrogel Balancing Antibacterial Activity and Cytoprotection for Corneal Regeneration in Bacterial Keratitis”为题发表在知名学术期刊《ACS Nano》上。四川大学生物医学工程学院/国家生物医学材料工程技术研究中心吴凯博士为文章第一作者。该研究得到了国家自然科学基金委的支持。
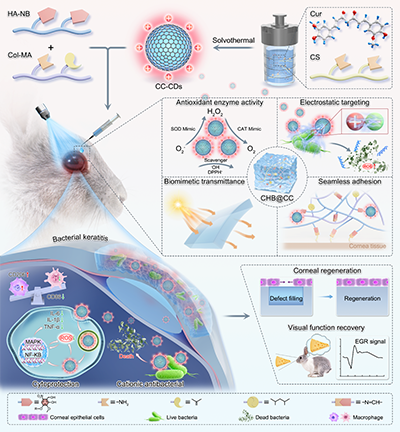
图1 多功能CHB@CC水凝胶治疗细菌性角膜炎的示意图,强调了其在杀灭细菌、调节炎症及促进角膜组织修复方面的协同作用,从而实现高效的再生治疗。
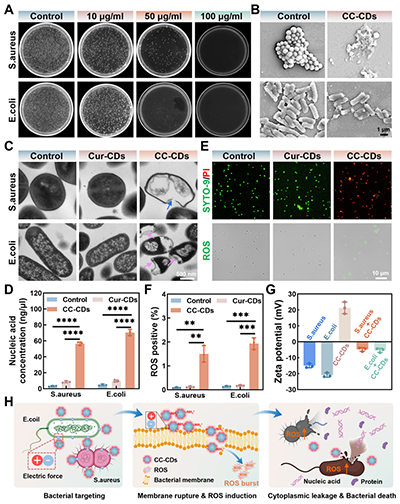
图2 CC-CDs的体外抗菌性能评价及机理研究。
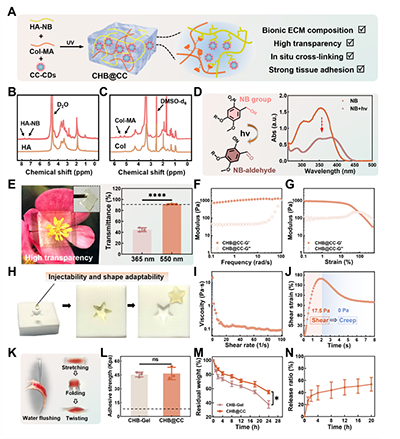
图3 光敏粘附型CHB@CC水凝胶的制备与表征。
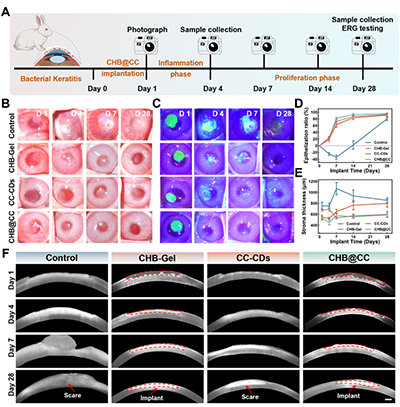
图4 CHB@CC水凝胶在金黄色葡萄球菌感染的角膜缺损模型中的体内治疗评价。
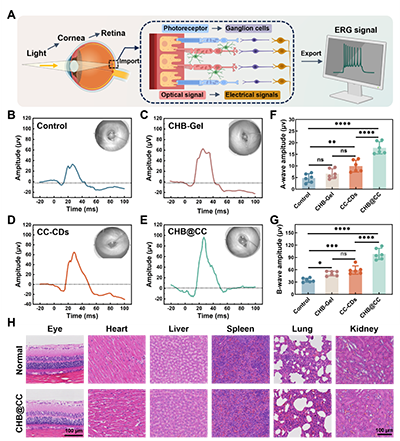
图5通过视网膜电图(ERG)评估视网膜光-电信号转导功能,侧面反映角膜损伤修复情况。
该工作是团队近期在仿生基质设计治疗眼表疾病领域的系列进展之一。针对复杂的眼科病理环境,该团队立足于组织再生医学,以胶原蛋白、羊膜等天然生物基质为核心,通过分子水平的功能化修饰与仿生结构构建,开发了一系列具备高度生物相容性与微环境调控能力的诱导性修复材料。近两年来,团队构建了全方位的眼科治疗矩阵:首先,以胶原蛋白为基石,研制出具有仿生层状结构、高透光率及优异力学性能的人工角膜替代物,为缓解临床供体匮乏提供了新路径(Small 2024);针对传统缝合并发症及单一基质功能局限,团队开发了集原位粘附、抗菌、抗氧化于一体的复合水凝胶,实现了细菌性角膜炎的高效治疗(ACS Nano 2026);此外,通过在羊膜基质中整合多酶活性锰基碳点,有效抑制了角膜碱烧伤后的新生血管与瘢痕形成(Acta Biomaterialia 2025)。在眼底疾病领域,团队构建了胶原/环糊精可注射递送系统,实现了美法仑与溶瘤病毒的协同递送,为视网膜母细胞瘤的治疗提供了新策略(Acta Pharmaceutica Sinica B 2025)。目前,该团队正积极探索材料功能化在视神经损伤修复中的前沿应用,致力于打造覆盖眼表至眼底的全域治疗体系。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c22118
- 陕科大王学川教授/党旭岗副教授 JCIS:具有增强抗菌活性和防腐性能的多功能玉米淀粉基可持续食品包装 2025-04-27
- 康涅狄格大学罗阳超团队 Adv. Compos. Hybrid Mater.:壳聚糖基双网络水凝胶的构建与特性及其强抗菌活性 2023-11-11
- 浙江大学朱蔚璞教授团队 AM:高耐热咪唑盐抗菌剂用于PET废料的升级回收利用 2023-04-30
- 内大董阿力德尔图教授、吉大杨英威教授 ACS Nano:基于自诱导肽信号的伪装技术治疗细菌性角膜炎 2025-09-17
- 浙大王征科课题组《Adv. Sci.》综述:生物材料在角膜再生中的应用 2025-01-02
