胞外靶向蛋白降解(extracellular targeted protein degradation, eTPD)作为近年来发展迅速的一类新型药物策略,通过双功能嵌合体将目标蛋白募集至细胞膜受体并诱导内吞,进而递送至溶酶体实现降解,已发展出LYTACs、AbTACs、KineTACs和TransTACs等多种体系。然而,这类体系通常依赖抗体或其衍生物进行构建,往往需要复杂的化学修饰或蛋白工程改造,且由于分子尺寸较大,在实体瘤中的组织渗透能力有限;相比之下,小分子体系虽具备更好的渗透性,但存在体内清除较快以及靶点范围受限等问题。因此,开发兼具高效降解能力与深部组织穿透能力的eTPD平台具有重要意义。
针对上述问题,浙江大学邵世群研究员联合浙江省人民医院陈玉平研究员,发展了一种CD44受体介导的转胞运触发型蛋白降解嵌合体CATCH。该体系基于透明质酸-聚赖氨酸纳米颗粒构建,并引入IgG亲和肽,实现对未经修饰抗体的“即插即用”组装,从而可快速构建针对不同靶点的蛋白降解体系。CATCH通过CD44介导的内吞与转胞运过程实现对目标蛋白的高效清除,既可将靶蛋白递送至溶酶体降解,又可通过跨胞转运实现蛋白外排,形成“降解+外排”的协同机制;同时,其连续转胞运能力使其能够逐层渗透实体瘤深部并实现蛋白清除。
2026年3月5日,该工作以“CD44-Assisted Transcytosable Chimeras for Extracellular Protein Depletion in Deep Tumors”为题,发表在Angewandte Chemie International Edition期刊上。浙江大学许馨露(硕士生)、谢静雯(博士生)和浙江省人民医院助理研究员司晶星为该论文的共同第一作者。
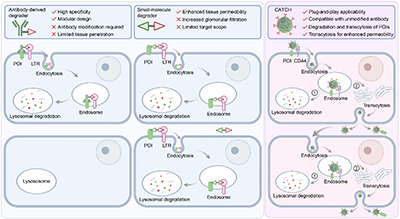
CATCH的设计原理及作用机制示意图。
研究首先构建了透明质酸-聚赖氨酸纳米颗粒(HA-PLL NP)作为CATCH的核心载体。结果表明,该纳米体系可通过CD44受体介导实现高效内吞,并在细胞内进入溶酶体、内质网及高尔基体等多种细胞器通路:一部分被递送至溶酶体参与降解过程,另一部分则经内质网-高尔基体途径参与转胞运(图1),为后续实现深部组织渗透奠定了基础。
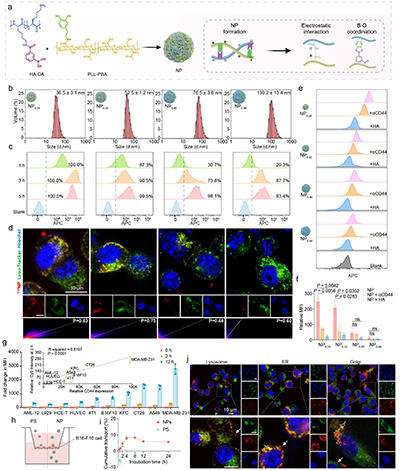
图1 HA-PLL纳米颗粒的构建、CD44介导内吞及转胞运特性。
在纳米平台基础上,研究引入IgG亲和肽Fc-III-4C,实现对天然抗体的高效加载,构建出无需改造抗体的“即插即用”式CATCH体系。实验表明,抗体修饰后的纳米颗粒可显著促进目标蛋白的内吞(提升超过10倍以上),且该过程依赖CD44介导(图2)。这一结果验证了CATCH在构建便捷性与功能实现上的双重优势。
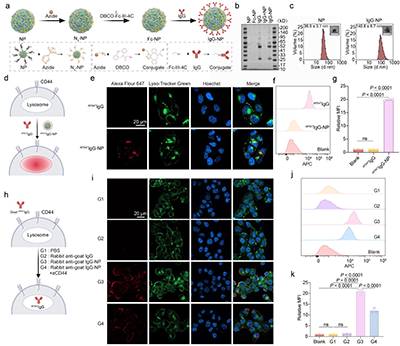
图2 CATCH模块化构建与“即插即用”特性。
CATCH体系展现出优异的蛋白降解能力:在低纳摩尔浓度下,仅需约3小时即可实现细胞表面蛋白(如PD-L1)的近乎完全清除,同时对HER2等不同靶点同样有效。进一步研究表明,该过程依赖CD44介导的溶酶体降解途径(图3),且降解效率显著优于现有eTPD体系,体现出快速、高效、广谱的特点。
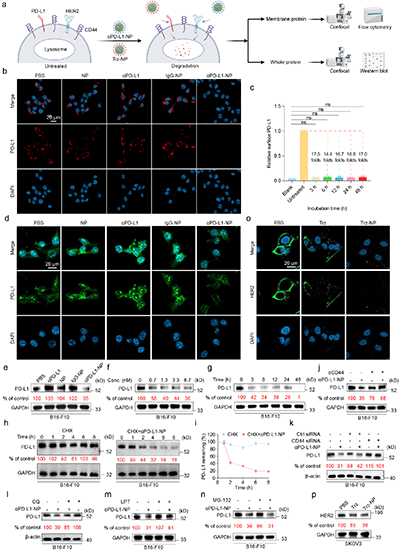
图3 高效清除膜蛋白(PD-L1 / HER2)。
机制研究发现,CATCH不仅通过溶酶体降解蛋白,还可通过转胞运将靶蛋白转运至细胞外,实现“降解+外排”的双机制协同作用。更重要的是,CATCH可在细胞间连续转运,并在三维肿瘤球模型中实现对深部区域蛋白的有效清除,明显优于单独抗体处理(图4)。这一结果证明其具备突破实体瘤渗透屏障的能力。
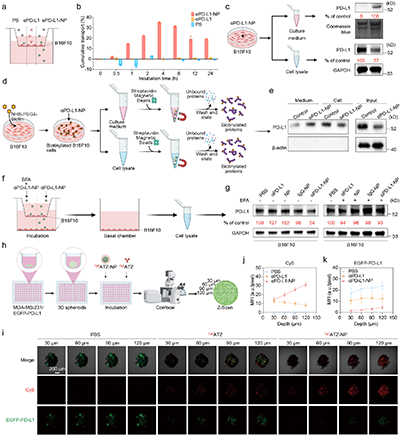
图4 转胞运驱动深部肿瘤蛋白清除。
在小鼠黑色素瘤模型中,CATCH显著抑制肿瘤生长,并有效降低肿瘤组织中PD-L1水平。免疫分析显示,该体系可增强CD8? T细胞浸润并提升其杀伤活性,同时未观察到明显毒性,体现出良好的体内安全性(图5)。该结果表明,CATCH不仅能够实现深部蛋白清除,还可激活抗肿瘤免疫反应,展现出良好的治疗潜力。
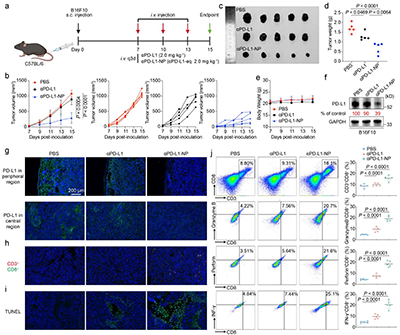
图5 体内抗肿瘤效果与免疫激活。
该研究首次将转胞运机制引入胞外蛋白降解领域,实现了对肿瘤深部区域蛋白的高效清除,为实体瘤治疗提供了新的策略和思路。本研究得到了国家自然科学基金、国家重点研发计划、国家科技重大专项及浙江省自然科学基金等项目的支持。
原文链接:https://onlinelibrary.wiley.com/doi/epdf/10.1002/anie.202521770
- 北化王兴教授团队《Adv. Mater.》:具有级联靶向功能的聚氨基酸基纳米粒子通过原位递送抗菌剂高效清除胞内菌 2022-02-17
- 合肥工业大学:新型复合材料可高效清除持久性水污染物 2016-06-12
