近年来,干细胞疗法在多种疑难疾病的治疗中大放异彩,但其临床应用仍受到免疫排斥、致瘤性等安全隐患的限制。作为干细胞的“衍生产物”,小细胞外囊泡(Small extracellular vesicles, sEV)富含蛋白质、核酸和脂质等活性成分,这些具备治疗特性的生物分子递送给受体细胞,可以有效地改变它们的生物反应,在许多疾病的治疗和医疗美容领域都显示出巨大的潜力。相较于直接使用干细胞,sEV通过低免疫原性和免疫调节功能避免免疫排斥,又因无增殖能力而降低了致瘤风险,安全性更高。因sEV具备干细胞的治疗效果,同时规避了干细胞治疗的固有局限性,从而成为了干细胞治疗的安全替代方案。但通常情况下干细胞sEV的产量极低,传统增产手段依赖昂贵药物或复杂设备,导致其治疗成本高昂,限制了临床推广。
近日,中国科学技术大学张青川团队在Nano Letters杂志上发表题为“High Efficiency Production of Functional Small Extracellular Vesicles through Cellular Self-Motivation”,提出利用细胞自身产生的牵引力与特定生物智能软材料的力电转换效应,可实现无需外部刺激的sEV分泌增强。中国科学技术大学博士研究生王晨为第一作者,张青川教授、吴尚犬教授以及安徽医科大学陈旭林教授为共同通讯作者。该研究得到了国家自然科学基金和国家重大科技专项的资助。
研究团队关注到,贴壁细胞在生长过程中会持续对其附着的基底施加周期性的牵引力。由此,研究者提出“细胞自我刺激(Cellular self-stimulation)”的新概念,借助一种具有压电特性,且刚度接近细胞外微环境的柔性水凝胶,通过细胞自身行为驱动sEV高效分泌。当细胞在压电水凝胶材料表面粘附生长时,细胞自然产生的微小牵引力(~10 nN)即可引发水凝胶结构形变,触发阳离子定向迁移并形成局部电场,这些电信号再反过来刺激细胞自身,使sEV分泌数量实现量级上的提升。
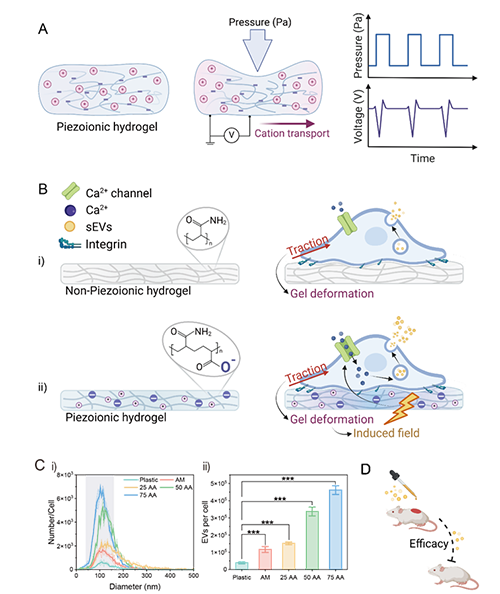
图1. (A) 实现力-电转换的柔性压电水凝胶; (B, C) 牵引力触发的“细胞自我激励”提升sEV产量; (D) 获得的sEV具备出色治疗效果.
与传统依赖外部刺激手段不同,该策略让细胞“自主开启生命开关”,无须昂贵药物或大型设备,具备更高的经济性与适用性。所获得的sEV已在体内外实验中被证实具备出色的治疗效果,有望在炎症治疗、组织修复、再生医学乃至医疗美容领域,作为药物递送载体和细胞修复工具展现出广阔应用前景。同时,这种以生物亲和性压电柔性材料为基础的“自激励”策略,也为无创植入材料与细胞环境调控提供了全新的思路。
参考文献
Wang, C.; Zhao, X.; Yan, T.; et al. High Efficiency Production of Functional Small Extracellular Vesicles through Cellular Self-Motivation. Nano Letters 2025, 25 (16), 6471-6480.
https://doi.org/10.1021/acs.nanolett.5c00094.
