自3D 生物打印首次被报道后,该领域得到迅速发展。相较于传统的组织工程,3D生物打印具有能够制造特定结构的优势,是有望能转化进入临床应用的生物制造方法。然而截至目前很少有真正进入临床试验的研究,究其原因在于研究3D生物打印的科学家和临床医生所关注的点不同,导致无法实现标准统一。如何跨越这道鸿沟,步入临床应用的通途是3D生物打印领域接下来面临的挑战。作为生物打印的主体,生物墨水的角色尤其重要。3D生物打印的临床转化与新一代的生物墨水的开发密不可分。对此,弗莱堡大学高分子研究所的Shastrilab对目前3D生物打印技术(挤压成型式)进行了总结并提出生物墨水开发的五个阶段(TRL1-5),生物墨水需要具备的特性和标准化的工具,以期对未来研究3D生物打印的研究者提供一些参考(图1)。

图1 生物墨水开发的五个阶段以及各阶段涉及到的标准化工具
此前有学者将生物墨水定义为“能够适用于自动化制造和成型的包含细胞的配方,可包含生物活性成分和生物材料”。这一定义强调了细胞在生物墨水中的重要性。然而在真实的打印中,生物材料本身的作用不可忽视。在构建复杂结构的例子中,细胞的打印几乎离不开生物材料的支撑。生物材料不仅扮演了传递细胞的作用,其本身对细胞和其他生物活性物质的影响更是不容小觑。早在本世纪初年就有学者提出生物材料的指引作用,其给内含细胞提供了机械力、物理、化学和生物信号。因此本文将生物墨水中的介质(生物材料)比喻为空白的画布,通过后期的控制和改性具有特定的生物学功能和理化特性,比如引入特殊的基团控制其交联机制,调控内部原有基团的比例而操控硬度,或者接枝生物小分子使其具备特定的生物功能。
3D生物打印的临床转化可以借鉴组织工程的发展历程,因为二者具有很多相似性。比如二者都涉及生物材料和细胞的应用,都可应用于组织的修复或替代。目前,组织工程领域已经有产品进入临床应用,但数量不多,其原因也在于当时组织工程在快速发展后并没有迅速设想到后期应用的涉及的问题,以至于在后期转化中出现标准化较慢的阶段。所幸3D生物打印和除组织工程以外其他的一些领域都有交集,比如3D打印,基因和细胞治疗(图2)。这三个领域目前都有用于临床的产品,也有相应的管理条例和标准化规则,可以作为未来3D生物打印的转化的借鉴。作为产品开发前端的科学家,一方面需要了解领域内相关的标准和规定,让研发对象从“学术可接受”转化为“临床可接受”,另一方面需要确保研发的内容能够在满足科学和临床规范的条件下顺利进入转化的生产线。
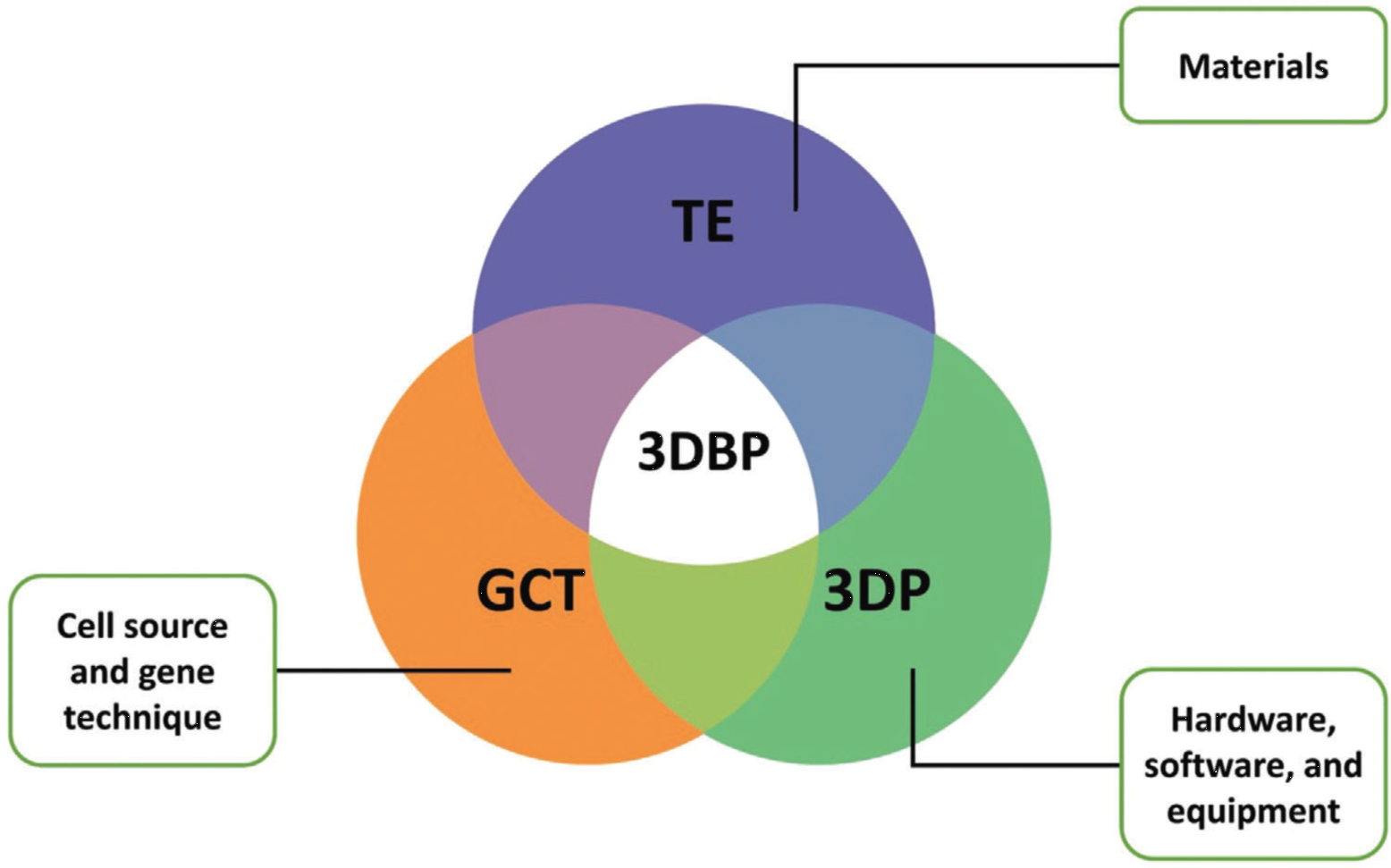
图2 3D生物打印与其他已经有进入临床应用的技术(组织工程,3D打印以及基因和细胞治疗)的交集
生物打印的结构转化为存活的组织,需要具备以下特点:在体外培养时保持其结构稳定,能够适应手术移植过程中的各种操作,在相应的移植部位存活足够的时间。这些特征可总结为“3P特征”,即可预测的物理特性(predictable physical properties),可预测的生物反应(predictable biological response)和可预测的体内结果(and predictable in vivo outcomes)。为此,生物墨水不仅需要具有适合打印的理化性能,还需要具备促使组织再生的特性,能够确保打印的结构稳定且能够再移植后仍然保持活性和特定的生物功能,并且最终能够转化为具有功能的体内组织。
在生物制造过程中,生物墨水首先需要满足一定的温度特性。由于生物打印大多涉及打印细胞和生物活性分子,这些内容对温度要求比较苛刻。通常认为最优的打印温度为人类生理温度。一般过高的温度不作推荐,原因在于高于生理温度的条件下会引起细胞活动的异常,如细胞内钙和钠离子的升高,线粒体膜电位的升高,或活性氧簇水平的升高,这些都会导致细胞损伤或细胞死亡。在40℃时,细胞核可能发生变化;而更高的温度(41℃)则可能在数分钟内直接导致细胞的死亡。低于生理温度的打印此前也有报道,但该温度不能过低,因为过低的温度也会导致细胞冻伤和裂解。因此,推荐的打印温度应该介于室温(细胞培养操作时的温度)与生理温度之间。
另外生物墨水还要达到医疗使用级别,这意味生物墨水需要无菌且没有病原体。因此在材料的选择上和化学制备中需要建立执行标准。材料本身是否含有病原体,化学合成的副产物和分解产物的水平都需要进行规定和测量。在一些聚合物反应中,如果有较多的单体或未反应的催化剂的遗留,势必对细胞产生毒性。如何对生物墨水灭菌则是另一个难点。目前FDA批准的标准灭菌方法为0.22μm滤器过滤灭菌,高温高压灭菌和环氧乙烷灭菌。此前已有报道对这些方法进行了比较,其结果显示高温高压灭菌会破坏聚合物的化学结构,可能引起其性能的改变。而0.22μm滤器过滤只适合于粘度较低的液体,因此应用有限。环氧乙烷可能是更安全而不引起物质特性改变的方法。
打印本身可以分解为三个过程:1.生物墨水从口径较小的管道中挤压出;2.瞬时的结构稳定;3.长期的结构稳定。因此要满足3D生物打印的制造要求,生物墨水还需要具有剪切变稀,可控的胶化,对结构的保真度和高稳定度以实现上诉三个过程的顺畅连接。文中以表格形式列举了近五年来3D生物打印领域的研究成果,罗列了打印所用的材料,打印的结构,是否为无支撑打印,采用的交联方式等。
生物墨水不仅要满足制造的需求,也需要满足生物性能的需求,从而达到组织再生。在组织再生过程中,免疫调控和血管化至关重要。现有证据表明,固有免疫和获得性免疫都在组织再生的过程中有重要的作用。例如在固有免疫中巨噬细胞的极化是免疫调控的重要过程,通常M1型巨噬细胞提供了炎症前的重要信息,而M2型巨噬细胞则与修复和再生有关。此外,组织再生还涉及调控型T细胞,其分泌的白介素参与到与再生相关的免疫抑制活动中。实现器官型的血管化则是组织再生的另一难点。而血管化本身也和免疫调控藕连。如何实现二者的平衡以维持组织稳态是未来面临的挑战(图3)。

图3 生物修复过程所涉及的免疫调控
因此选择合适的生物墨水的材料实现多种需求尤为关键。一直以来生物活性材料被认为良好的选择,因为它们具有更接近正常组织的成分,有较好的细胞亲和力。但活性材料也存在一些劣势,例如较差的可加工性,更有可能引起不良的排异和免疫反应,无法控制的降解速率等等。而生物惰性材料由于不具备细胞粘附性和降解速度慢一直门可罗雀。实际上,生物惰性材料的优势在于来源充足,获取廉价,可成型性好以及可修饰。文中列举了本实验室研发的羧基化琼脂糖生物材料,该材料不仅可以通过羧基化程度来调控成胶的硬度,还能接枝如RGD的小分子来提高细胞粘附力,并且体内实验证明该材料能稳定存在,未引起强烈的免疫反应,同时允许宿主细胞的进入。
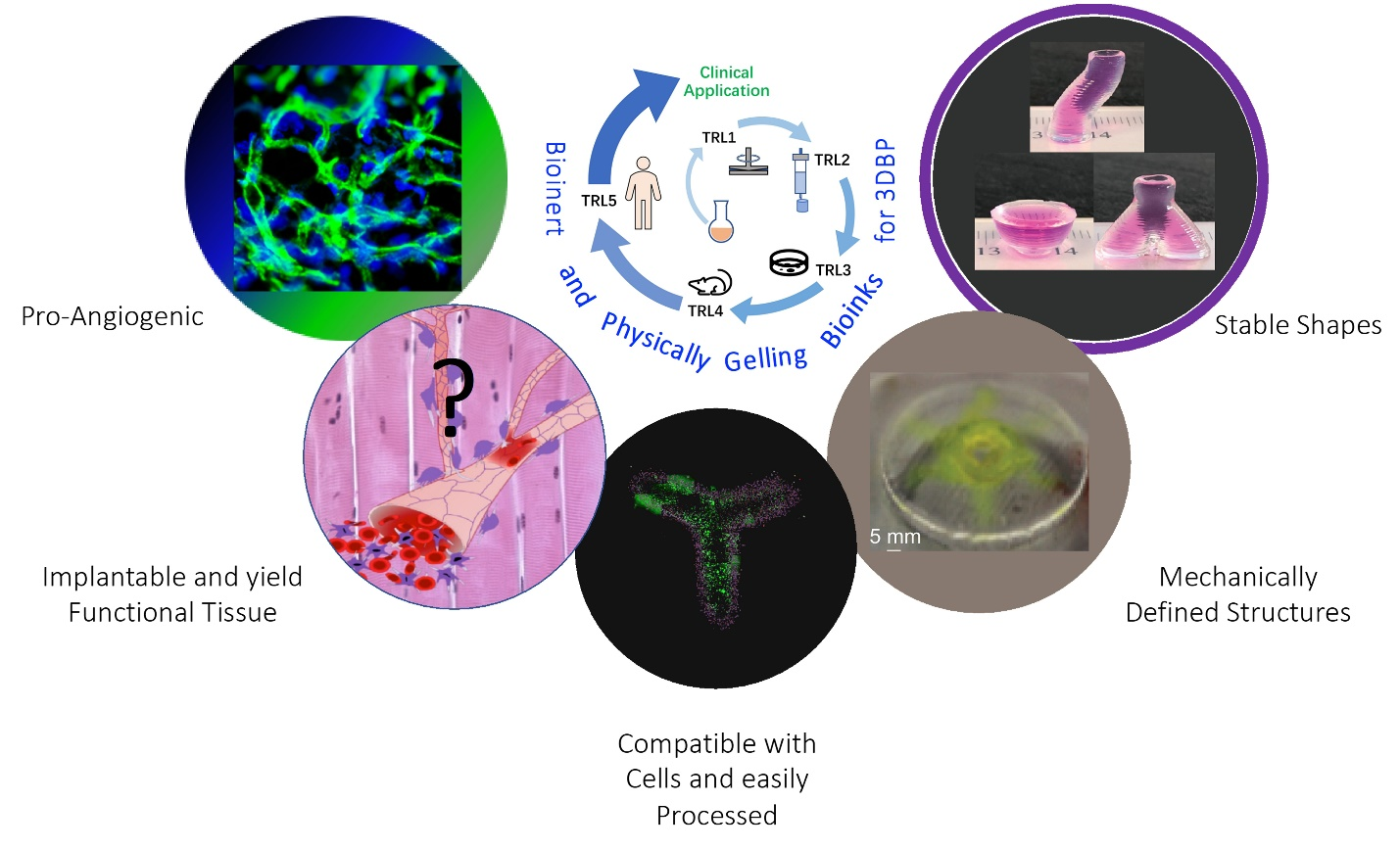
图4 以羧基化琼脂糖为例的生物惰性材料的开发过程
针对上述提出的生物墨水需满足的特性,文章最后提出三种开发性工具套件用于各阶段研究的标准化。它们分别是流变学检测,交联策略(TRL1-2)和可用于体内外研究的生物技术(TRL3-4)。流变学检测可以提供充分的证据以支持生物墨水具有良好的可打印性能。这些检测应当在确定了灭菌方法后进行以确保获得的数据为灭菌后材料的特性,同时这些检测的设计应尽可能模拟打印的条件而能真实反映生物墨水在加工过程中经历的变化。不仅如此,已有研究发现细胞的占比对生物墨水的流变学性能有影响。大量的细胞占会阻碍分子的交联,改变成胶的硬度。在涉及高浓度细胞打印的研究中,对含有细胞的生物墨水进行检测不可或缺。选用交联机制并制定最优交联策略不仅能减少打印过程对细胞的损害,还能提高产能。随着新的聚合物的研发,打印硬件的升级以及高效的交联剂的应用,交联过程并非一成不变。实时交联,多重交联机制的联合应用都能让交联变得高效而副作用降低。最后,打印的结构能形成具有特定功能的组织还有待于体外培养和体内培育的结果。在过往的很多研究中,3D生物打印的生物实验往往浮于表面,真正能推进3D生物打印前进的是更加严格和系统的生物实验。被打印的细胞能否维持其表型,能否分化成成熟的组织都需要更深入的研究。已经有越来越多的研究表明细胞可以通过精密的力学传导器感受外部环境的力学变化从而引起细胞核内的变化。打印过程和生物材料的机械性能都能对细胞产生影响,这些影响是否会改变细胞功能的表达有待揭示。事实上很多实验方法在生物医学上的应用已经很成熟,而在3D生物打印中则并不多见;此外随着表观遗传学和高通量测序的普及,这些检测手段也变得更容易。在未来的研究中,这些研究方法都是3D生物打印的结构能进一步发展的重要基石。
弗莱堡大学博士研究生顾亚伟为本文第一作者,弗莱堡大学讲师Aurelien Forget博士为第二作者,Prasad Shastri教授为本文通讯作者。
作者团队简介:
Prasad Shastri教授目前就职于德国弗莱堡大学高分子研究所,兼弗莱堡大学生物信号研究中心教授。Shastri教授1995年在伦斯勒理工学院获博士学位,随后在Robert Langer教授实验室做博士后研究。此后长期致力于材料科学、修复医学和肿瘤生物学的研究。目前实验室的工作重心为生物材料调控细胞微环境,体内组织工程修复,肿瘤生物学,细胞治疗和纳米生物材料。
原文链接:https://doi.org/10.1002/advs.202103469
- 东华大学史向阳教授团队 Bioact. Mater.:全活性含磷树冠大分子纳米药物通过多靶点免疫调控与神经保护缓解缺血性脑卒中 2026-04-10
- 山东大学崔基炜教授团队 AFM:复合水凝胶通过免疫调控促进骨质疏松性骨折修复 2025-11-14
- 空军军医大学牛丽娜教授团队 ACHM:仿生结构协同免疫调控的DNA-胶原敷料实现烧伤无瘢痕再生? 2025-08-19
- 东华大学何创龙教授团队《Adv. Funct. Mater.》:3D生物打印支架重塑神经调节微环境促进骨再生 2023-06-02
- 哈佛医学院Y. Shrike Zhang课题组 PNAS:双水相嵌入(生物)打印构建无海藻酸、独立、可灌注的超细和超薄壁管状结构 2023-02-07
- 东华大学何创龙教授团队《Carbohyd. Polym.》:3D生物打印双交联网络的明胶/吉兰糖胶基支架用于血管化骨再生 2022-07-12
