通过胞内多肽自组装,以阻断微管抑制细胞增殖、限供能量促进细胞凋亡的方式,来有效治疗耐药肿瘤。这种双管齐下的“非药物疗法”为临床晚期肿瘤和耐药性肿瘤的治疗提供了新思路。3月31日,同济大学材料科学与工程学院杜建忠/范震团队的这一研究成果以“Intracellular Self-Assembly of Peptides to Induce Apoptosis against Drug-Resistant Melanoma”为题,作为增选封面(Supplementary Cover)发表于国际顶级期刊《美国化学会志》(Journal of the American Chemical Society)。
化疗是治疗肿瘤的主要方法之一,但也容易诱发肿瘤耐药性,从而导致“无药可治”。因此,开展针对耐药肿瘤的“非药物疗法”研究具有重要的临床价值和社会意义。
微管是由微管蛋白构成的一种重要的细胞骨架,在动物细胞有丝分裂DNA合成后期(G2期)参与中心体的形成。在肿瘤细胞分裂间期(M期),中心体会引导细胞分裂,即意味着肿瘤扩增。因此,抑制微管的形成就可能抑制肿瘤扩增。另外,线粒体作为细胞能量代谢的主要场所,不仅影响细胞分裂,其功能紊乱时还会诱导细胞凋亡,继而抑制耐药肿瘤。
目前,主要采用化疗药来抑制微管的形成并干扰线粒体功能。然而,患者难以承受反复、长期使用化疗药而导致的高系统性毒性。由此产生了一个具有挑战性的科学问题:如何通过“非药物疗法”来抑制肿瘤细胞中微管的形成并导致线粒体功能紊乱,“双管齐下”治疗耐药肿瘤?
针对该问题,研究团队设想,是否可以合成一种无毒的短肽,使其在细胞内自组装形成纳米颗粒,以干扰微管蛋白聚合的方式调控细胞周期(G2/M)并干扰线粒体功能,进而治疗耐药肿瘤?
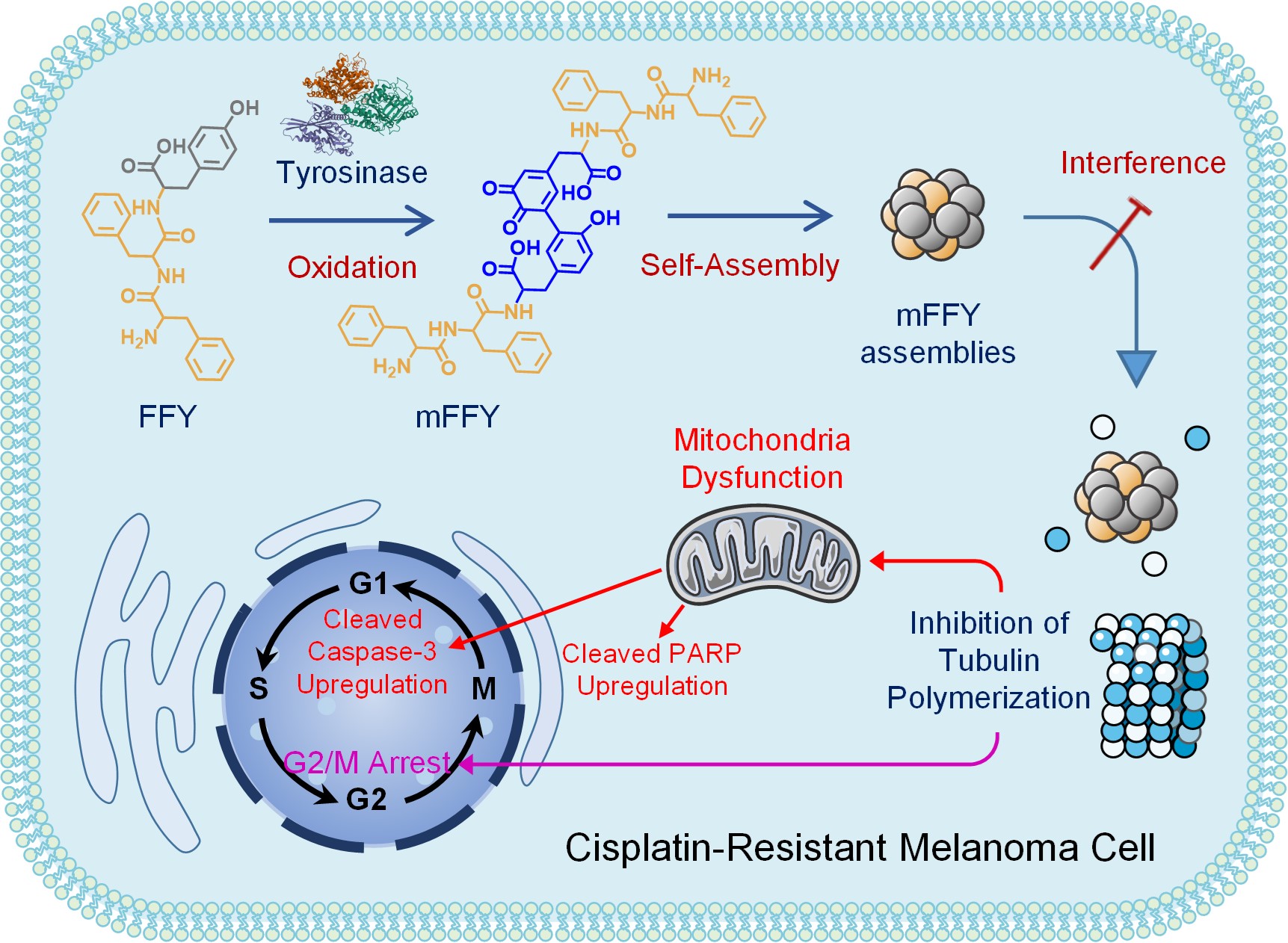
图1. “非药物疗法”:阻断微管抑增殖,限供能量促凋亡。多肽胞内酶促自组装诱导G2/M期阻滞和线粒体功能紊乱,实现黑色素瘤耐药性的逆转。
团队提出了“阻断微管抑增殖,限供能量促凋亡”的“非药物疗法”,并以耐药黑色素瘤为肿瘤模型开展了研究。
研究人员向耐药黑色素瘤细胞中引入三肽(FFY),三肽在细胞内通过酶促自组装形成了mFFY纳米颗粒。
研究发现,将mFFY纳米颗粒与微管蛋白共孵育后,该纳米颗粒有效抑制了微管蛋白聚合。
如图2所示,在经过“非药物疗法”治疗后,由于微管蛋白不能聚合成微管,导致大多数肿瘤细胞停滞于DNA合成后期或分裂间期(即G2/M阻滞),从而抑制肿瘤细胞增殖。同时,线粒体功能紊乱也诱导了凋亡因子的过表达,如cleaved caspase 3(相比对照组提高3.1倍)和cleaved PARP(提高6.3倍),这进一步促进了耐药肿瘤细胞凋亡,最终实现了肿瘤耐药性逆转。
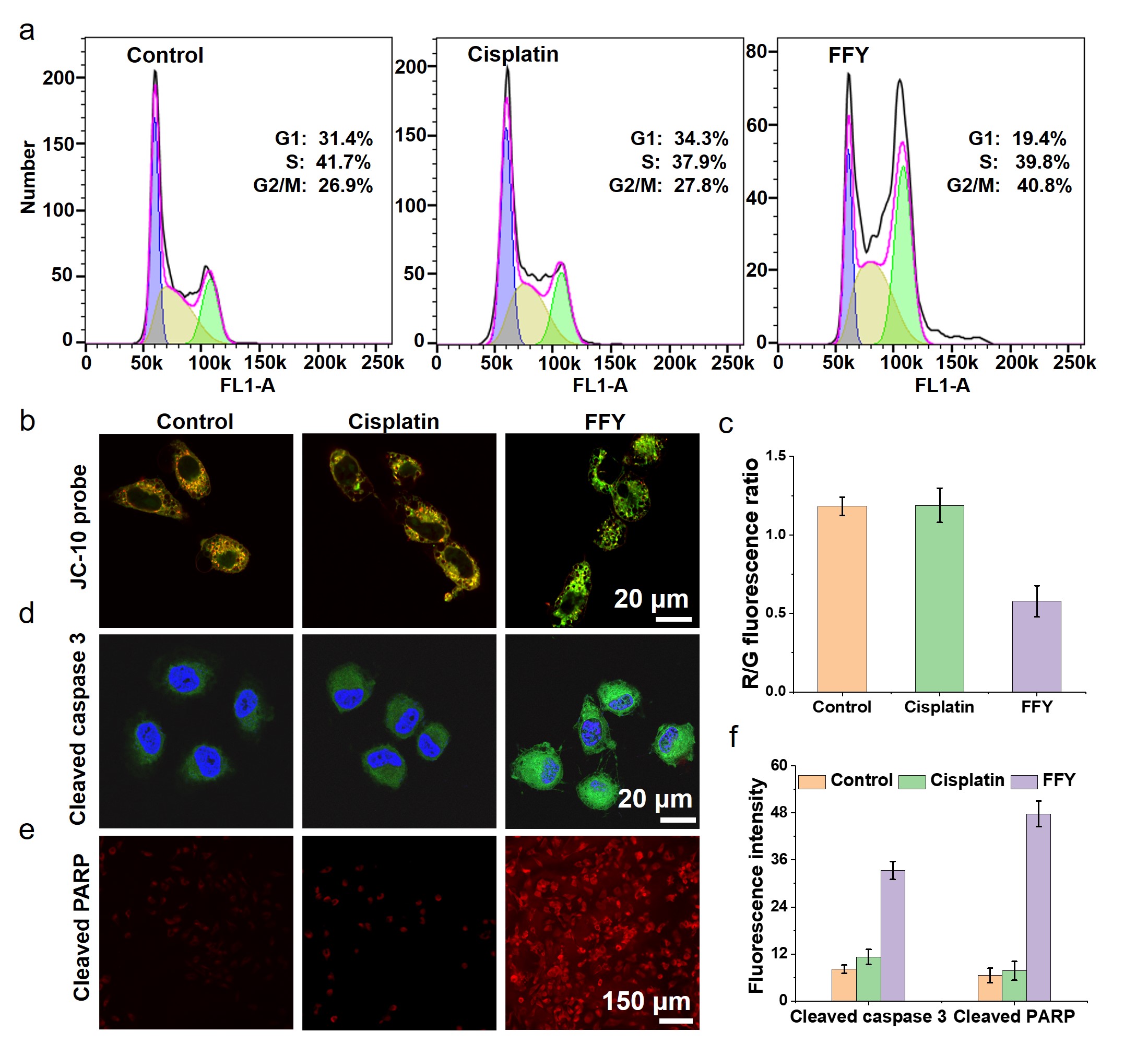
图2. 酶诱导FFY逆转黑色素瘤耐药性的机制研究。
体内实验也证明了“非药物疗法”可有效逆转肿瘤耐药性。动物实验表明,在黑色素瘤周注射FFY后,观察到高水平耐药肿瘤抑制,即在两次治疗后肿瘤体积相比对照组减少了87.4%(如图3所示)。同时,与化疗药物治疗组相比,“非药物疗法”能有效减少或避免系统毒性。
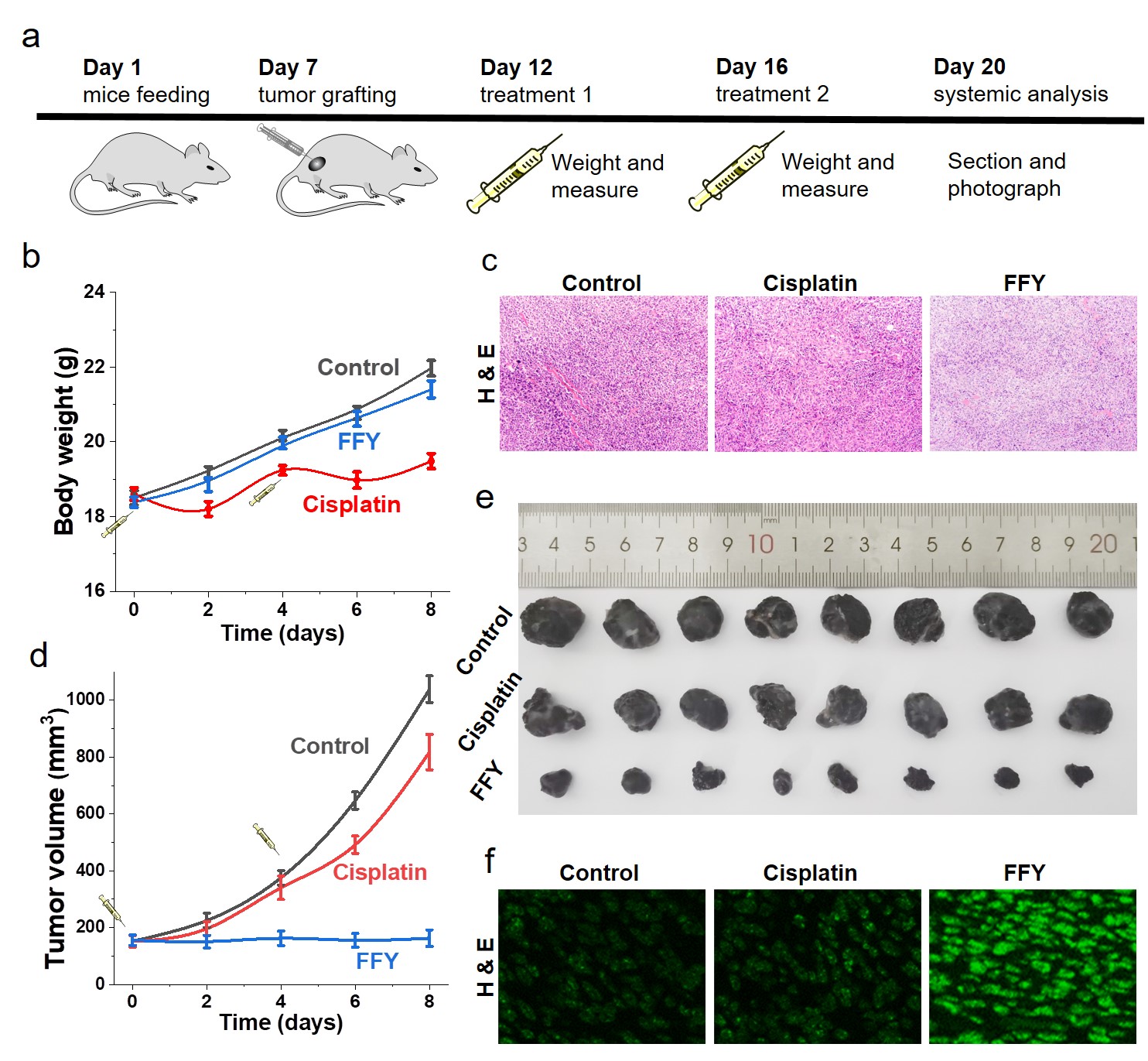
图3. “非药物疗法”对耐药性黑色素实体瘤的抑制效果。
同济大学高分子材料系博士生孙敏为论文的第一作者,杜建忠教授和范震研究员为共同通讯作者。该研究得到了国家杰出青年科学基金、国家自然科学基金面上项目等资助。
论文链接:https://pubs.acs.org/doi/abs/10.1021/jacs.2c00697
- 王育才/刘庄/蒋为 JACS:发展聚合物–脂质载体通过配方优化建立mRNA器官选择性递送的定量预测模型 2026-03-03
- 昆士兰大学乔瑞瑞教授团队 AFM:液态金属纳米颗粒赋能高分辨水凝胶3D打印 2025-12-01
- 北化许海军教授团队 CEJ: 低成本原位光催化技术突破摩擦纳米发电机高性能电极瓶颈 →在疏水性聚合物表面原位生长银纳米颗粒电极 2025-08-07
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 西安交大吴道澄团队 ACS Nano:分子堆砌@无限配位聚合物复合纳米粒实现肿瘤连续高强度光热-热动力交替循环治疗和化疗 2025-08-01
- 巴黎高科化学学院李敏慧教授与合作者 JACS: 创新型“类酶”纳米材料 → 饿死癌细胞 2025-07-20
- 中国科大发现特殊短肽 可降低癌症诊疗毒副作用 2012-10-15
