胶质母细胞瘤(GBM)是最具侵袭性的中枢神经系统恶性肿瘤之一。即便在最大安全范围手术切除后,残留的浸润性肿瘤细胞和高度免疫抑制的微环境仍导致几乎必然的复发,患者中位生存期不足15个月。术后手术腔局部给药策略虽受到广泛关注,但传统水凝胶释放的治疗药物在脑组织中扩散深度有限,难以清除远离腔隙的浸润肿瘤细胞。此外,手术创伤会进一步招募M2型抗炎巨噬细胞,加剧局部免疫抑制。如何同时解决药物深层穿透和免疫微环境重塑两大难题,是术后GBM治疗的关键挑战。
近期,华南理工大学医学院杜金志教授、都小姣教授开发了一种可注射双交联水凝胶平台(PF127-PTX Gel),该水凝胶利用Pluronic F127(PF127)固有的低黏附与润滑特性,可在手术切除腔内原位生成具有高度穿透性和免疫刺激活性的纳米胶束。
2026年4月13日,相关工作以“Injectable Trojan Horse Hydrogel Unleashing Penetrable and Immunostimulatory Nanomicelles for Postoperative Treatment of Glioblastoma” 为题发表在《ACS Nano》上(ACS Nano 2026, DOI: 10.1021/acsnano.6c03253)。文章共同第一作者为华南理工大学医学院硕士研究生张鑫和华南理工大学附属第二医院博士后罗佳琪。该研究得到国家自然科学基金委的支持。
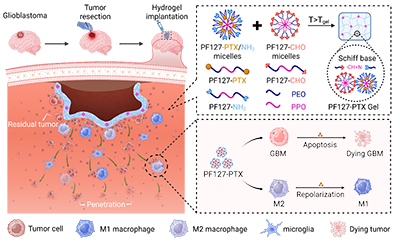
图1. 可注射PF127-PTX前药水凝胶预防GBM术后复发的示意图。
水凝胶注入切除腔后,动态亚胺键在生理条件下逐步断裂,持续释放PF127-PTX前药胶束。胶束的小尺寸和抗黏附表面特性增强了其在脑组织中的扩散和深层穿透。释放的PTX前药清除残留肿瘤细胞,同时诱导“吃我”信号表达,促进巨噬细胞介导的吞噬作用,并将巨噬细胞重编程为促炎M1表型。
1、精准设计兼具物理与化学双交联的智能水凝胶
研究团队首先基于两亲性高分子Pluronic F127(PF127),分别合成了氨基封端PF127-NH2和醛基封端PF127-CHO,并将化疗药物紫杉醇(PTX)通过琥珀酸连接臂偶联到PF127-NH2上,得到高分子前药PF127-PTX。在水溶液中,PF127-PTX可自组装成平均直径约28 nm的纳米胶束。将PF127-PTX胶束与PF127-CHO胶束混合后,氨基与醛基之间形成动态席夫碱化学交联,同时PF127嵌段间的疏水作用提供物理交联,二者协同形成可注射的物理-化学双交联水凝胶PF127-PTX Gel。该水凝胶在低温下为可流动溶胶,注射至体温(37 °C)后迅速凝胶化。与单纯物理交联的PF127水凝胶相比,双交联体系在皮下注射后荧光信号可维持长达15天,显著延长了局部滞留时间,并且降解过程中可持续释放出PF127-PTX纳米胶束,为后续深层穿透提供了保障。
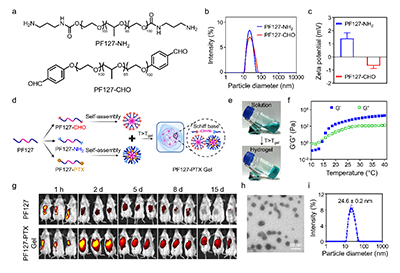
图2. 原位形成水凝胶的构建与体内滞留评价。
2、“特洛伊木马”策略:小尺寸润滑胶束实现脑组织深层穿透
研究团队采用Cy5标记的PF127胶束,分别在体外3D肿瘤球模型和离体GBM组织切片中验证其穿透能力。体外3D肿瘤球模型中,游离Cy5主要局限在肿瘤球外周,而PF127-Cy5可均匀穿透至深部。在离体GBM组织切片中,PF127-Cy5同样实现了更深、更均匀的分布,证实了其优异的组织穿透能力。
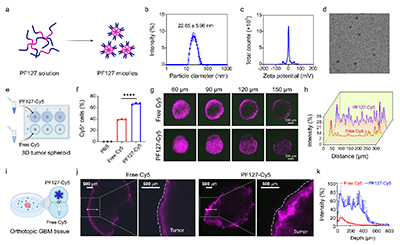
图3. PF127胶束在3D肿瘤球和离体GBM组织中的穿透能力。
3、体内免疫重塑与协同抗CD47抗体治疗
团队构建小鼠颅内原位GBM切除模型,并于术后原位注射PF127-PTX Gel。对照组小鼠中位生存期仅约20天。单独使用PF127-PTX Gel治疗后,50%的小鼠存活超过100天;联合抗CD47抗体后,长期生存率进一步提升至66.7%。免疫荧光染色显示,联合治疗组肿瘤组织中浸润的巨噬细胞多为CD86? M1型,而CD206? M2型显著减少,证实了有效的免疫微环境重塑。
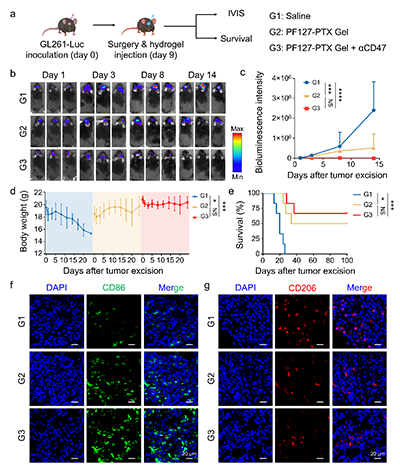
图4. PF127-PTX Gel联合抗CD47抗体在GBM术后切除模型中的治疗效果。
总结
该研究成功构建了一种基于Pluronic F127的双交联可注射水凝胶平台,通过巧妙利用PF127固有的抗黏附润滑特性,实现了小尺寸纳米胶束在脑组织中的深层穿透;同时,释放的PTX前药不仅直接杀伤残留肿瘤细胞,还能将肿瘤相关巨噬细胞从免疫抑制M2表型重编程为促炎M1表型,恢复其吞噬功能。与抗CD47抗体联合应用时,进一步激活了适应性T细胞免疫应答,在多种GBM原位/切除模型中显著抑制肿瘤生长并延长生存期。这一“特洛伊木马”策略为克服局部治疗药物穿透深度不足和术后免疫抑制两大瓶颈提供了全新思路,有望成为GBM术后辅助治疗的有力候选方案。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.6c03253
- 中国科大李良彬教授团队崔昆朋/李薛宇 Macromolecules:双交联强韧聚两性电解质水凝胶的多轴应力松弛机制 2026-04-29
- 北京林业大学张世锋教授团队 Nano Lett.:双交联策略突破无甲醛胶黏剂性能瓶颈 2025-02-14
- 中石大(华东)戴彩丽、赵明伟课题组 AFM:超分子作用+化学延迟交联构筑超深层冻胶压裂液 2024-04-26
- 港中大(深圳)唐本忠院士团队 ACS Nano:可注射NIR-II水凝胶实现荧光成像引导的肥胖局部精准治疗 2026-05-24
- 复旦大学俞麟教授 AFM:可注射的热疗水凝胶通过调节炎症和细胞外基质代谢来抑制椎间盘退变 2026-04-05
- 浙大张鹏 Adv. Mater.:阴离子-π互锁结构可注射导电水凝胶 - 构建稳定的组织-生物电子桥梁 2026-03-21
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
