相关研究表明,口服蛋白类药物凭借副作用小、高选择性和高效率等优点经常被作为治疗许多人类疾病的前药。然而,面对口服过程中苛刻的胃酸和多种酶环境以及肠道黏膜屏障的挑战,如何提高口服蛋白类药物的生物利用率仍然是口服递送系统待解决的技术瓶颈。因此,寻找一种新的口服药物递送策略是提高治疗性蛋白药物的口服利用率的潜在解决方案。

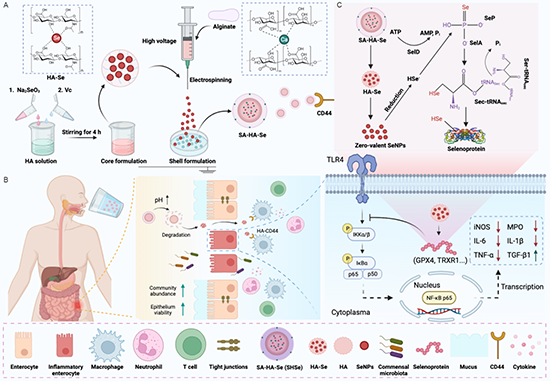
图1 :海藻酸钙纳米硒水凝胶SHSe的制备以及原位合成硒蛋白的机制示意图
硒蛋白在免疫细胞和炎症调节中起着至关重要的作用。然而,作为一种在胃酸性和酶环境中易变性或降解的蛋白质类药物,硒蛋白的高效口服给药面临着巨大的挑战。基于此,该研究创新设计了一种基于口服海藻酸钙(SA)纳米硒水凝胶微珠的生化策略,可以跨越胃肠道的生理屏障直接在体内原位合成硒蛋白,因此绕过了口服蛋白类药物递送要求的必要性和苛刻条件,同时有效地产生用于治疗应用的硒蛋白,在一定意义上极大地改善了治疗性蛋白类药物的口服利用率。SHSe纳米硒水凝胶微珠是通过用海藻酸钙(SA)水凝胶保护壳包裹核心药物透明质酸(HA)修饰的硒纳米颗粒合成的。
炎症性肠病IBD 是与肠道免疫和微生物群相关的最具代表性的疾病之一,因此该研究在IBD模型小鼠中验证了这一原位合成硒蛋白的策略。研究结果表明,SHSe纳米硒水凝胶微珠介导的原位合成的硒蛋白可以显著减少促炎因子的分泌并介导免疫细胞(例如,减少中性粒细胞和单核细胞并增加免疫调节性 T 细胞),从而有效缓解结肠炎相关症状。该策略还能够调节肠道微生物群组成(增加益生菌丰度并抑制有害菌群)以维持肠道稳态。考虑到与癌症、感染、炎症等广泛相关的肠道免疫和微生物群,这种原位硒蛋白合成策略也可能广泛应用于各种疾病。
HA-Se纳米颗粒和SHSe纳米硒凝胶微珠的合成与表征
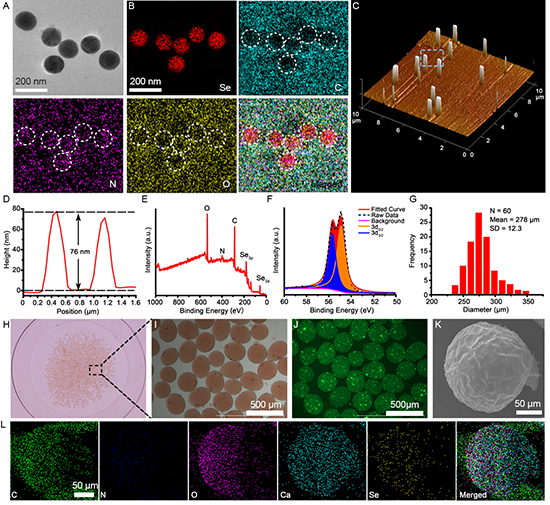
图2 : HA-Se纳米颗粒和SHSe纳米硒凝胶微珠的合成与表征
HA-Se纳米颗粒和SHSe纳米硒凝胶微珠的体外特性

图3 : HA-Se纳米颗粒和SHSe纳米硒凝胶微珠的体外特性
SHSe纳米硒凝胶微珠对DSS诱导的IBD小鼠的治疗效果

图4:SHSe纳米硒凝胶微珠对DSS诱导的IBD小鼠的治疗效果
体内的治疗效果。该研究首先评估了SHSe纳米硒凝胶微珠在DSS诱导的IBD小鼠体内的靶向能力和在结肠中的停留时间。接着,通过对比不同处理组IBD小鼠中的结肠长度、便血情况、体重和脾重的变化发现,口服SHSe纳米硒凝胶微珠后的这些指标均趋近于对照组。并且HE染色的结肠切片进一步表明,口服SHSe纳米硒凝胶微珠后的治疗组中杯状细胞和肠隐窝的数量明显增多,且炎症细胞的浸润明显减少(Control组(G1)、DSS组(G2)、DSS+SA组(G3)、DSS + HA-Se组(G4)、DSS + SHSe组(G5))。
SHSe纳米硒凝胶微珠抑制肠道炎症并促进组织修复
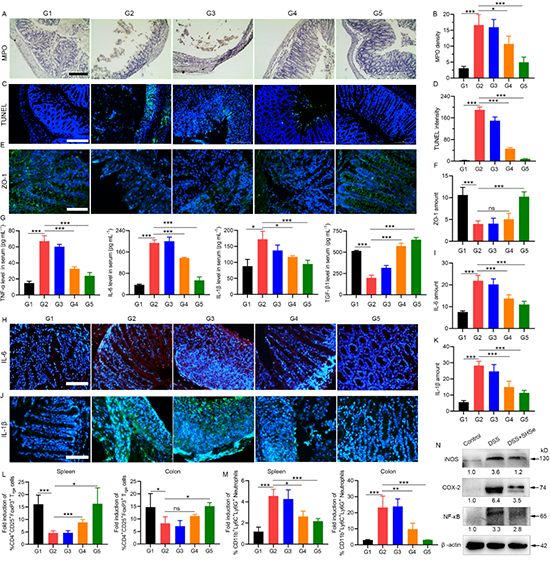
图5:SHSe纳米硒凝胶微珠抑制肠道炎症并促进组织修复
SHSe纳米硒凝胶微珠体内合成硒蛋白的机理研究
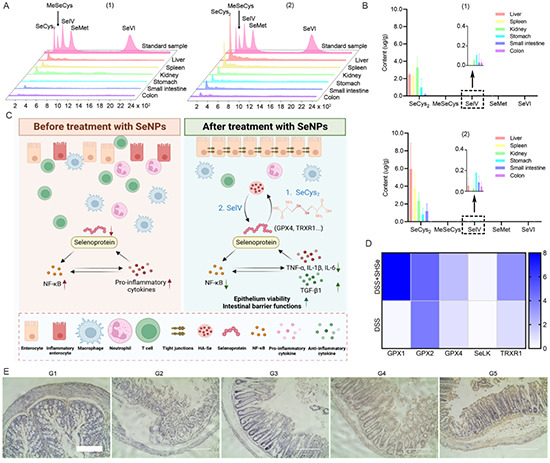
图6:SHSe纳米硒凝胶微珠体内合成硒蛋白的机理研究
16S核糖体RNA测序分析SHSe纳米硒凝胶微珠调控的肠道菌群
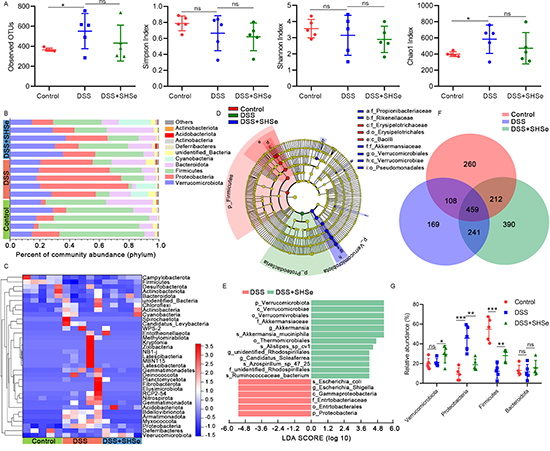
图7:16S核糖体RNA测序分析SHSe纳米硒凝胶微珠调控的肠道菌群
课题组简介
陈填烽教授,现任暨南大学教授,国家杰出青年基金获得者、万人计划青年拔尖人才、国家863青年科学家、教育部新世纪优秀人才、霍英东青年教师奖获得者、广东省杰青/特支计划入选者。现任化学与材料学院副院长,附属第一医院纳米诊疗研究所所长,广东省纳米化学创新药物工程技术研究中心主任。研究方向为硒纳米医学与疾病精准诊疗应用。相关研究成果在Signal Transduct.Target. Ther.,Cell子刊Matter,Sci. Adv.,J. Am. Chem. Soc.,Angew. Chem. Int. Ed., Adv. Funct. Mater., Biomaterials等本领域IF>10期刊发表论文86篇,封面论文41篇,h-index73,连续三年入选“中国高被引学者”榜单;2021、2022年入选全球顶尖10万科学家榜单。申报中国专利92项,授权国家发明专利23项,实现技术成果转化13项,实现了纳米硒GMP吨级生产,并开展多中心临床研究。以第一完成人获得2020年高等学校科学研究优秀成果奖技术发明二等奖,2020年中国抗癌协会科技二等奖,2018年中华医学科技奖青年科技奖,2018广东省自然科学二等奖等科技奖励。
课题组网页:https://chembio.jnu.edu.cn/
陶伟教授是哈佛大学附属布莱根妇女医院Farokhzad Family创新杰出讲席教授(Endowed Chair)、哈佛大学医学院助理教授,也是所在单位历史上第一个以助理教授身份获得冠名杰出讲席教授头衔(Farokhzad Family Distinguished Chair for Innovation)的华人学者。陶教授致力于药物载体和生物材料的研发及其广泛的生物医学应用(尤其是mRNA/siRNA等核酸药物的递送),目前以独立通讯或最后通讯作者身份在《自然》系列期刊(Nat Med, Nat Nanotechnol, Nat Rev Cancer, Nat Rev Mater, Nat Rev Cardiol, Nat Protoc等)、《美国科学院院刊》(PNAS)、《细胞出版社》系列期刊(Matter, Med, Trend Chem等)、Nat Commun/JACS/Angew Chem/Adv Mater/Chem Rev/Chem Soc Rev等国际顶级期刊发表论文80余篇。
陶教授是科睿唯安“全球高被引学者”、全球前2%顶尖科学家,《麻省理工科技评论》曾将他选为中国科技创新35人之一(TR35),微软学术曾将他选为纳米技术的全球前5位趋势作者以及纳米医学的顶级作者。此外,化学领域期刊Chem Soc Rev曾将陶教授选为全球范围内的Emerging Investigator,材料领域期刊Adv Mater和Mater Today也都曾共同将陶教授评为Rising Star。陶教授还作为PI获得了美国METAvivor青年研究员奖、美国心脏协会合作科学奖、哈佛大学医学院/布莱根妇女医院启动基金、纳米医学研究中心基金、系基础科学基金、Khoury科技创新奖、Gillian Reny Stepping Strong研究中心突破创新者奖、纳米技术基金、健康技术创新基金等项目资助。陶教授还受邀担任了多个科学期刊的主编/副主编/编委会成员(包括《细胞出版社》Matter期刊的顾问编委等)。
课题组网页:https://www.weitaolab.com/
原文链接:https://doi.org/10.1021/jacs.3c02179
- 中国矿业大学 Nat. Commun.:深地深空复杂条件微环境管理多级异质界面纳纤 2026-05-15
- 杭师大朱雨田教授、陈建闻副教授/南开刘遵峰教授 AFM:连续静电纺丝核鞘摩擦电纳米纱线 - 无缝集成的高输出多功能传感材料 2025-11-25
- 北京纳米能源所董凯团队 Adv. Mater.:提高半晶生物聚合物机电转换性能的通用取向工程策略 2025-08-19
- 广西大学林宝凤教授团队 IJBM: 铜氨纤维的新应用 - 原位合成 HKUST-1构建壳聚糖季铵盐活性包装膜 2025-02-20
- 河北大学张海磊/杨艳民与马萨诸塞大学韩刚合作再发 Nat. Commun.:在X射线诱导原位合成水凝胶领域取得新进展 2024-04-18
- 浙江大学徐志康教授/张超研究员团队 Small:支撑液膜穿上聚酰胺装甲,耐用的新型气体分离膜 2024-02-22
