
针对这一挑战,美国劳伦斯伯克利国家实验室Yi Liu课题组在前期工作基础上(Angew. Chem. Int. Ed. 2019, 58, 17978 – 17985; Chem. Commun. 2020,56, 4472;Nat. Commun.2021,12, 6818; J. Am. Chem. Soc. 2023, 145, 5474?5485; Acc. Chem. Res. 2023, 56, 1669–1682; Nat. Commun. 2025, 16, 3498),与澳大利亚费林德斯大学Michelle L. Coote课题组合作,创新性地提出通过调控单体的芳香性来改变其反应性,从而实现对TCP路径的精确控制。研究人员选择对位-氮杂醌二甲烷(AQM)环体系作为研究对象,通过改变其末端基团的芳香性,研究了不同取代基对反应路径的影响。具体而言,他们将传统的苯基(Ph)替换为芳香性较弱的呋喃基(Fu),发现这种改变能够显著影响单体的电子自旋密度分布,进而引发独特的反应行为。

图1(a) 先前报道的与(b)当前研究的AQM单体在固态反应中表现出不同的反应活性。(c)和(d)展示了这两种单体的显著基态共振贡献结构。
研究团队设计并合成了两种AQM衍生物:苯基取代的Ph-AQM-Ph和呋喃基取代的Fu-AQM-Fu。通过X射线单晶衍射(SCXRD)分析,发现两种单体在固态下均呈现柱状堆积结构,但Fu-AQM-Fu的分子间距离更短(3.56 ? vs. 3.67 ?),且柱间排列方式不同。研究表明,Ph-AQM-Ph与Fu-AQM-Fu表现出截然不同的固态反应性和溶液反应性。

图2 X射线单晶结构显示(a) Fu-AQM-Fu和(b) Ph-AQM-Ph不同的柱状堆积模式及碳碳间距(dcc)。(c) Fu-AQM-Fu的差示扫描量热曲线。(d) Fu-AQM-Fu粉末在150°C加热1小时过程中的X射线衍射图谱。(e) Fu-AQM-Fu及其聚合产物的傅里叶变换红外光谱。(f) Fu-AQM-Fu及其聚合产物的交叉极化魔角旋转13C核磁共振谱。
固态反应性差异
Ph-AQM-Ph在光照或加热条件下,反应仅局限于环外的亚甲基碳,形成传统的线性聚合物。Fu-AQM-Fu对光不敏感,但在加热条件下表现出独特的反应性。通过差示扫描量热法(DSC)和粉末X射线衍射(PXRD)证实,Fu-AQM-Fu在142°C左右发生放热聚合反应,生成两种聚合物(P1和P2)。其中,P1通过柱间呋喃-亚甲基偶联形成,其主链包含呋喃单元,这是一种前所未有的结构。P2则通过柱内亚甲基-亚甲基偶联形成,与传统路径类似。同位素标记实验和固态核磁共振(CP-MAS 13C NMR)进一步验证了这两种路径的存在。
溶液反应性
在甲苯溶液中加热Fu-AQM-Fu时,主要生成一种环蕃二聚体(cyclophane 1),其结构通过X射线晶体学确认。这种二聚体的形成表明,呋喃基的引入使得反应中心从亚甲基扩展到呋喃环,从而实现了区域选择性的偶联反应。相比之下,Ph-AQM-Ph在相同条件下不发生反应,凸显了呋喃基对反应性的关键影响。

图3 (a) Fu-AQM-Fu在溶液中通过热活化二聚反应形成环蕃1。(b) 环蕃1的X射线单晶结构棒状图示,右侧图中省略了三氟甲磺酸基团以增强清晰度。(c) 环蕃1的1H核磁共振谱和(d) 13C核磁共振谱(CD2Cl2,298 K)。星号标注的峰为真空脂杂质峰。
密度泛函理论(DFT)计算表明,Fu-AQM-Fu在基态为闭壳层单线态,但其开壳层双自由基共振形式在热激活下显著参与反应。电子自旋密度分析显示,Fu-AQM-Fu的自旋密度不仅分布在亚甲基碳上,还扩展到呋喃环,从而为新的反应路径提供了可能。计算还揭示了三种可能的二聚化路径,其中呋喃-亚甲基偶联路径(path 2)在能量上最为有利,与实验结果一致。

图4
图4 分数占据数加权电子密度(FOD)图显示Fu-AQM-Fu和Ph-AQM-Ph在0.005 e/Bohr3等值面的电子分布(渲染为青柠色)。Fu-AQM-Fu的电子在整个共轭骨架上离域分布,而Ph-AQM-Ph的电子则局域于亚甲基中心。
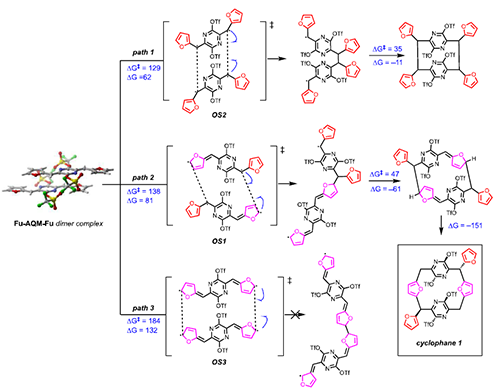
图5
图5 Fu-AQM-Fu通过三种不同偶联路径二聚化的能垒和反应吉布斯自由能(120°C,甲苯溶剂),计算采用ωB97X-D/may-cc-pVTZ/SMD//M06-2X-D3/6-31G(d,p)/PCM理论方法。能垒值从反应二聚体预复合物开始计算。
通过调控末端基团的芳香性,该研究成功实现了对TCP路径的精准控制,合成了主链含呋喃单元的聚合物(P1),这种结构通过传统方法难以获得。

图6 (a) Fu-AQM-Fu固态反应产物的直接13C核磁共振谱。低化学位移区的显著峰对应于13C标记的sp3杂化碳特征信号,而高化学位移区的弱峰源自天然丰度的未标记碳。(b) Fu-AQM-Fu聚合产物与环蕃1的sp3碳共振信号叠加谱。直接13C NMR谱表明同时生成的聚合物P1与P2的比例为1:1.5。(c)和(d)分别展示了通过(c) OS1开壳中间体的柱间聚合和(d) OS2开壳中间体的柱内聚合形成P1和P2的示意图。星号(*)标示13C标记的碳中心。
该研究通过调控AQM衍生物的末端基团芳香性,成功实现了对拓扑化学聚合路径的定向调控,并揭示了自旋密度分布对反应路径的关键影响,提出了“自旋中心导向”的TCP机制,为设计新型功能材料提供了理论依据。另外,环蕃二聚体的形成展示了其在主-客体化学中的潜在应用价值。这一发现不仅丰富了TCP的化学工具箱,还为设计具有特定功能的聚合物材料提供了新思路。未来,这一策略有望应用于更多前芳香体系,推动功能材料的发展。
原文链接https://pubs.acs.org/doi/10.1021/jacs.5c03077?goto=supporting-info
