心血管疾病作为全球首要致死病因,其约85%的死亡源于血管阻塞所致的缺血性心脏病。在冠状动脉介入治疗领域,药物涂层球囊(DCB)以其“无植入”优势引领临床革新,但术后管腔再狭窄仍困扰临床。其核心问题在于内皮屏障完整性的破坏--球囊扩张引发活性氧(ROS)爆发,导致内皮细胞间紧密连接(TJs)结构崩解,进而触发炎症风暴与平滑肌异常增生。传统疗法聚焦抗增殖或促内皮再生,但常忽视了TJs修复这一维系血管稳态的“第一道防线”。
为此,浙江大学傅国胜/黄翯/赵静团队,从介入创伤引发的血管微环境变化出发,创新性地将“内皮屏障精准修复”理念融入介入器械设计,开发了一种可喷涂、ROS响应型水凝胶涂层(OA@G-NO/B-EC)。它像“感知伤口”般响应微环境变化,精准修复内皮屏障,破解再狭窄难题。凝胶涂层适配超声喷涂工艺,制备精确可控,具有重要的转化潜力。

研究成果以“Sprayable Reactive Oxygen Species-Responsive Hydrogel Coatings Restore Endothelial Barrier Integrity for Functional Vascular Healing”为题发表于ACS Nano期刊,并得到浙江大学计剑教授与任科峰教授的指导与支持。
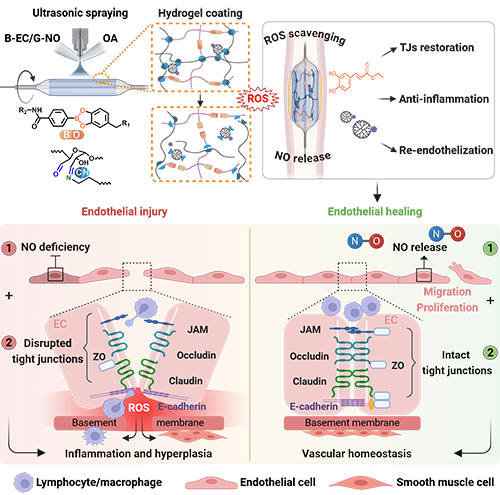
图1 ROS响应水凝胶涂层(OA@G-NO/B-EC)动态修复内皮屏障,抑制血管再狭窄。病理阶段:球囊损伤导致TJs破坏,ROS爆发诱发M1型巨噬细胞浸润及平滑肌增生;修复阶段:涂层靶向释放抗氧化剂(清除ROS,修复TJs)与NO(激活内皮迁移),逆转M1/M2巨噬细胞极化,重建血管稳态
【文章要点】
一、ROS清除与NO释放水凝胶涂层
OA@G-NO/B-EC水凝胶通过超声静电喷涂工艺精确制备,主要由可逆的苯硼酸咖啡酸酯前药(B-EC)和大分子一氧化氮(NO)供体(G-NO)组成。二者通过席夫碱反应与多巴胺修饰的氧化多糖(OA)在共喷涂过程中实现瞬时自交联。水凝胶能够通过氢键、阳离子-π等多重作用力与血管内壁发生相互作用。双动态共价键(席夫碱键+苯硼酸酯键)使得该水凝胶涂层能在ROS积累时逐步解聚,精准释放抗氧化剂咖啡酸酯和NO供体。实验结果显示,在1 mM H?O?刺激下,药物释放率达到42%,ROS清除率超过85%。在300 μM H?O?刺激下,G-NO释放量即达到60%。
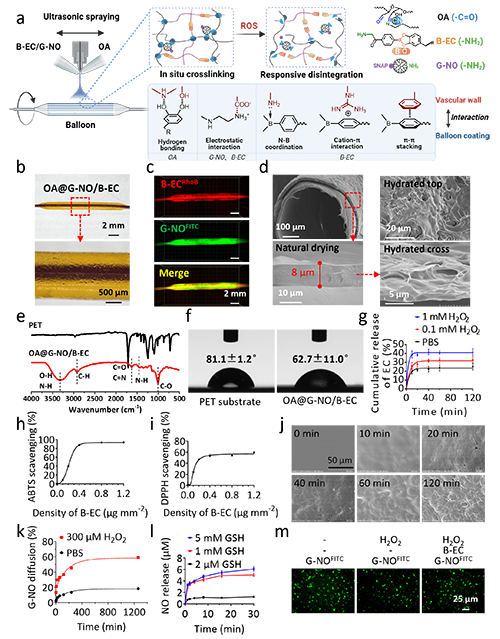
图2 OA@G-NO/B-EC凝胶涂层的制备与表征
二、加强内皮紧密连接、减少炎性细胞浸润
涂层能够有效恢复内皮细胞间TJs关键蛋白(如ZO-1、Claudin-5和JAM-A的表达分别增加26%、111%和54%),减少巨噬细胞的黏附与迁移(分别降低78%和19%),降低内皮通透性(Evan blue和FITC-dextran的渗透分别减少64%和7%)。RNA测序分析表明,涂层通过上调TJs相关基因,抑制NF-κB通路,促进内皮修复。
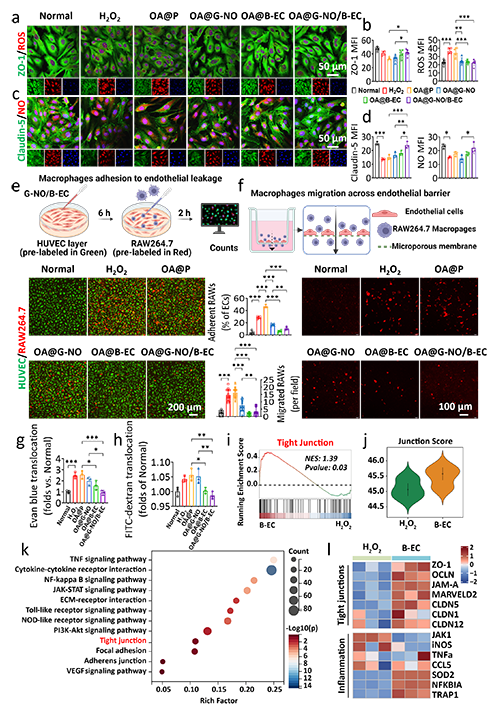
图3 OA@G-NO/B-EC介入后内皮间紧密连接和巨噬细胞渗透
三、即时涂层转移、维持血管通畅性
在大鼠腹主动脉模型中,水凝胶涂层能迅速转移到动脉壁上,且该涂层未促进血小板附着或聚集,无栓塞风险。30天后超声显示,OA@G-NO/B-EC涂层组血流速度积分(VTI)提升12%,血管内径扩大17%。H&E染色显示新生内膜面积减少38%。
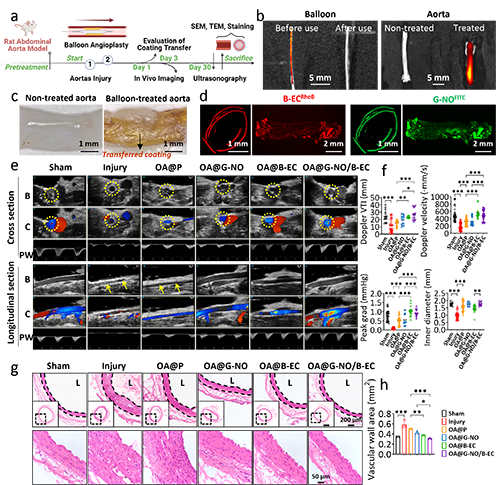
图4 OA@G-NO/B-EC涂层球囊进行体内腹主动脉扩张
四、加速内皮愈合和功能修复
OA@G-NO/B-EC涂层显著促进了内皮细胞增殖与迁移(eNOS免疫荧光染色证实内皮覆盖率超70%),并恢复了内皮TJs的结构(TJs宽度从91.56 nm恢复至17.21 nm,接近正常水平)、提升相关蛋白表达和分布,为血管修复提供了长效保护。该凝胶涂层能够有效促进内皮修复,抑制炎症反应,防止再狭窄。
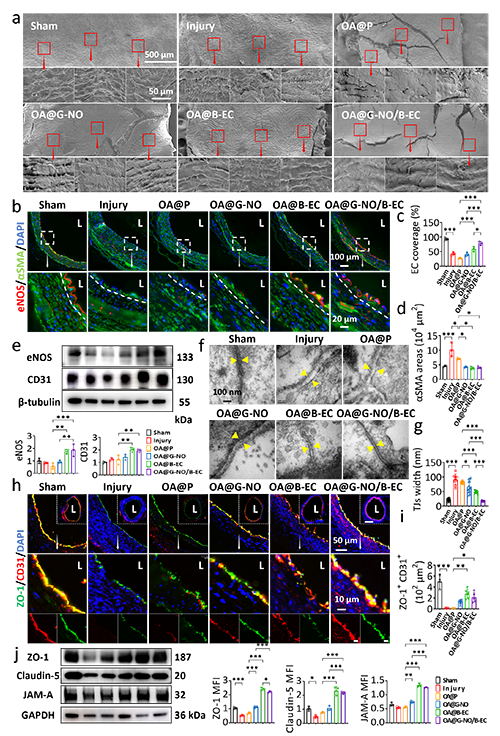
图5 介入治疗后主动脉的内皮覆盖和屏障功能完整性
【结论与展望】
本研究设计的新型ROS响应水凝胶涂层(OA@G-NO/B-EC)通过双动态共价键实现精准治疗,功能协同:ROS触发涂层崩解,释放咖啡酸酯(清除ROS,修复内皮TJs)与NO供体(促进内皮再生),提升TJs蛋白(ZO-1、Claudin-5、JAM-M)表达,降低内皮通透性。动物实验显示,涂层球囊使血管壁面积恢复至近正常水平,炎症因子显著下降,内皮覆盖率提升;RNA测序证实其通过调控NF-κB/Nrf2通路重塑血管稳态。该涂层具有重要转化价值,适配超声喷涂工艺,涂层厚度及降解速率精确可控,且可拓展至支架、人工血管、心脏瓣膜等器械表面,推动局部药物递送技术的革新。
第一作者
赵静:浙大邵逸夫医院特聘研究员,天津大学博士,浙江大学博士后。主要研究方向为心血管植介入材料及表面改性,主持国家自然科学基金、浙江省自然科学基金和中国博士后自然科学基金等多个科研项目。近年来以第一/共一身份在Advanced Functional Material,ACS Nano,Acta Biomaterialia等国际著名期刊发表论文10余篇,授权国家发明专利3项,参编学术专著1章。并担任Front. Bioeng. Biotechnol.审稿编辑,以及Exploration、VIEW及J. Zhejiang Univ., Sci., A等杂志青年编委。
通讯作者
傅国胜:留德医学博士、主任医师、博士生导师、浙江大学求是特聘医师。现任浙江大学附属邵逸夫医院心内科主任,浙江省心血管介入与精准诊治研究重点实验室主任,心血管创新器械浙江省工程研究中心主任,浙江省医学重点学科心血管再生医学创新学科带头人。长期从事心血管临床和基础研究,是我国知名介入心脏病学专家,在复杂冠心病、瓣膜病介入治疗领域具有较高的造诣。所领导的科研团队致力于缺血性心脏病再生修复治疗和心血管介入器械的创新研究工作,近年来先后主持国家自然科学基金、国家重点研发项目子课题、省重点研发等多项重大科研项目,发表SCI论文50余篇,并荣获2015年度浙江省科技进步一等奖。
黄翯:浙江大学医学院附属邵逸夫医院副院长,浙江省心血管介入与再生修复研究重点实验室PI,中华医学会心血管病学分会女性健康学组委员,浙江省医学会心血管病学分会秘书长,浙江省医学会介入心血管病学分会委员,浙江省生物医学工程协会心律专业委员会腔内影像及干预学组副组长。主要研究巨噬细胞动脉粥样硬化进展与糖尿病代谢紊乱,动脉腔内影像学与多组学研究整合工作,主持国家自然科学基金,浙江省领雁项目,浙江省自然科学基金,浙江省中医药重大项目,浙江省委省共建重点项目多项,负责并管理浙江省多临床中心临床及转化研究。
傅佳寅:浙江大学本科及硕士,新加坡南洋理工大学博士,美国康奈尔大学博士后,现任浙江大学医学院附属邵逸夫医院特聘研究员。主要从事金属可降解心血管支架材料,水凝胶载药系统治疗血管损伤后内膜增生,人工血管及药物涂层球囊等研究。承担浙江省自然科学基金委探索青年项目1项,浙江省医药卫生科技计划青年创新项目1项,浙江省医药卫生科技计划一般项目1项。近5年发表SCI论文32篇,其中以第一作者或共同第一作者在Advanced Functional Material, ACS Nano,Bioactive Materials,Biomaterials,Small,Acta Biomaterialia,Trends in Biotechnoloqy等国际著名期刊上发表论文8篇,以第一发明人授权发明专利1项。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c05477
- 常州大学王建浩教授团队 IJBM:负载鱼腥草囊泡的微环境响应胶原水凝胶治疗糖尿病伤口的研究成果 2025-07-14
- 上海市第一人民医院马小军/东华大学何创龙 Bioact. Mater.:TME响应复合水凝胶靶向抑制MYC驱动型骨肉瘤生长与转移 2025-01-17
- 四川大学李旭东教授团队 ACS AMI:微环境响应型茶多酚-姜黄素颗粒稳定的多功能Pickering乳液用于感染伤口的愈合 2024-09-02
- 南京大学王炜/曹毅/薛斌团队 Nat. Commun.:仿生分级picot纤维水凝胶涂层实现超低摩擦与高耐磨性 2026-02-09
- 阿尔伯塔大学曾宏波/郑州大学杨闻帅团队 AFM:离子诱导构筑仿生装甲 - 强化水凝胶涂层防污防腐 2025-10-22
- 宁波材料所赵文杰、严明龙 Small:污损抑制/阻抗与自我更新协同的可降解有机硅水凝胶涂层 2025-05-10
- 中国人民大学贺泳霖等 Small:可喷涂超分子丙二醇凝胶 2025-05-15
