近年来,植入式生物电子器件正在深刻改变人类对神经系统和肌肉系统的调控方式。通过植入电极,人们可以实现神经信号记录、神经刺激以及疾病治疗。然而,这类技术仍面临一个关键挑战:植入电极与生物组织之间的长期稳定界面难以维持。尽管现代生物电子器件已经能够以较高精度与大脑、脊髓以及外周神经建立电学接口,但其刚性结构仍然难以适应生物组织复杂且动态变化的微环境。这种机械—生物学不匹配往往会引发一系列问题,例如微运动导致的组织损伤、模量差异持续引起的炎症反应,以及材料本身免疫原性带来的免疫反应。这些因素会逐渐降低电极信号质量,并缩短器件的使用寿命。因此,如何构建能够稳定维持的组织—电极界面,仍然是当前生物电子医学领域亟待解决的核心挑战。
近日,浙江大学高分子系张鹏研究员团队提出了一种基于阴离子-π互锁结构的可注射导电水凝胶(SSPH),用于构建长期稳定的生物电子接口。
2026年3月18日,相关研究以An Immunocompatible Conductive Hydrogel Via Anion-π Interlocking as an Injectable Bridge for Sustained Bioelectronic Interfacing为题发表在Advanced Materials上。浙江大学高分子系博士生朱梓豪为本文的第一作者,该研究得到国家自然科学基金委、浙江省基金委、经血管植入器械全国重点实验室的支持。
该材料兼具优异的可注射性、机械适配性、长期电化学稳定性以及与软组织的良好整合能力。不同于传统的贴片或涂层策略,SSPH能够通过微创注射直接填充不规则的组织间隙,随后将生物电子器件植入水凝胶中,从而在柔软的生物活性组织与刚性器件表面之间形成平滑的过渡界面。这种界面桥接策略不仅避免了传统生物电子器件在植入过程中面临的贴合性与涂层稳定性问题,还能有效缓解机械—生物学不匹配,从而支持植入生物电子器件的长期稳定运行。
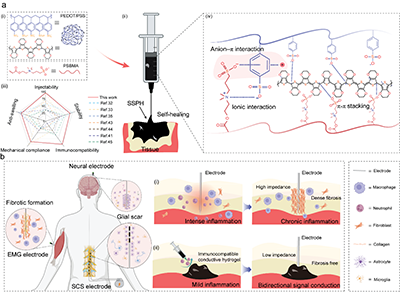
图1.可注射组织桥接材料(SSPH水凝胶)的设计及其界面应用。
一种可注射的“导电桥梁”
研究团队设计的SSPH水凝胶 由导电聚合物PEDOT:PSS与两性离子聚合物 PSBMA 自发组装形成。当两种组分在溶液中混合后,可迅速构建三维网络结构,形成兼具良好导电性与力学柔顺性的水凝胶体系。该网络的形成源于阴离子-π相互作用及多种协同非共价相互作用 的共同驱动,使体系在分子层面实现高度整合。具体而言,该结构主要包括三个关键特征:(i)PSBMA与PSS之间形成的 阴离子-π互锁结构;(ii)体系中多价带电基团之间的 静电相互作用;以及(iii)由PEDOT富集形成的连续纳米结构域,这些结构域在网络中充当稳定的物理交联节点。在多重相互作用的协同作用下,水凝胶内部形成了稳定且连续的导电通路,并且这一导电网络并不依赖传统的渗流结构。当材料受到形变或损伤时,动态非共价作用能够驱动网络结构重新组装,使水凝胶同时恢复其 力学性能与电化学性能。
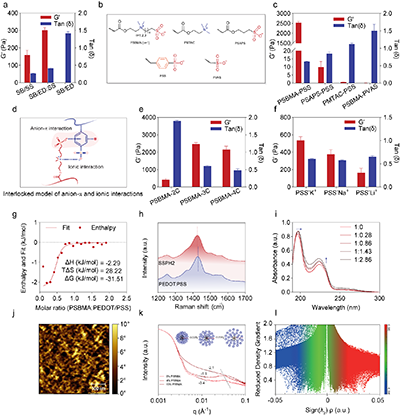
图2.SSPH水凝胶的成胶机理。
良好的电化学性能与免疫相容性
实验结果表明,该水凝胶不仅具有稳定的机械性能,还表现出优异的电化学稳定性。循环伏安测试显示,在1000次循环后电荷储存能力仍保持约90%,同时在10万次充放电循环中性能几乎没有明显衰减,说明其能够满足长期生物电子应用需求。此外,研究团队还通过体外细胞实验与体内动物实验系统评估了该材料的免疫相容性。结果表明,SSPH水凝胶在细胞培养实验中未表现出明显的细胞毒性;在小鼠皮下植入模型中,与对照材料相比,其诱导的炎症因子表达水平显著降低,同时材料周围的纤维化包裹也明显减少。这些结果表明,SSPH水凝胶能够有效缓解材料植入后引发的免疫反应,从而为植入器件提供更加稳定、友好的生物微环境,有利于长期体内应用。
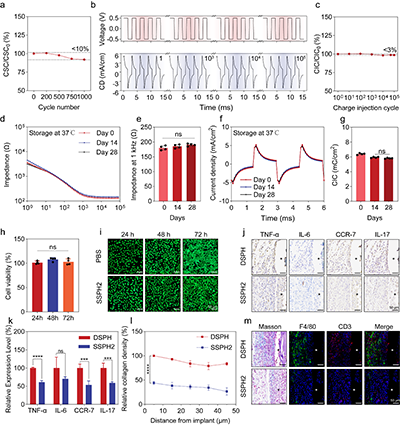
图3.电化学性能与免疫相容性评估
稳定的双向信号传导能力
在神经刺激实验中,研究团队首先将SSPH水凝胶注射到大鼠坐骨神经周围,并将刺激电极植入水凝胶内部,使电极不再直接接触神经组织。实验结果表明,在不同刺激电压和频率条件下,电刺激信号可以通过水凝胶稳定传递至神经组织,并成功诱导后肢产生与刺激信号一致的运动响应。与此同时,由于水凝胶在电极与神经之间形成了一层柔软且导电的界面缓冲层,不仅能够有效传导电信号,还显著减少了电极直接接触神经组织所可能造成的机械损伤,从而提高了神经刺激过程中的组织保护能力。
在慢性电极植入实验中,研究人员进一步评估了SSPH水凝胶对电极长期性能的影响。实验将电极植入大鼠肌肉组织,并通过对比裸电极与SSPH水凝胶桥接电极在28天内的信号变化情况,评估其记录性能。结果显示,在植入初期,两种电极均能够获得较高质量的肌电信号;然而随着时间推移,裸电极由于炎症反应和纤维组织包裹逐渐加重,其信号质量明显下降。而在SSPH水凝胶桥接条件下,电极周围的炎症反应和纤维化程度显著降低,使电极能够持续保持较低界面阻抗和较高信噪比,即使在长达四周的植入过程中仍能稳定记录高质量电信号,显示出优异的长期界面稳定性。
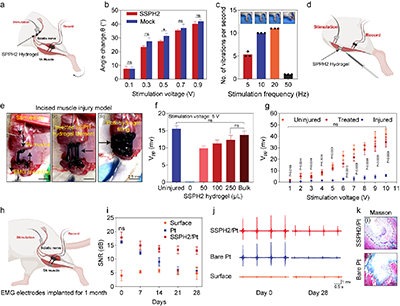
图4. SSPH2水凝胶在神经肌肉信号桥接及长期肌电电极性能提升中的评估
在脊髓刺激治疗中的长期稳定表现
脊髓刺激是目前临床上广泛应用的一种神经调控技术,主要用于治疗慢性神经病理性疼痛等疾病。通过在脊髓硬膜外空间植入电极并施加电刺激,可以调节脊髓神经信号的传导,从而减轻患者的疼痛症状。近年来,SCS技术也被进一步探索用于改善脊髓损伤后的运动功能恢复等神经系统疾病。然而,在长期植入过程中,电极与脊髓组织之间的机械不匹配以及持续的免疫反应,往往会导致电极阻抗升高、刺激效率下降,最终影响治疗效果。
针对这一问题,研究团队在大鼠神经病理性疼痛模型中评估了SSPH水凝胶在脊髓刺激中的应用潜力。实验中,研究人员将SSPH水凝胶注入脊髓硬膜外腔,并将刺激电极植入水凝胶内部,从而在电极与脊髓组织之间构建柔软且导电的界面桥梁。实验结果显示,在植入初期,两组电极均能够产生明显的镇痛效果;然而随着时间推移,裸电极由于炎症反应和纤维化包裹逐渐加重,其阻抗持续升高,刺激效果明显减弱。相比之下,SSPH水凝胶桥接电极能够有效缓解电极与组织之间的机械不匹配,降低炎症反应并减少纤维化包裹,使电极在长期植入过程中保持较低阻抗和稳定的刺激阈值。在持续数周的实验中,SSPH桥接电极仍能够维持稳定的镇痛效果,显示出长期神经调控性能。
综上所述,由阴离子-π相互作用驱动构建的SSPH可注射桥接材料,在可植入生物电子器件与生物组织之间形成了稳固、相容且柔顺的界面,从而在长期植入条件下保持稳定性能。在水凝胶网络内部,PSS与PSBMA之间的阴离子-π相互作用促进了凝胶的形成,而离子相互作用与疏水相互作用则进一步增强了三维网络结构。得益于这些相互贯穿网络之间的多重协同作用,该水凝胶同时表现出良好的可注射性、与组织匹配的力学顺应性、稳定的电化学性能以及优异的免疫相容性。当应用于组织—器件界面时,SSPH水凝胶能够实现有效的组织整合,并实现生理电信号几乎无损的传输。最终,这种可注射桥接材料能够显著减少由于刚性器件与柔软组织之间模量不匹配所引发的炎症反应和组织损伤,缓解免疫介导的纤维化包裹,从而支持生物组织与植入式生物电子器件之间的长期稳定电信号通信。
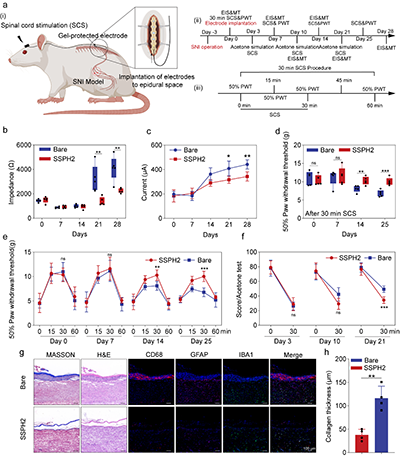
图5. 慢性神经痛模型中SSPH2/Pt脊髓刺激电极的长期性能与镇痛效果评估
张鹏研究员简介
张鹏,浙江大学高分子系百人计划研究员,博士生导师,经血管植入器械全国重点实验室成员。本科硕士毕业于天津大学。2018年博士毕业于美国华盛顿大学(西雅图)化学工程系,2018-2020年于美国麻省理工学院科赫综合癌症研究所Robert Langer院士团队进行博士后研究。张鹏研究员专注于生物医用高分子材料的研究,并以新材料为基础开发创新型的植介入医疗器械、大分子药物来满足相关临床需求。至今已在Nat. Biomed. Eng.、Nat. Comput. Sci,、Sci. Transl. Med.、 Nat. Commun.、PNAS、JACS、Adv. Mater. Angew. Chem. Int. Ed. 等国际一流期刊发表论文70余篇,引用8000余次。
原文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.72820
- 港中大(深圳)唐本忠院士团队 ACS Nano:可注射NIR-II水凝胶实现荧光成像引导的肥胖局部精准治疗 2026-05-24
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
- 复旦大学俞麟教授 AFM:可注射的热疗水凝胶通过调节炎症和细胞外基质代谢来抑制椎间盘退变 2026-04-05
- 华科大罗志强教授团队《Nat. Commun.》:可注射导电水凝胶实现无线、微创深部脑神经调控 2026-02-10
- 大连工业大学郭静/张森教授团队 Macromolecules:多重相互作用形成的有序纳米结构用于增韧超拉伸导电水凝胶 2025-11-10
- 中山大学付俊/南京林业大学韩景泉 AFM:基于Hofmeister效应的各向异性、抗溶胀导电水凝胶用于水下监测 2025-11-07
