干眼症(Dry eye disease, DED)是一种以泪液稳态失衡、眼表慢性炎症为核心特征的全球性眼表疾病,其发病率因电子屏幕过度使用等因素持续攀升,严重影响患者视力与生活质量。DED 的病理机制形成了氧化应激-炎症的恶性循环:泪膜不稳定引发的高渗环境会诱导眼表活性氧(ROS)过量积累,进而激活促炎因子释放,造成角膜上皮损伤、杯状细胞丢失,进一步加剧泪液分泌异常与炎症反应。
目前临床一线治疗以人工泪液润滑和环孢素A 等抗炎药物为主,但存在一定局限性:眼表黏液层、角膜上皮等生理屏障导致药物滞留时间短、生物利用度低,需频繁给药;且单一药物难以同时阻断氧化应激与炎症的多重病理环节,治疗效果有限。开发兼具长效眼表滞留、ROS 清除、抗炎修复的多功能治疗体系,成为突破 DED 临床治疗瓶颈的关键方向。天然多酚类物质因优异的抗氧化与抗炎活性备受关注,但其水溶性较差、酚羟基含量低导致的生物活性受限问题,阻碍了其临床转化。
近日,上海交通大学王寅教授与浙江大学韩海杰研究员团队合作在Nature Communications上发表了题为“Self-polymerized Polyphenol-based Platform for the Management of Dry Eye Pathogenesis” 的研究论文,上海交通大学博士研究生王子昕、浙江大学硕士研究生吕泽恩为论文共同第一作者。该研究开发了一种基于迷迭香酸自聚合的多酚基纳米滴眼液(s-RHC NPs),通过透明质酸(HA)模板调控、铈离子共组装及巯基化修饰,实现了眼表黏附性、抗氧化、抗炎与上皮修复等功能的多效整合。在苯扎氯铵(BAK)诱导的蒸发型干眼和东莨菪碱(SCOP)诱导的水液缺乏型干眼两种小鼠模型中,该纳米平台展现出优于临床药物环孢素 A(Restasis®)的治疗效果,为干眼症的综合治疗提供了新型多酚基纳米策略。
研究团队针对天然多酚的应用瓶颈和DED 的多重病理特征,设计了自聚合、共组装、巯基化的三步制备策略,构建了单分散的 s-RHC NPs 纳米复合体,并从理化特性、体外功能到体内疗效进行了系统验证(图1)。
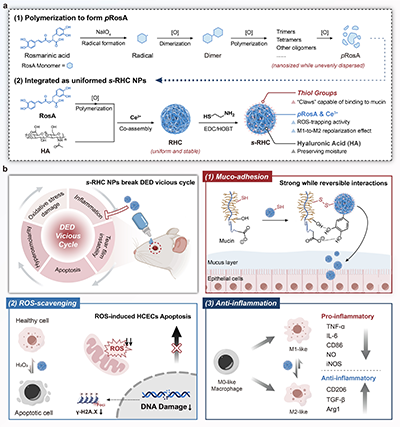
图1. s-RHC纳米颗粒的制备流程及干眼症治疗机制示意图
1. s-RHC NPs 的设计与理化特性表征(图2)
团队首先以高碘酸钠为氧化引发剂,对迷迭香酸(RosA)进行氧化自聚合得到聚迷迭香酸(pRosA),并引入 HA 作为模板提高聚合产物的稳定性,再与铈离子(Ce3?)共组装形成 RHC NPs;随后通过缩合反应在 RHC NPs 表面修饰巯基基团,得到不同巯基含量的 s-RHC NPs(s1/s2/s3-RHC)。结果显示,s2-RHC(后续简称 s-RHC) 表现出最优的黏蛋白结合能力,且巯基修饰未降低其抗氧化活性。
X 射线光电子能谱(XPS)证实 s-RHC NPs 中 Ce 以 Ce3?(78.9%)和 Ce??(21.1%)双价态存在,借助 Ce3?/Ce??的氧化还原循环实现 ROS 清除;体外抗氧化实验表明,s-RHC NPs 对多种自由基 展现出浓度依赖的清除能力。同时,s-RHC NPs 在 ROS 微环境中会发生形貌响应性变化,在表面逐渐形成小尺寸氧化铈颗粒,显著增加比表面积,进一步增强抗氧化效能。
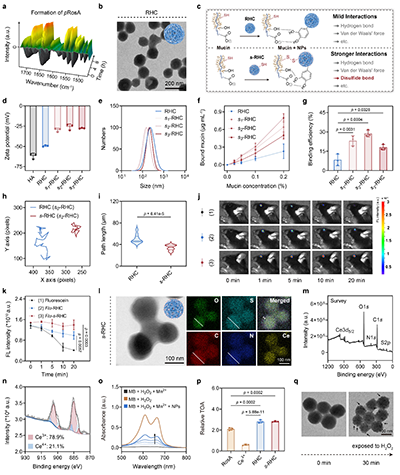
图2. s-RHC纳米颗粒的表征分析
2. 巯基化修饰实现长效眼表黏附与细胞内吞(图2+图3)
为实现眼表长时间滞留,研究团队利用巯基与黏蛋白中的二硫键进行交换反应,增强该纳米复合体的黏膜黏附性。纳米颗粒追踪分析(NTA)显示,RHC NPs 在黏蛋白溶液中自由扩散,而 s-RHC NPs 运动受限,均方位移(MSD)和有效扩散系数(Deff)显著降低;体内滞留实验证实,荧光标记的 s-RHC NPs 在小鼠眼表的滞留时间超过 20 min,荧光强度是游离荧光素的 4.5 倍、RHC的 2.3 倍,证实巯基化修饰能增强黏附作用。
同时,团队通过人角膜上皮细胞(HCECs)跨膜模型验证了 s-RHC NPs 的细胞内吞特性:其与黏蛋白的二硫键结合具有可逆性,初期内吞受抑制但后期可恢复至与 RHC NPs 相当的水平,且主要通过巨胞饮和小窝介导的内吞途径进入细胞,为后续胞内功能发挥奠定基础。
3. s-RHC NPs 的体外抗氧化性能与细胞保护作用(图3)
在H?O?诱导的 HCECs 氧化应激模型中,s-RHC NPs 能显著清除胞内 ROS,降低丙二醛(MDA,脂质过氧化标志物)水平,同时使超氧化物歧化酶(SOD)活性恢复至正常水平。流式细胞术结果显示,s-RHC NPs可有效抑制 H?O?诱导的细胞凋亡,活细胞比例显著高于游离的 RosA 或 Ce3?单药处理组。
转录组学(RNA-seq)和蛋白质组学分析进一步揭示了其分子机制:s-RHC NPs 显著下调p53 信号通路、IL-17 信号通路及细胞应激 / 凋亡相关基因(PPP1R15A、JUN、GADD45A),上调抗凋亡的 BCL-2 家族基因;亚细胞定位分析显示,差异蛋白主要分布于细胞核(34.18%),且 γ-H2A.X(DNA 双链断裂标志物)荧光焦点减少 80.5%,证实 s-RHC NPs 具有细胞核保护作用,有效缓解 ROS 介导的 DNA 损伤。
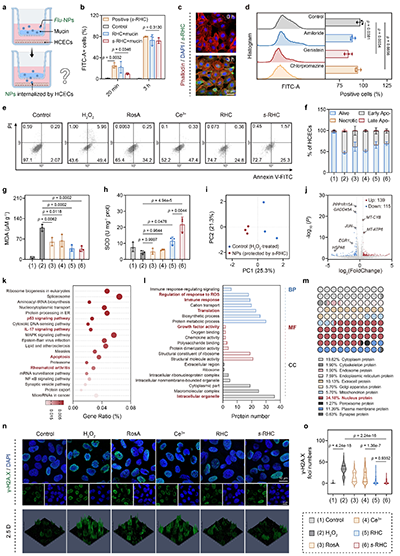
图3. s-RHC 纳米颗粒的内吞机制探究及抗氧化性能分析
4. s-RHC NPs 介导巨噬细胞 M1 向 M2 复极化,发挥抗炎作用(图4)
巨噬细胞的M1 型促炎表型在 DED 的炎症恶性循环中起关键作用,研究团队利用 LPS 诱导的 RAW264.7 巨噬细胞模型验证了 s-RHC NPs 的免疫调节功能。结果显示,s-RHC NPs 可被巨噬细胞通过网格蛋白介导的内吞和微胞饮摄取,并使巨噬细胞从 M1 型的不规则多边形转变为 M2 型的梭形;流式细胞术证实,s-RHC NPs 处理后 M2/M1 表型比值显著升高,优于游离的 RosA 和 Ce3?。
进一步机制研究表明,s-RHC NPs 可显著降低促炎因子 TNF-α、IL-6 的分泌和一氧化氮(NO)的生成,同时上调抗炎因子 TGF-β 的表达;免疫荧光染色显示,其能抑制诱导型一氧化氮合酶(iNOS)的表达,升高精氨酸酶 1(Arg1)水平,证实其可通过巨噬细胞 M1向M2 复极化阻断炎症信号传导,且能缓解炎症引发的继发性氧化应激。
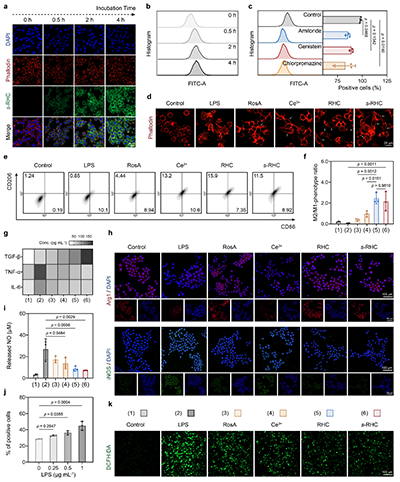
图4. s-RHC 纳米颗粒的抗炎性能分析
5. s-RHC NPs 在两种干眼小鼠模型中展现出优异的体内治疗效果(图5+图6)
最后,该团队在BAK(蒸发型)和 SCOP(水液缺乏型)两种小鼠干眼模型中,以临床药物 Restasis®为对照,证实了 s-RHC NPs 的卓越疗效。该制剂不仅能快速修复角膜损伤(3天显著改善,7天基本恢复),还显著延长了泪膜破裂时间,效果均优于阳性对照组。组织学分析显示,s-RHC NPs 有效恢复了角膜上皮厚度与杯状细胞数量,缓解了泪腺萎缩及炎症浸润;同时通过显著降低眼表 ROS、MMP-9 和 IL-6 水平,减少了细胞凋亡,展现出全面的抗炎与组织保护能力。
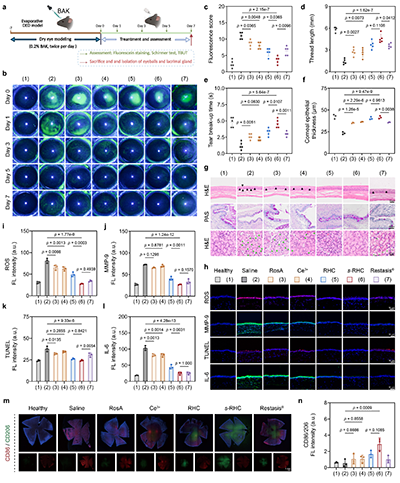
图5. s-RHC纳米颗粒在BAK蒸发型干眼症模型中的治疗效果探究
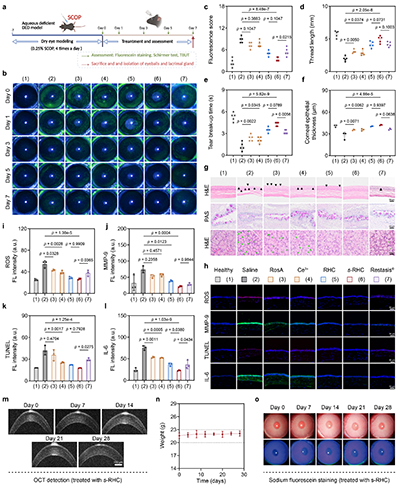
图6. s-RHC纳米颗粒在SCOP水液缺乏型干眼症模型中的治疗效果探究
本研究成功构建了一种基于迷迭香酸自聚合的多酚基纳米平台s-RHC NPs,通过 HA 模板调控解决了天然多酚聚合产物尺寸和形貌不均一的问题,Ce3?的引入实现了抗氧化与交联的双重功能,巯基化修饰则显著提升了眼表黏附性,最终实现黏附、抗氧化、抗炎、修复的多效协同。该纳米复合体在两种干眼小鼠模型中均展现出优于临床药物 Restasis® 的治疗效果,其核心优势在于:1)突破了天然多酚水溶性差、活性低的瓶颈,通过自聚合增强抗氧化与抗炎活性;2)实现了眼表长效滞留,提高了生物利用度,减少给药频率;3)多靶点阻断 DED 的氧化应激 - 炎症恶性循环,而非单一环节干预;4)制备工艺简便,采用自聚合与共组装策略,契合绿色化学理念。
研究也存在一定的局限性:目前仅在小鼠模型中验证了疗效,后续需在更接近人眼生理的大动物模型(如兔、猴)中进一步验证;其次,该纳米平台为局部滴眼给药,尚未探索其对干眼全身相关病理环节的调控作用。
尽管如此,该研究为干眼症的治疗提供了新型多酚基纳米策略,其天然多酚自聚合的设计思路可拓展至其他酚类化合物,为开发更多针对氧化应激和炎症相关疾病的多功能纳米平台奠定基础;同时,巯基化修饰增强眼表黏附的策略,也为其他眼用纳米制剂的设计提供参考。未来可通过进一步的剂型优化(如凝胶、眼膏)提升其滞留效果,并结合临床需求开展制剂的产业化研究,推动其向临床转化。
本研究得到了浙江省重点研发计划(2024C03073)、国家自然科学基金(22375128、82572387、82271064、22105126)、浙江省自然科学基金(LR23H120001)等项目的资助。
原文链接 https://www.nature.com/articles/s41467-026-70388-1
作者简介
王寅,博士生导师,入选上海市海外高层次人才引进计划,上海药学会药剂学专业委员会委员,长期从事硫化氢释放材料的相关研究,以第一作者(含共同一作)、通讯作者(含共同通讯)论文在Nature Communications、Journal of the American Chemical Society、Angewandte Chemie International Edition、Biomaterials、Nano Letters、Advanced Drug Delivery Reviews等国际一流学术期刊上发表SCI论文49篇,入选ACS Editors’Choice文章一篇,ESI热点文章一篇,高被引文章两篇,封面文章亮点展示两次,总引用4400余次,其中他引4100余次,H因子38。主持国家自然科学基金两项,上海市自然科学基金面上项目一项等项目,获得中国发明专利授权1项,Chemical Communications Emerging Investigators 2024,美兰湖优秀青年学者报告奖等荣誉与奖励。
韩海杰,博士生导师,浙江省杰出青年基金获得者,中国生物材料学会眼科生物材料及器械分会委员,并入选省科协青年人才托举培养项目。主要研究领域为针对重要致盲眼病的生物医用材料的基础和转化研究。以通讯/第一作者在Science Advances, Nature Communications, Advanced Science, Journal of the American Chemical Society, ACS Nano, Advanced Drug Delivery Reviews等学术期刊上发表论文近40篇,6篇论文入选ESI高被引论文,1篇论文入选热点论文;以第一申请人获得国家发明专利3项,其中2项已转化;作为负责人主持承担了包括国家自然科学基金面上项目(2项)和青年基金、浙江省“领雁”研发攻关计划项目、浙江省杰出青年基金、国家重点研发项目子课题等8项国家及省部级项目,及各类科研项目共计20余项。是国家重点研发计划,国家自然科学基金面上/青年项目等多个项目的评审专家。
- 华西口腔王军/西南交大谢超鸣/华西医院刘瑾 Nat. Commun.:多酚介导锌氧协同水凝胶通过重塑衰老微环境促进牙周再生 2026-03-14
- 川大李乙文/杨振团队 Adv. Mater.:从黑色素到木质素-基于多酚-金属离子配位效应制备生物质可持续界面蒸发器用于废水处理 2025-08-28
- 东南大学葛丽芹教授与合作者 Research:微气泡为模板的免疫活性金属多酚胶囊用于药物递送和增强的肿瘤免疫治疗 2025-07-31
- 东华大学/苏州大学严锋教授团队 Angew:离子液体与CO2自聚合成聚碳酸酯 2026-05-14
- 浙江理工大学吕维扬/华东理工大学邢明阳 Nat. Commun.:高效芬顿催化剂合成新策略 2023-12-05
- 四川大学顾志鹏/高会乐 Adv. Mater.:天然多酚纳米点材料用于阿尔兹海默症治疗 2023-11-29
- 苏州大学刘庄教授/张晓峰教授等 Adv. Mater.: 干眼症治疗新曙光 - 天然抗氧化酶纳米滴眼液的创新之旅 2025-03-26
