嵌合抗原受体(CAR)T细胞疗法在治疗血液恶性肿瘤中取得了显著突破,但其在实体瘤(如胰腺癌)中的疗效仍受限制。山东大学药学院栾玉霞教授团队发现,CAR-T细胞在实体肿瘤中的导航缺陷(包括肿瘤内浸润不足和空间定位不佳)是导致疗效不理想的关键因素。基于此,团队提出了一种创新的胶原酶纳米凝胶背包策略,旨在解决这一导航缺陷,从而大幅提高CAR-T细胞治疗实体瘤的疗效。

相关研究成果以“A collagenase nanogel backpack improves CAR-T cell therapy outcomes in pancreatic cancer”为题,已在线发表于Nature Nanotechnology,2025,DOI: 10.1038/s41565-025-01924-1。山东大学为唯一单位,博士研究生赵志鹏与李倩为本文共同第一作者,栾玉霞教授为唯一通讯作者。
该研究中的纳米凝胶(DV1@O-Colase)通过化学交联胶原酶制备,并用CXCR4拮抗剂(DV1)修饰。这些纳米凝胶通过受体-配体相互作用与CAR-T细胞结合,形成CAR-T细胞结合的纳米凝胶背包递送系统(DV1@O-Colase#CAR-T)。该系统能够有效突破胶原蛋白丰富的细胞外基质,破坏趋化因子(CXCL12)介导的CAR-T细胞“禁锢”现象,从而增强CAR-T细胞在肿瘤中的浸润与定位,解决了其在实体肿瘤中的导航缺陷。研究表明,DV1@O-Colase#CAR-T显著提升了胰腺癌的治疗效果,浸润率相较于游离CAR-T细胞提升约5倍,能够有效消退肿瘤并延长小鼠生存期。
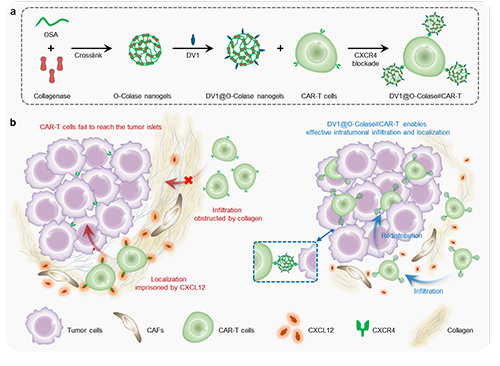
这一胶原酶纳米凝胶背包增强CAR-T细胞疗法的概念为实体肿瘤治疗开辟了新途径。同时,采用化学交联固定酶的策略为纳米凝胶提供了卓越的稳定性和高酶负载能力,展现出作为高效酶递送系统的广泛应用前景。
这项研究为解决CAR-T细胞在实体肿瘤中疗效受限的问题提供了一个创新的解决方案。研究结果有望推动CAR-T细胞疗法在实体肿瘤临床应用中的发展,并为癌症免疫治疗领域的进一步创新奠定基础。团队目前正在进行该方法的临床前研究,积极推进成果的临床转化应用。
栾玉霞教授长期致力于药物递送系统开发及抗肿瘤等生物应用,已在国际期刊发表SCI论文140余篇,包括Nat. Nanotechnol., J. Am. Chem. Soc., Adv. Funct. Mater., ACS Nano,Biomaterials, J. Controlled Release, Nano Lett.等。本研究得到国家自然科学基金的资助,并得到齐鲁医院程玉峰教授以及宋庆旭副主任医师的支持。
原文链接:https://doi.org/10.1038/s41565-025-01924-1
