由于其独特的化学和物理特性,水凝胶近年来在基础研究和生物医学应用中受到越来越多的关注。从水凝胶广义的定义来说,人体软组织的天然细胞外基质 (ECM)是通过千万年生物进化所形成的最佳性能的生物医药水凝胶。很多软组织ECM(如软骨、皮肤、韧带等) 不但具有极为优秀的宏观生物力学性能,可以承载高强度的生物力学荷载,同时还兼具良好的微观结构动态性质,可以有效支持细胞在ECM三维环境中的增殖、迁移、组装、分化、发育等各项细胞行为。尽管经典的、具有静态网络的水凝胶已经在几十年见被广泛报告,但最近研究表明,结构动态水凝胶可以更好地模拟人体组织中天然细胞外基质 (ECM) 的动态特性与功能。但是由于需要维持细胞活性的考量,现有的可负载细胞的水凝胶力学性能普遍较弱。水凝胶的宏观力学性能和其微观的结构动态性质看似是一对相互矛盾的设计要求,因此开发兼具宏观稳定性与微观结构动态性的水凝胶服务于基础及转化生物医学研究是水凝胶研究的重要的挑战之一。

近日,美国约翰霍普金斯大学谷洛(Luo Gu)教授和华南理工大学边黎明教授团队在Chemical Reviews期刊上发表了题为Structurally Dynamic Hydrogels for Biomedical Applications: Pursuing a Fine Balance between Macroscopic Stability and Microscopic Dynamics的综述文章,介绍了动态水凝胶性能的总体预期与设计原则,着重强调了其宏观稳定性与微观动态性之间的良好平衡。本文总结了动态水凝胶设计与制备方式的最新进展,包括从降解依赖性策略到降解非依赖性策略的发展、不同凝胶体系的特性及其在生物医学领域的应用,并在此基础上讨论了动态水凝胶研发与应用中尚存的挑战与新趋势。
首先,软组织ECM的微观动态性是细胞铺展、迁移、增殖、分化等正常生命活动的基础。在人体中,包括脑、肝脏在内的许多重要器官与组织在力学上都表现出应力松弛、蠕变等动态特性。从微观角度来看,不同聚合物链之间可逆相互作用的瞬时破坏与重建通常被认为是ECM重组和产生粘弹性行为的物质基础。ECM这些微观结构的动态性质对所包含细胞的增殖、迁移、分化、发育等各项细胞行为有重要的调控作用。因此,利用动态水凝胶中重现这种动态微观结构对于模拟 ECM的功能至关重要。同时,很多软组织(如软骨、皮肤、韧带等)的ECM都具有非常优良的力学性质,可以承担高强度的反复生物力学载荷。从水凝胶功能的角度来讲,动态水凝胶在体外培养或植入体内后,需要在一定时间内保持整体结构的稳定性及一定的力学强度以维持其特定功能。材料的宏观整体稳定性与微观结构动态性这一对看似矛盾的特性却在软骨、皮肤等软组织的天然ECM中同时得到了完美的呈现。因此,这也是以生物医学应用为导向的动态水凝胶仿生设计的重要目标。此外,动态水凝胶应具有明确定义的化学成分,以提供稳定、可重现的性质。为确保水凝胶的安全应用,相应成分应具有最小的细胞毒性和良好的生物相容性。此外,为应对转化应用的需求,动态水凝胶制备的成本、效益、以及规模化生产的可行性亦应该得到考虑。
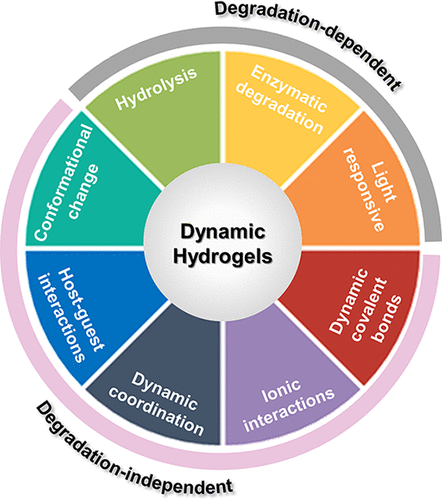
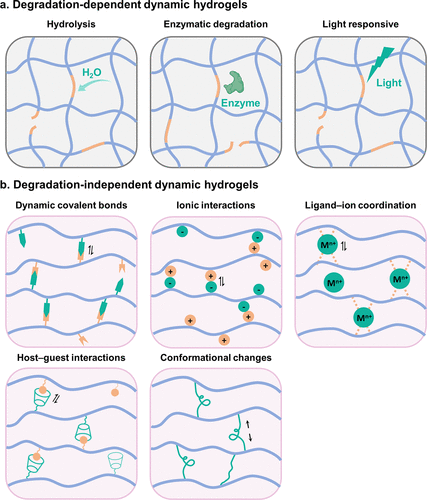
近年来,随着对水凝胶动态行为分子机制的不断了解,研究者们开发了许多有前途的方法来制造水凝胶并调节其动态特性,例如,通过调整聚合物结构或交联方法。根据水凝胶动态性的来源不同,这些方法可以分为两大类:降解依赖性策略以及降解非依赖性策略。前者主要包括水解、酶解、光响应降解等,后者则涵盖了动态共价键、离子(静电)相互作用、动态离子-配体相互作用、主-客体相互作用、动态构型变化、氢键等动态相互作用。
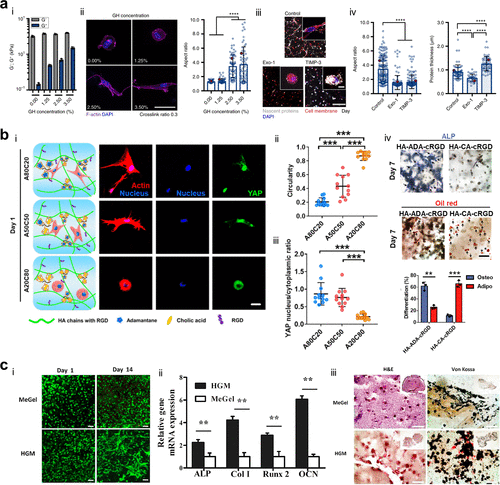
在生物医学应用方面,由于其独特的物理与生化特性,动态水凝胶可以更好地提供细胞三维培养所需动态微环境,并通过水凝胶网络结构的改变或动态相互作用实现生物活性分子的可控递送,因而在细胞/类器官培养、体外肿瘤模型、组织工程、免疫调节和药物递送等方面均得到了广泛的探索与应用。
作者亦在本文中提出了动态水凝胶的进一步发展所面临几个挑战和机遇:(1)需要进一步研发动态交联策略,以拓宽水凝胶网络动态性的时间尺度。(2)考虑到动态水凝胶的功能和应用,其微观动态性和宏观稳定性应该达到更好的平衡。(3)开发先进的方法和技术将有助于在更高分辨率下实时表征水凝胶的动态特性及其对相关细胞行为的影响。(4)需要简化水凝胶制备过程并提升工艺稳定性,从而促进动态水凝胶在基础研究和临床转化中的广泛应用。
本文作者包括约翰霍普金斯大学张琨雨博士、重庆大学冯茜副教授(共同第一作者)、约翰霍普金斯大学博士生方志伟,通讯作者为约翰霍普金斯大学谷洛助理教授与华南理工大学边黎明教授。
原文链接:https://pubs.acs.org/doi/full/10.1021/acs.chemrev.1c00071
通讯作者简介:
谷洛教授于2017年加入约翰霍普金斯大学,任材料科学与工程系助理教授。谷教授实验室着重研究细胞对微环境中力学与生化信号的感知与响应,探索细胞力学信号传导在组织再生、免疫治疗和基因编辑的中的作用与意义,并由此启示的新型生物材料的研发。
边黎明教授2021年入职华南理工大学生物医学科学与工程学院,现任长江学者特聘教授。边教授长期致力于发展先进纳米材料与水凝胶材料在生物医学领域的应用,并且逐渐建立了从基础材料学,生物医学研究到医疗应用研究的多方向的深度研究。边教授课题组近期在高水平学术期刊发表多篇论文。
1. +Peng, X.; +Xia, X., +Xu, X.; Yang, X.; Yang, B.; Zhao, P.; Yuan, W.; *Chiu P.W.R.; *Bian, L. Ultra-fast self-gelling powder mediate robust wet adhesion to promote healing of gastrointestinal perforations. Science Advances, 2021, Vol. 7, no. 23, eabe8739
2. +Yang, B.; +Wei, K.; Loebel, C.; Zhang, K.; Feng, Q.; Li, R.; Wong, D.S.H.; Xu, X.; Lau, C.; Chen, X.; Zhao, P.; Yin, C.; Burdick, J.A.; *Wang, Y.; *Bian, L. Enhanced mechanosensing of cells in synthetic 3D matrix with controlled biophysical dynamics. Nature Communications, 2021, Article number: 3514.
3. +Wong, S.H.D.; +Xu, X.; Chen, X., Xing, Y.; Xu, L.; Lai, N.C.H.; Oh, J.; Wong, R.W.K.; Wang, X.; Han, S.; You, W., Shuai, X.; Wong, N., *Tan, Y.; *Duan, L.; *Bian, L. Manipulation of the nanoscale presentation of integrin ligand produces cancer cells with enhanced stemness and tumorigenicity. Nano Letters, 2021, 21, 7, 3225–3236.
4. +Zhao, P.; +Yang, B.; Xu, X.; Lai, N.C.H.; Li, R.; Yang, X.; *Bian, L. Nanoparticle-assembled vacuolated coacervates control macromolecule spatiotemporal distribution to provide a stable segregated cell microenvironment. Advanced Materials, 2021, 33, 9, 2007209.
5. +Yuan, W.; +Wang, H.; +Fang, C.; Yang, Y.; Xia, X.; Yang, B.; *Lin, Y.; *Li, G.; *Bian, L. Microscopic local stiffening in supramolecular hydrogel network expedites stem cell mechanosensing in 3D and bone regeneration. Materials Horizons, 2021, 8, 1722-1734.
6. +Xu, X.; +Xia, X.; +Zhang, K.; Rai, A.; Li, Z.; Zhao, P.; Wei, K.; Zou, L.; Yang, B.; Wong, W.K.R., *Chiu, P.W.Y.; *Bian, L. Bioadhesive hydrogels demonstrating pH-independent and ultrafast gelation promote gastric ulcer healing in pigs. Science Translational Medicine 2020, 12, 58, eaba8014.
7. Li, R.; Lin, S.; Zhu, M.; Deng, Y.; Chen, X.; Wei, K.; Xu, J.; Li, G.; *Bian, L. Synthetic presentation of noncanonical Wnt5a motif promotes mechanosensing-dependent differentiation of stem cells and regeneration. Science Advances, 2019, 5: eaaw3896.
8. Chen, X.; Li, R; Wong, S.H.D.; Wei, K.; et al.; Xia, J.; Chen, G..; L., G.; *Bian, L. Conformational manipulation of scale-up prepared single chain polymeric nanogels for multiscale regulation of cells. Nature Communications, 2019, volume 10, Article number: 2075.
9. +Kang, H.; +Yang, B.; Zhang, K.; Pan, Q.; Yuan, W.; Li, G.; *Bian, L. Immunoregulation of macrophages by dynamic ligand presentation via ligand-cation coordination. Nature Communications, 2019, volume 10, Article number: 1696.
10. +Kang, H.; + Jung, H.J.; Wong, S.H.D.; Kim, S.K.; Lin, S.; Chan, K.F.; Zhang, L.; Li, G.; Dravid, V.; *Bian, L. Remote control of heterodimeric magnetic nanoswitch regulates the adhesion and differentiation of stem cells. J. Am. Chem. Soc., 2018;140 (18): 5909-5913.
- 西交大魏钊/北大杨根 Small 综述: 力学性能可调动态水凝胶用于3D类器官培养 2025-06-27
- 华南理工大学边黎明教授团队《Biomaterials》: 主客体动态水凝胶促进胚胎干细胞在长期三维培养中的增殖和干性保持 2022-09-22
- 华南理工大学边黎明教授课题组《Nat. Commun.》:超结构动态水凝胶促进干细胞在三维环境中的力学传感与分化 2021-06-17
- 天大崔春燕/刘文广、清华李舟 Sci. Adv.:抗溶胀生物降解水凝胶重塑电微环境驱动脑缺损后内源性神经再生 2026-05-30
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 南通大学孙文旭/张雷团队 AFM:仿生界面工程设计兼具高拉伸与高灵敏度的双纳米复合水凝胶 2026-05-29
- 温医大宋伟宏院士团队包敏课题组全球招聘研究员、副研、博后 - 神经生物学、脑科学、分子/细胞生物学、生物材料学、生物力学、生物信息学 2026-04-17
