在生命科学与医学领域,液-液相分离驱动的无膜细胞器是揭示细胞区室化机制的核心方向。应激颗粒等无膜细胞器通过相分离调控细胞应激响应,其快速组装可保护mRNA和关键蛋白。同时,持续存在的应激颗粒与癌症化疗耐药性相关,索拉非尼等药物疗效因受激颗粒影响显著降低。因此,靶向调控此类无膜细胞器成为克服耐药性的潜在策略。尽管已有针对其成分蛋白或上游通路的小分子药物,但缺乏直接融合无膜细胞器并调节其活性的方法。
针对该挑战,南开大学余志林教授课题组通过发展酶响应相分离多肽YSO4F,制备了具有无膜细胞器靶向的原位相分离凝聚物,实现了无膜细胞器靶向的肿瘤有效治疗。该多肽分子以“粘合子-间隔子-粘合子”为原型,连接病毒来源FGDF结构域以靶向应激颗粒核心蛋白G3BP2。在溶酶体硫酸酯酶催化下,YSO4F转化为相分离多肽YF并形成凝聚液滴,通过与G3BP2结合实现与应激颗粒融合,阻断其对RACK1蛋白的隔离,激活促凋亡通路,显著增强了索拉非尼的抗肿瘤效果,且生物安全性良好。该研究为靶向细胞器的癌症治疗提供了新策略。(图1)
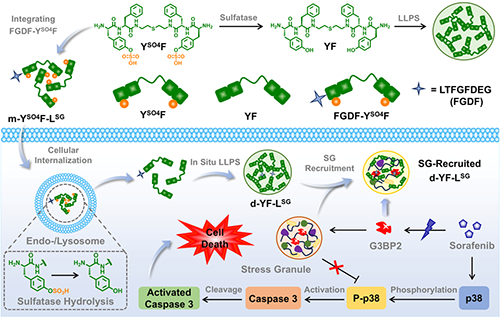
图1.活细胞内多肽原位相分离形成液滴并靶向应激颗粒,与索拉非尼联合进行癌症化疗示意图。图片来源Adv. Mater.。
作者首先介绍了具有原位液-液相分离能力的多肽分子YSO4F的酶响应水解以及酶响应相分离能力。研究团队设计了含双硫酸化酪氨酸的多肽YSO4F,其结构遵循“粘合子-间隔子-粘合子”基序,硫酸化修饰赋予其亲水性及酶响应性。体外实验表明,YSO4F在硫酸酯酶催化下逐步脱去硫酸基团,转化为疏水性多肽YF,进而发生液-液相分离形成球形液滴。荧光漂白恢复及液滴融合实验证实,该液滴具有典型的凝聚体动态特性,半恢复时间为23.4s,表明分子在液滴与胞质间快速交换(图2)。
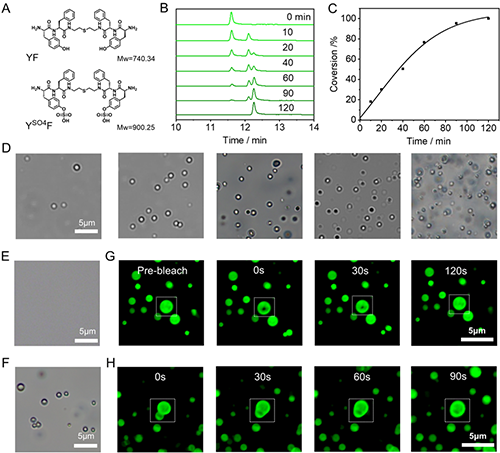
图2.多肽YSO4F溶液中酶响应水解与酶响应相分离行为研究。图片来源Adv. Mater.。
接下来研究团队对细胞内的原位相分离过程进行了进一步研究(图3),研究发现YSO4F通过网格蛋白介导的内吞作用进入细胞,定位于溶酶体后经硫酸酯酶催化去硫酸化,并通过质子海绵效应逃逸至细胞质,最终发生液-液相分离形成液滴。共聚焦激光扫描显微镜显示,胞质内形成的液滴具备典型的液-液相分离特征,其荧光漂白后恢复特性证实了液滴与周围环境中分子的快速交换能力。对照实验显示,当使用硫酸酯酶抑制剂预处理癌细胞,或在不过表达该酶的正常成纤维细胞中,均未观察到液滴形成,充分验证了酶响应是触发原位相分离的关键条件。
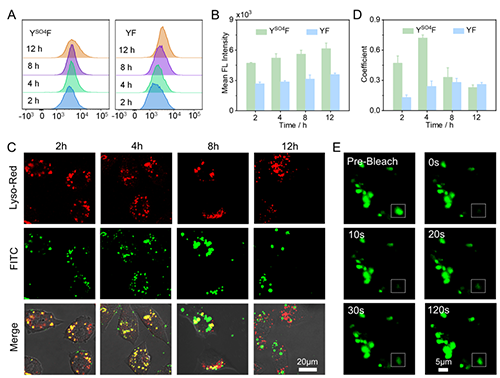
图3.多肽YSO4F癌细胞内原位相分离行为研究。图片来源Adv. Mater.。
在无膜细胞器靶向研究中,研究团队通过引入能特异性结合应激颗粒核心蛋白G3BP2的配体FGDF,成功构建了m-YSO4F-LSG体系。该体系在肿瘤细胞内形成的功能性液滴(d-YF-LSG)可通过配体-蛋白识别作用,与应激颗粒发生特异性融合,实现对这一无膜细胞器的精准靶向。微量热泳动实验表明,液滴微环境使FGDF-YF与G3BP2的结合亲和力提升3.9倍,显著增强了对应激颗粒的募集效果。共聚焦激光扫描显微镜显示,含有应激颗粒靶向配体的m-YSO4F-LSG体系具有优异的应激颗粒靶向能力。当与化疗药物索拉非尼联合使用时,显著提升了化疗药物对肺癌细胞的杀伤效力,使药物半数抑制浓度大幅降低,细胞凋亡率显著升高,为克服肿瘤化疗耐药性提供了关键的作用靶点和增效策略(图4)。
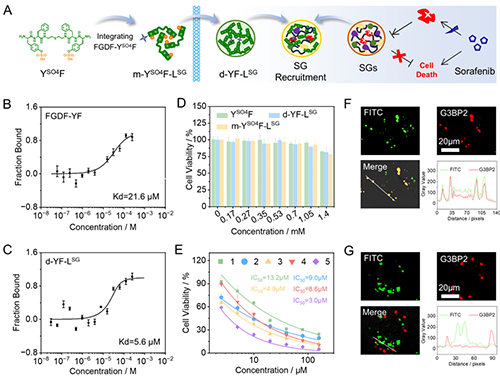
图4.m-YSO4F-LSG对应激颗粒靶向性与化疗增效研究。图片来源Adv. Mater.。
研究团队进一步对化疗增效的机制进行研究,利用共聚焦激光扫描显微镜观察到,经m-YSO4F-LSG处理并联合索拉非尼刺激的肿瘤细胞中,液滴荧光信号与另一种应激颗粒核心组分TIA-1蛋白免疫荧光信号呈现高度共定位,线扫描分析显示两者重叠度显著高于对照组。由于液滴未携带TIA-1靶向配体,这一现象直接证明液滴通过物理融合与应激颗粒结合,而非单个蛋白募集。同时,共聚焦实验结果表明液滴与应激颗粒的融合能够抑制其对RACK1蛋白的隔离。先前的研究表明,应激颗粒主要通过隔离蛋白RACK1并抑制MTK1-SAPK信号通路,从而阻止p38磷酸化和caspase-3活化,促进细胞存活。蛋白印迹实验表明,液滴与应激颗粒的特异性融合触发了MTK1蛋白的磷酸化激活,进而激活p38-MAPK信号通路级联反应,最终导致促凋亡关键因子caspase-3的剪切活化(图5)。
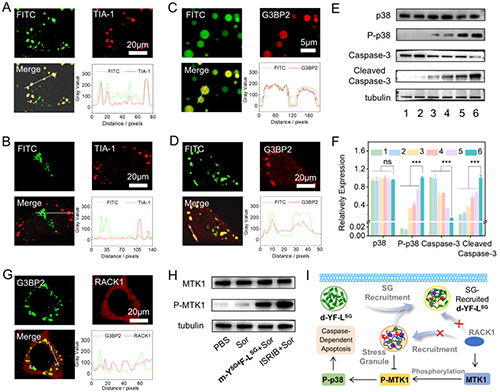
图5.m-YSO4F-LSG的化疗增效机制研究。图片来源Adv. Mater.。
最后,在荷瘤小鼠的体内疗效验证中,研究团队采用瘤内注射m-YSO4F-LSG 联合腹腔注射索拉非尼的治疗方案,结果显示该联合疗法在21天的观察期内实现了显著肿瘤体积抑制,优于单一药物治疗组,展现出强大的协同抗肿瘤效应。免疫荧光分析进一步揭示,肿瘤组织中形成的功能性液滴与应激颗粒核心蛋白 G3BP2的共定位系数高达0.77,直接证实了液滴对应激颗粒的高效靶向能力。蛋白印迹检测显示,联合治疗组中p38磷酸化水平显著升高,同时cleaved caspase-3蛋白表达量大幅增加,明确印证了caspase-3依赖凋亡通路的激活。重要器官的苏木精和伊红(H&E)染色及血液生化分析结果表明,m-YSO4F-LSG体系具有良好的生物相容性。
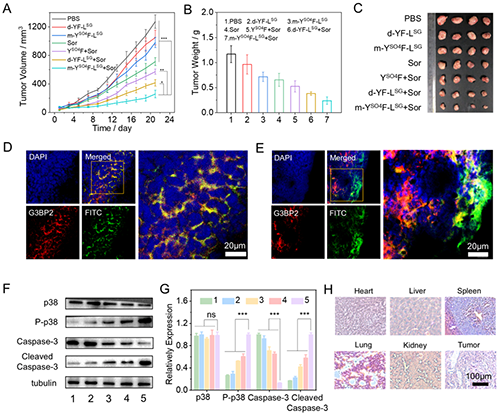
图6.m-YSO4F-LSG的体内抗肿瘤化疗增效与生物安全性研究。图片来源Adv. Mater.。
这一成果近期发表在Advanced Materials上。南开大学硕士研究生王维庶和博士研究生王昊为共同第一作者,南开大学化学学院余志林教授为通讯作者。相关研究得到了科技部重点研发项目、国家自然科学基金委、天津市科技局和海河实验室经费资助。
论文信息:
In Situ Liquid-Liquid Phase Separation of Peptides into Droplets Targeting Membraneless Organelles for Enhanced Cancer Chemotherapy
Weishu Wang, Hao Wang, Zhilin Yu*.
Advanced Materials.
论文链接:https://doi.org/10.1002/adma.202420399
- 港中深张祺/长春应化所段晓征 AFM:原位相分离构筑超强离子凝胶胶粘剂 2024-12-21
- 四川大学金勇教授课题组 CEJ:原位相分离构筑坚韧的多功能疏水离子凝胶 2023-11-04
- 西安交大胡建/北卡州立Michael Dickey《Nat. Mater.》:基于原位相分离制备高强韧可拉伸离子液体凝胶 2022-02-23
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 香港中文大学(深圳)唐本忠团队 Nat. Commun.:均聚多肽自组装体系圆偏振室温磷光 2026-02-24
- 华东理工刘润辉教授课题组 Nat. Commun.:双胍化多肽模拟物抗多药耐药ESKAPE与脑膜炎 2025-12-12
- 吉大杨英威教授团队与合作者 Adv. Sci.:金属有机框架材料用于靶向治疗炎症性肠病 2026-04-07
