生物大分子自组装成纤维状纳米结构是原核生物和真核生物机体内普遍存在的一个生理过程,对细胞的生命活动至关重要。由于形态独特和结构有序、以及具有良好的生物降解性和较低的免疫原性,多肽已经成为生物医学领域的一颗新星,广泛应用于多功能纳米载体的设计中,在抑制肿瘤进展方面显示出巨大的潜力。然而,目前报道的自组装多肽纤维用于生物医药研究存在以下两方面的问题:1)多肽纳米纤维溶解性普遍较差,无法实现直接静脉给药;2)体内生理条件复杂多变,自组装的多肽结构单元在特定靶标部位自组装形成纳米结构的过程不可控。因此,提高纳米纤维的溶解度以及增强纳米纤维自组装的肿瘤微环境响应性是目前亟需解决的一大难题。
基于多肽FFKY结构,通过PEG修饰得到一种具有细胞内还原型谷胱甘肽(GSH)响应的多肽纳米给药系统(PEG-TGA-NapFFKY),并包载化疗药物阿霉素,可在细胞内实现从三维胶束向一维纳米纤维的重组过程,从而发挥协同化疗的作用(图1)。
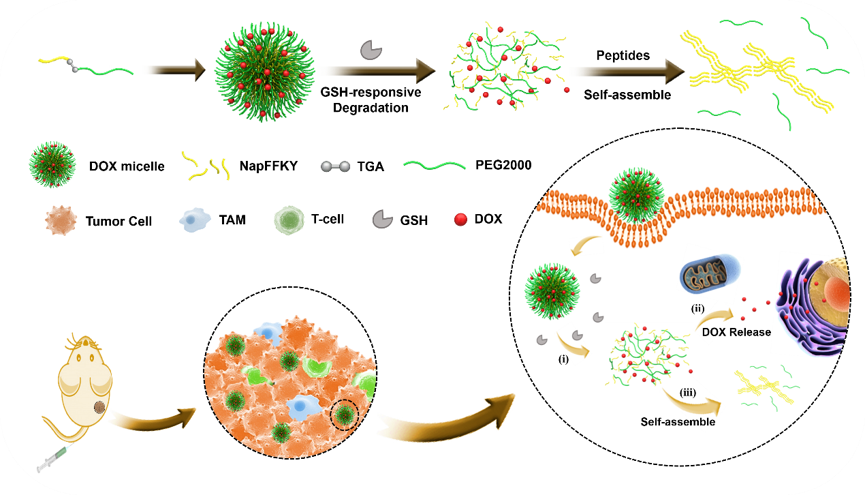
图1. 肿瘤细胞中GSH响应性PEG-TGA-NapFFKY多肽纳米制剂从三维胶束到一维纳米纤维的重组示意图。(i)TGA提供的二硫键发生细胞内高GSH水平响应性断裂。(ii)DOX从胶束中释放后作用于细胞核。(iii)游离多肽单元在细胞内形成自组装的纳米纤维,发挥协同化疗作用。
该纳米制剂具有良好的溶解性,形成的球形胶束粒径为192nm,电位接近中性,载药量可达4.6%,具有良好的分散性。同时,在不同水平均表现出良好的GSH响应性降解及自组装形成纳米纤维的能力;且形成的纳米纤维刚性较强,长度可达2μm左右,呈致密网状结构。作者首先从细胞水平上验证了自组装的多肽纳米纤维能够与阿霉素发挥良好的协同化疗作用,随后作者对其协同化疗作用的机制进行初步探索,通过对细胞表面形态、细胞骨架以及细胞因子等方面的研究,结果如图2所示,纳米纤维由于具有一定刚性,能够对肿瘤细胞细胞表面形态、空间结构、钙离子等相关细胞因子水平产生较为显著的影响,从而抑制肿瘤细胞活性。
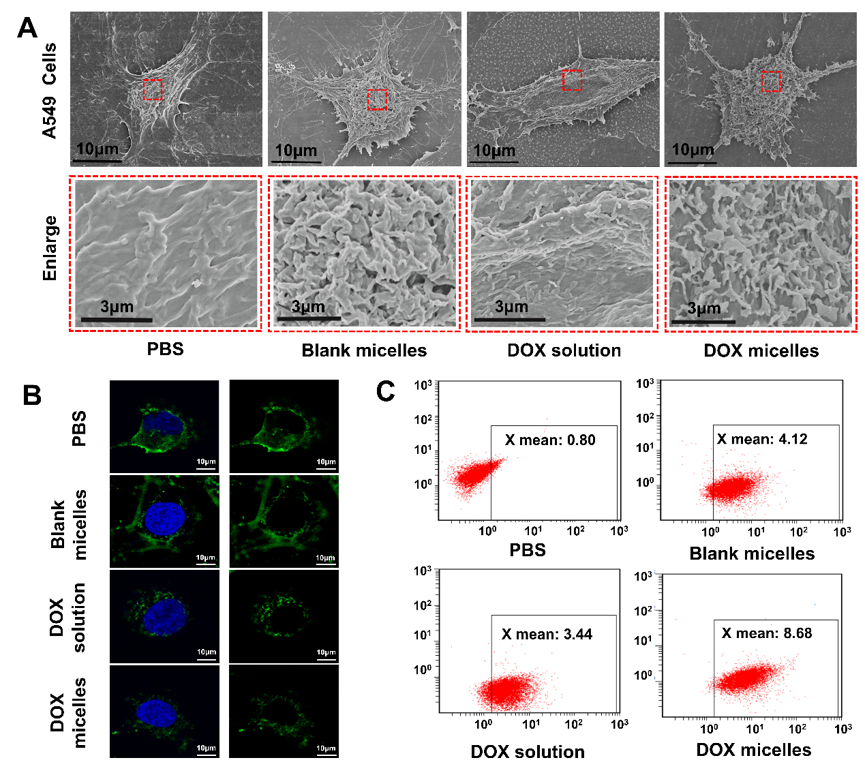
图2. PEG-TGA-NapFFKY多肽纳米制剂协同化疗作用的机制研究。A.肿瘤细胞表面结构形态变化;B. 肿瘤细胞骨架变化;C. 肿瘤细胞内钙离子浓度变化。
基于良好的体外研究成果,作者进行了一系列的体内实验,结果如图3所示,证实PEG-TGA-NapFFKY多肽纳米制剂能够充分借助EPR效应靶向肿瘤组织,且与化疗药物阿霉素发挥出理想的协同抗肿瘤效果。同时,肿瘤组织切片中清晰可见的自组装纳米纤维进一步表明多肽制剂在体内具备良好的GSH响应性降解以及自组装形成纳米纤维的能力,与体外一系列实验结果相一致。这项工作将为新型细胞内酶响应性药物递送系统的合理设计,以及从三维胶束到一维纳米纤维重组的研究,提供新的思路。
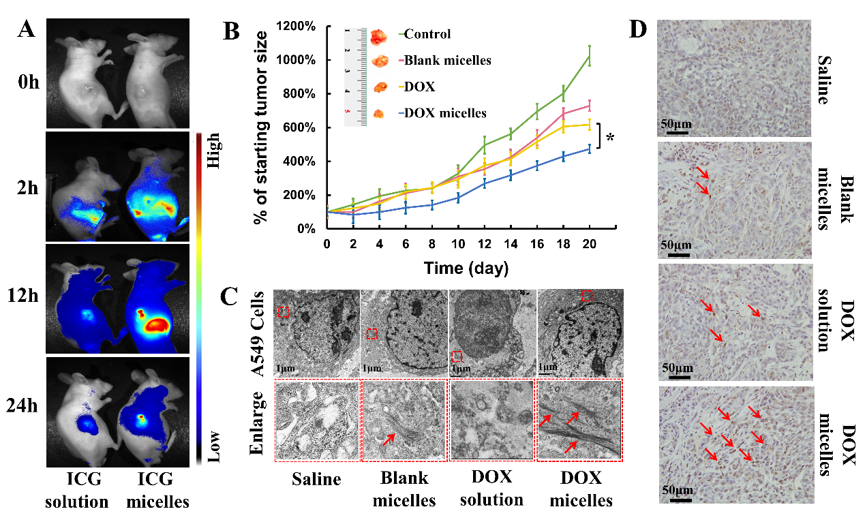
图3. PEG-TGA-NapFFKY多肽纳米制剂的体内分布及抗肿瘤效果。A. 活体荧光分布;B. 体内抑瘤曲线;C. 肿瘤组织切片; D. TUNEL染色。
相关成果以名为《Intracellular Restructured Reduced Glutathione-Responsive Peptide Nanofibers for Synergetic Tumor Chemotherapy》发表在Biomacromolecules(Biomacromolecules 2020 21 (2), 444-453)。论文第一作者为浙江大学药学院硕士生郭望葳,通讯作者为浙江大学药学院韩旻副教授和高建青教授。该项研究工作得到了国家自然科学基金(81673022,81572952, 81373346)等支持。
- 四川大学王云兵/胡成团队 AFM:基于手性活性多肽交联的多功能水凝胶协同缓解氧化应激与纤维化重塑 - 实现心肌梗死精准治疗 2026-05-30
- 香港中文大学(深圳)唐本忠团队 Nat. Commun.:均聚多肽自组装体系圆偏振室温磷光 2026-02-24
- 华东理工刘润辉教授课题组 Nat. Commun.:双胍化多肽模拟物抗多药耐药ESKAPE与脑膜炎 2025-12-12
- 东华大学朱美芳/成艳华团队 Adv. Mater.:轻质热防护材料助力空间离轨与柔性舱展开系统 2026-06-02
- 中国矿业大学 Nat. Commun.:深地深空复杂条件微环境管理多级异质界面纳纤 2026-05-15
- 苏州大学汪晓巧教授、张克勤教授团队 ACS Nano:兼具辐射制冷与空气过滤双功能的螺旋纳米纤维膜 2026-04-30
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
