与传统的癌症治疗方法相比,光热疗法和光动力疗法因其无创性,有效性和较小的副作用而引起了研究者们极大的兴趣。光热疗法(PTT)可以利用光热纳米剂的热量消融肿瘤。然而,温度过高会导致热休克蛋白的过表达,导致癌细胞不能完全凋亡和肿瘤复发,从而削弱PTT效应。另一方面,光动力疗法(PDT)可以产生高毒性的单线态氧(1O2),从而杀死癌症细胞。众所周知,肿瘤内部具有不同的生理环境。在常氧的肿瘤部位,1O2可以破坏细胞和血管以破坏肿瘤,因此,具有中等光热作用和强光动力作用的纳米剂可能是杀死这些部位的细胞和血管的最佳选择。另一方面,在致密肿瘤内部形成了缺氧微环境,这限制了PDT的作用,当PDT与PTT结合使用时,高热可以使致密肿瘤内部的微血管中的氧含量增加,因此,具有强光热和光动力作用的光疗纳米平台可能是消除低氧致密肿瘤内部癌细胞的最佳解决方案。综上所述,需要对材料的光热和光动力效应进行精准调控,从而实现肿瘤的精准治疗。
在前期工作中,黄辉教授团队通过分子设计,分别采用重原子效应策略和D-A结构和扭曲构象结合的策略,得到了一系列具有较强光热效应和光动力效应的有机半导体纳米粒子,并且对小鼠肿瘤具有很好的治疗效果(Small, 2020, 10.1002/smll.202000909;ACS Appl. Mater. Interfaces, 2019, 19, 17884-17893.)。
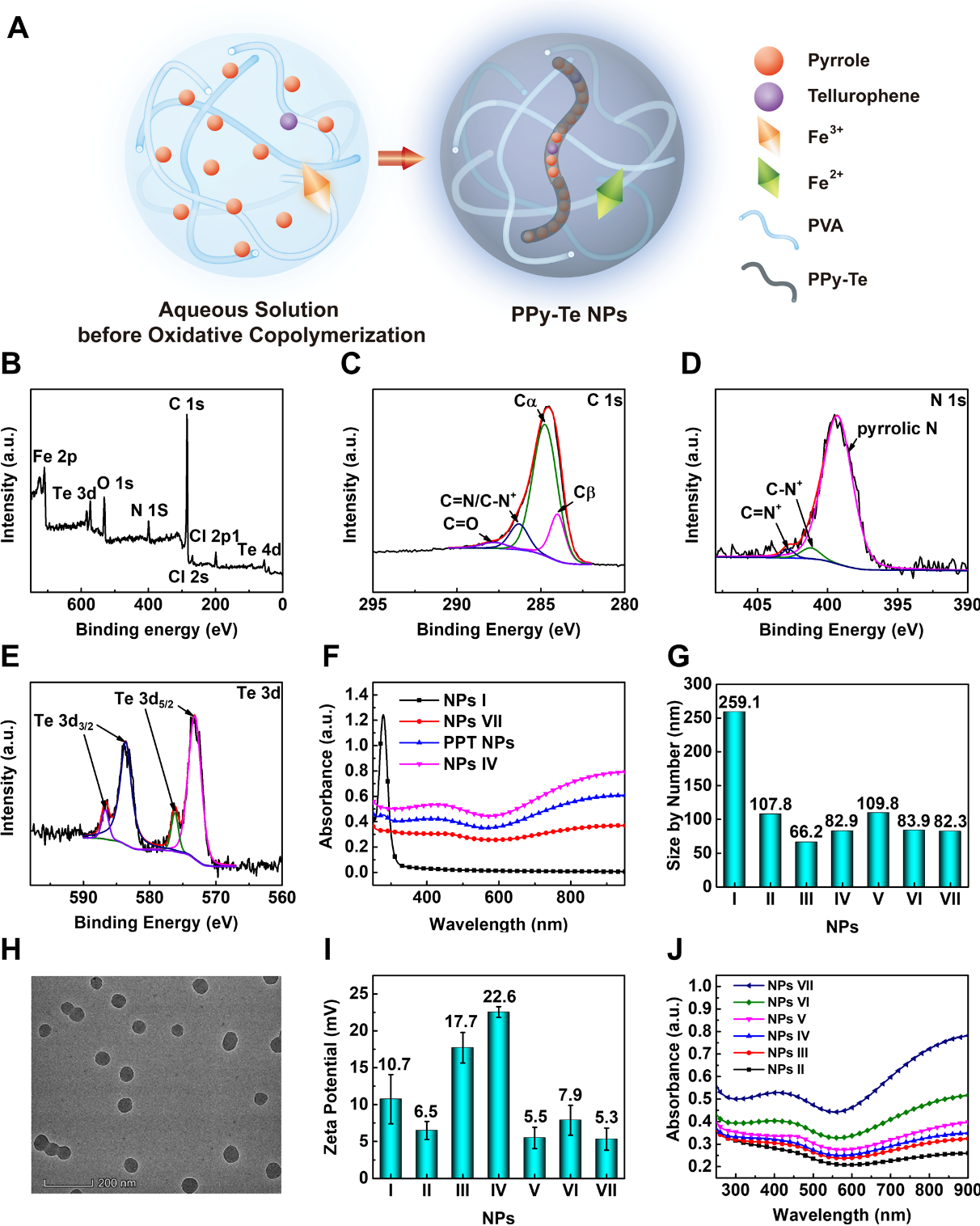
图1(A)PPy-Te NPs的制备示意图。(B-E)蚀刻后的NPs IV的全谱和C 1s,N 1s,Te 3d电子的XPS光谱。(F)NPs I,NPs VII,NPs IV和PPT NPs的UV-Vis-NIR吸收光谱(NPs的浓度为100μg mL-1)。(G)通过DLS测量的NP I-VII的大小。(H)NPs的TEM图像 比例尺,200 nm。(I)通过DLS测量的NPs I-VII的ζ电势。(J)NP II-VII(100μg mL-1)的UV-Vis-NIR吸收光谱。
为了进一步实现光热与光动力学效应的精准调控,黄辉教授带领的研究团队通过受控氧化共聚,原位合成了一系列具有不同比例的吡咯与碲吩的共聚物纳米颗粒。通过X射线光电子能谱以及紫外可见近红外光谱证实了碲吩和吡咯原位共聚合反应的实现。进一步系统研究发现,随着吡咯比例的提高,光热转换效率依次提高,随着碲吩比例的提高,活性氧物种产率增加。因此,通过改变吡咯与碲吩的摩尔比,可以精确而系统地调节半导体纳米剂在近红外一区激光辐射下的光热和光动力效应。动物实验表明,该类纳米粒子对肿瘤具有高效的治疗效果,并且具有良好的生物相容性。因此,这项工作提出了一种简单的方法来调节有机半导体纳米粒子的光热和光动力效应,并成功应用到肿瘤治疗中。
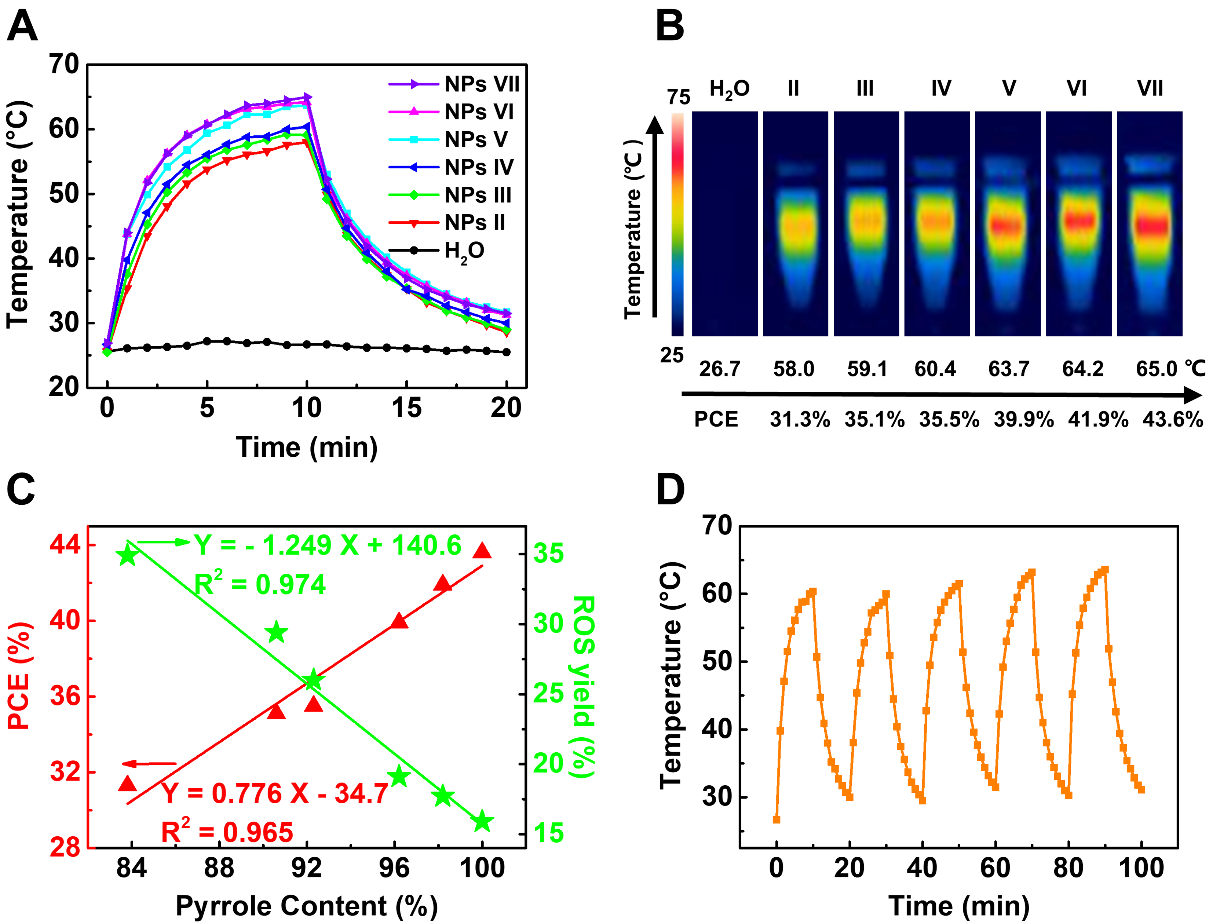
图2(A)NPs II-VII(100μg mL-1)和H2O的温度变化曲线。(B)最高温度下NPs II-VII的红外热图像和由图2A计算得出的NPs II-VII的PCE。(C)NPs II-VII中吡咯含量与PCE,活性氧物种(ROS)产率之间的拟合线。(D)NPs IV光照五个周期的(100μg mL-1)的温度变化曲线。
相关研究成果以《Precisely Tuning Photothermal and Photodynamic Effects of Polymeric Nanoparticles by Controlled Copolymerization》为主题,发表在化学材料领域著名期刊《Angewandte Chemie International Edition》 (Angew. Chem. Int. Ed. ) 上(DOI: 10.1002/anie.202004181)。论文的第一作者为中国科学院大学材料科学与光电技术学院博士生温凯凯,共同第一作者为西南科技大学硕士生吴丽芬,通讯作者为黄辉教授和西南科技大学段涛教授。另外,该工作还得到中山大学第五附属医院马寒教授在动物实验上的大力支持。
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/smll.202000909
https://pubs.acs.org/doi/10.1021/acsami.9b05196
https://onlinelibrary.wiley.com/doi/10.1002/anie.202004181
- 中国人民大学王亚培、贺泳霖/重庆大学卢阳/德累斯顿工业大学冯新亮 Sci. Adv.:具有超稳定自由基的二维共轭MOF实现高效NIR-II光热治疗 2026-05-10
- 天大封伟教授团队 Mater. Today:跨尺度键合作用视角下的光热能转换机制与材料设计 2026-04-21
- 天津大学封伟团队 AFM:氧化石墨烯-熔盐复合材料突破高温光热相变储能瓶颈 2026-04-20
- 南邮周晖/西工大胡文博/山东大学崔基炜/高丽大学 Jong Seung Kim JACS:逃避免疫清除 - 实现可重复光动力治疗 2026-03-18
- 西安交大郭保林/梁永平团队 AFM:光热/光动力协同抗菌与 pH/葡萄糖双重响应药物递送治疗糖尿病足溃疡 2024-11-21
- 华南理工唐本忠院士团队冯光雪教授/南开丁丹教授 ACS Nano:双模态ROS刺激的一氧化碳释放用于光动力和气体肿瘤的协同治疗 2024-11-05
- 华南理工大学杜金志教授、都小姣教授 ACS Nano:可注射“特洛伊木马”水凝胶 - 释放可穿透免疫刺激纳米胶束用于胶质母细胞瘤术后治疗 2026-04-20
